Clear Sky Science · de
Umlagerung des Zytoskeletts durch eine neuartige K6-K14-Keratin‑Fusion fördert Krebsstammzell‑Eigenschaften und zelluläre Plastizität via cGAS‑STING‑Selektion
Wie Gestaltwandler unter Krebszellen ihre Umgebung austricksen
Krebszellen wachsen nicht nur unkontrolliert; sie lernen auch, ihr inneres „Skelett“ gezielt zu verformen, um zu überleben, sich zu verstecken und sich auszubreiten. Diese Studie zeigt, wie ein bestimmter struktureller Defekt in Zellen von Kopf‑ und Hals‑Karzinomen den Zellkern beschädigen, einen eingebauten Gefahrenalarm auslösen, die Zellen in einen ruhenden Zustand drücken und sie schließlich als aggressivere, invasive, stammzellähnliche Zellen zurückkehren lassen kann. Das Verständnis dieses mechanischen Weges der Krebsentwicklung könnte neue Ansätze eröffnen, Rückfälle und Metastasen zu verhindern.
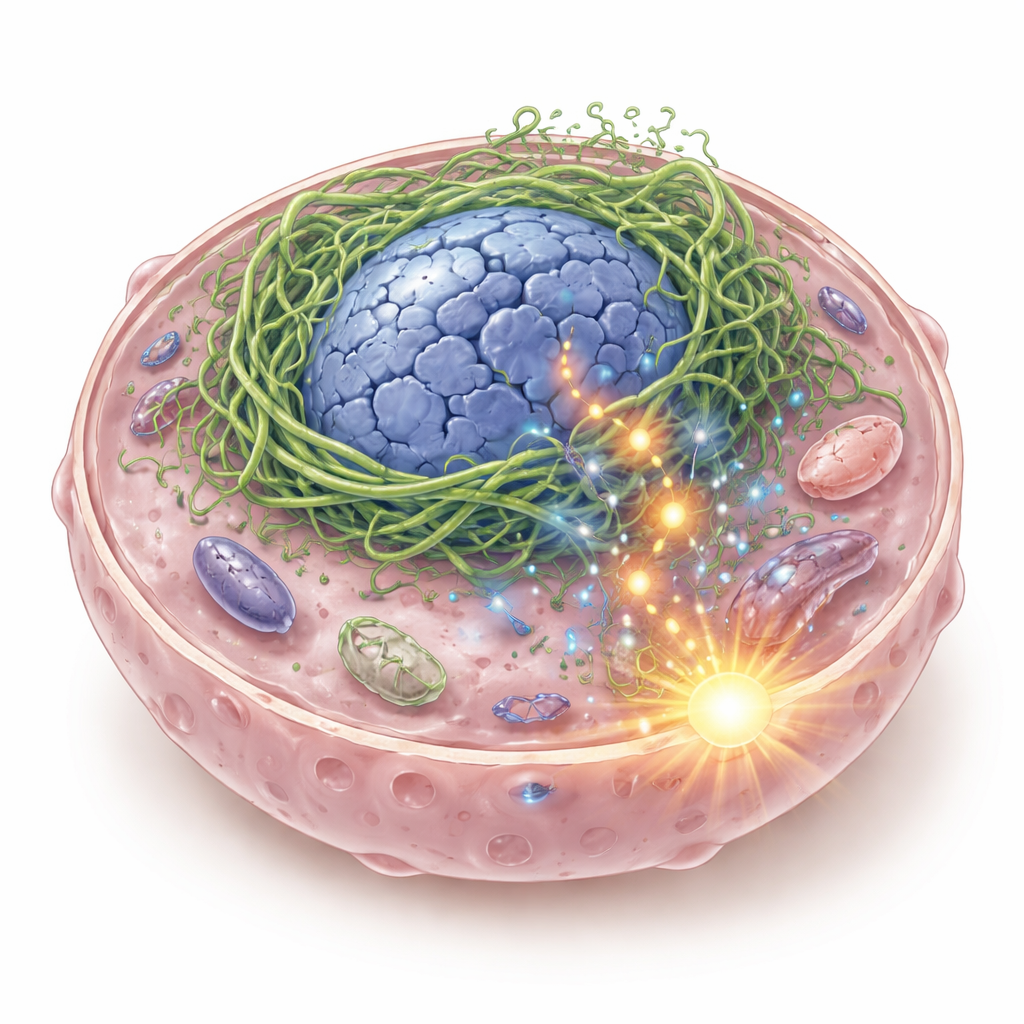
Ein gebrochener innerer Stützapparat mit gefährlichen Folgen
Im Inneren jeder Zelle gibt es ein flexibles Gerüst aus Proteinfilamenten, das Zelle und Zellkern stabilisiert und hilft, physikalische Kräfte wahrzunehmen. Die Autoren konzentrierten sich auf Keratine, eine Familie von Gerüstproteinen, die häufig in Epithelgeweben vorkommen, darunter im Mund‑ und Rachenraum. In einigen Plattenepithelkarzinomen von Kopf und Hals entdeckten sie ein hybrides Keratin, K6‑K14/V5, das entsteht, wenn zwei Keratin‑Gene zusammenführen. Wird dieses Fusionsprotein in Krebszellen exprimiert, bildet es kein gleichmäßiges Stütznetzwerk. Stattdessen verklumpt es sich dicht um den Zellkern, verzerrt ihn zu hohlräumigen, missgestalteten Strukturen und verursacht DNA‑Brüche. DNA‑Fragmente entwichen ins Zellplasma, wo sie von einem immunologischen Sensorsystem namens cGAS–STING erkannt werden, das normalerweise Alarm schlägt, wenn virale DNA vorhanden ist.
Vom Druck zum Zelltod zur verborgenen Überlebensstrategie
Die unmittelbare Folge dieser Kernschädigung ist für die Krebszellen schädlich: ihr Wachstum verlangsamt sich und viele sterben. Ein Teil schafft es jedoch zu überdauern. Diese Überlebenden werden stark von ihrer physischen Umgebung beeinflusst. Auf standardisierten flachen Plastikschalen verschwinden sie allmählich, doch wenn sie in einem weichen Kollagen‑Gel wachsen — näher an der Beschaffenheit von echtem Gewebe — bleiben sie bestehen und treten als neue Population, genannt 3D‑V5‑Zellen, wieder auf. Genexpressionsanalysen zeigen, dass diese Zellen auf den andauernden DNA‑Schadensalarm reagieren, indem sie Autophagie hochfahren, ein Selbstreinigungsprogramm, das beschädigte Zellbestandteile, insbesondere fehlerhafte Mitochondrien, recycelt. Diese Reaktion hilft ihnen, in einen ruhenden, wenig aktiven Zustand zu gelangen, der ihnen ermöglicht, Stress zu überstehen, statt ausgeschaltet zu werden.
Ruhende Zellen verdrahten sich um und bereiten die Bewegung vor
Im Ruhestatus schreiben diese überlebenden Zellen stillschweigend ihre inneren Programme um. Sie verändern die Zusammensetzung der Keratine und nehmen einen „partiellen“ epithelial‑mesenchymalen Übergang (pEMT) an — eine Zwischenidentität, die einige epitheliale Merkmale bewahrt, aber Flexibilität und Motilität verleiht. Sie werden deutlich besser darin, Kugeln zu bilden und neue Zellkolonien zu begründen, ein Kennzeichen von Krebsstammzell‑Eigenschaften. Mit der Zeit erholen sich ihre mechanischen Eigenschaften: Sie versteifen ihre Kerne wieder, bauen starke Aktinfasern auf und entwickeln lange Fortsätze, die die umgebende Matrix ertasten und greifen. Zudem erhöhen sie die Aktivität von Matrix‑Metalloproteinasen (MMPs), Enzymen, die das extrazelluläre Netz zersetzen und Wege für die Invasion öffnen.
Kommunikation mit Nachbarzellen zum Aufbau einer unterstützenden Nische
Diese umprogrammierten Krebszellen handeln nicht allein. Das Team beobachtete, dass 3D‑V5‑Zellen große Mengen winziger Pakete, sogenannter extrazellulärer Vesikel, in ihre Umgebung freisetzen. Wenn diese Vesikel benachbarte orale Fibroblasten — Bindegewebszellen — erreichen, ändern die Fibroblasten ihre Genaktivität und ähneln stärker Krebs‑assoziierten Fibroblasten, die das Tumorwachstum unterstützen. Viele der ausgetauschten Signale drehen sich um die FGF–FGFR‑Achse, eine Familie von Wachstumsfaktoren und ihren Rezeptoren, die Zellproliferation, Plastizität und Resistenz fördern. Sowohl in Zellkulturen als auch in Maus‑Tumoren verringerte die Blockade der FGFR‑Aktivität diesen Wachstumsvorteil. In Versuchstieren waren Tumoren aus 3D‑V5‑Zellen schlecht differenziert, invasiver, reich an Stammzell‑Markern und eher geneigt, über die Injektionsstelle hinaus zu streuen.
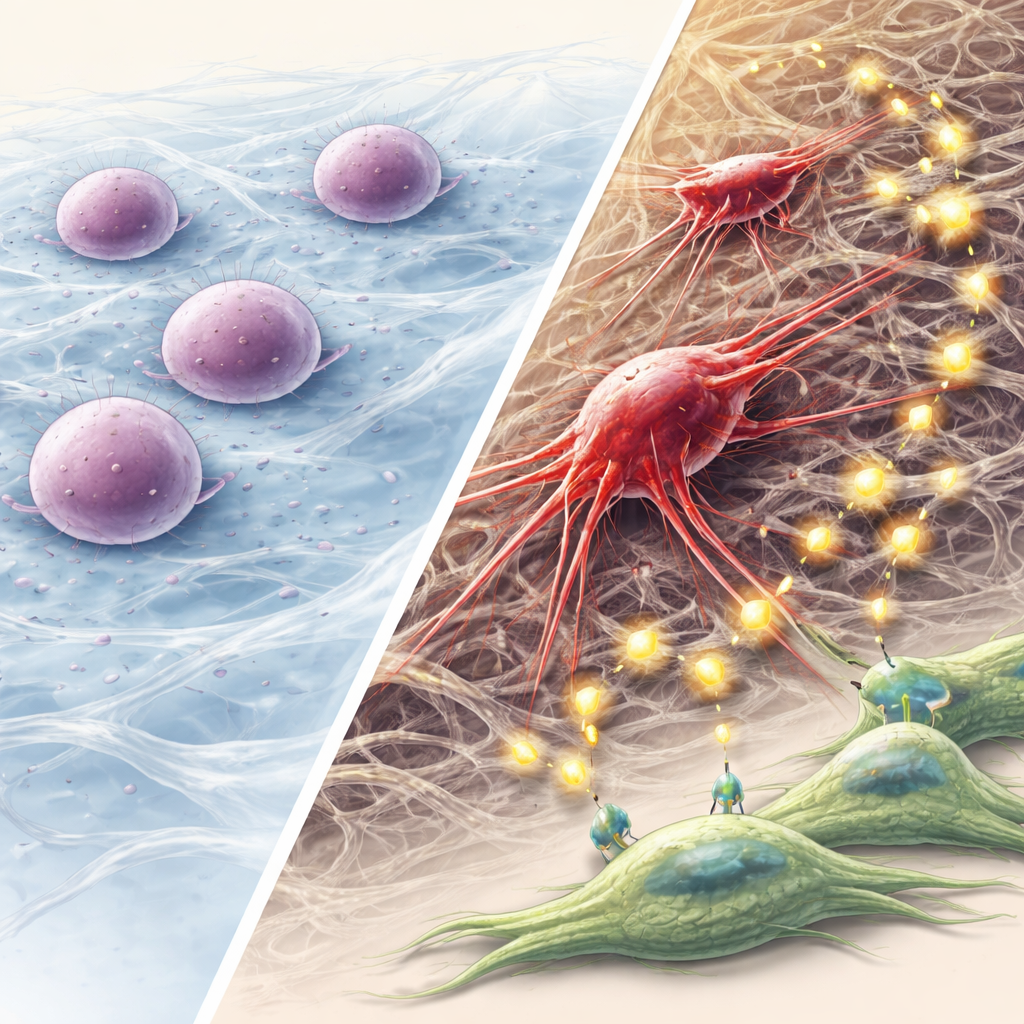
Warum dieser mechanische Pfad zu aggressivem Krebs wichtig ist
Diese Arbeit schlägt ein schrittweises Modell vor: Eine Keratinfusion stört das innere Zellgerüst, quetscht den Zellkern und löst einen DNA‑Schadensalarm aus; Autophagie ermöglicht es dann einigen Zellen, in Dormanz zu gehen statt zu sterben; im Laufe der Zeit reorganisieren diese Überlebenden ihr Skelett, erwerben stammzell‑ und invasionsähnliche Eigenschaften und gestalten ihre Umgebung durch Vesikel und FGF‑Signale um. Für Nicht‑Spezialisten ist die Kernbotschaft, dass physikalische Kräfte und Strukturproteine innerhalb der Zelle genauso wichtig sein können wie Gene und chemische Signale für die Förderung der Krebsentwicklung. Die gezielte Intervention in diesen mechanischen Stress–Autophagie–FGF‑Signalweg, insbesondere bei Kopf‑ und Hals‑Tumoren mit Keratinfusionen, könnte neue Strategien bieten, um ruhende Tumorzellen daran zu hindern, wieder aktiv zu werden und zu streuen.
Zitation: Chen, IH., Ravichandran, S., Lai, MT. et al. Cytoskeleton reorganization induced by a novel K6-K14 keratin fusion promotes cancer stemness and cellular plasticity via cGAS-STING selection. Oncogenesis 15, 5 (2026). https://doi.org/10.1038/s41389-026-00598-1
Schlüsselwörter: Krebsstammzell‑Eigenschaften, zelluläres Zytoskelett, Tumor‑Dormanz, Kopf‑ und Hals‑Krebs, Mechanotransduktion