Clear Sky Science · de
Die Rolle der Histondemethylase PHF2 als Tumorsuppressor beim hepatozellulären Karzinom durch Regulation von SRXN1
Warum diese Studie zu Leberkrebs wichtig ist
Leberkrebs gehört zu den tödlichsten Krebsarten weltweit, und verfügbare Medikamente verlängern das Leben vieler Patientinnen und Patienten nur moderat. Diese Studie stellt eine andere Frage: Statt die üblichen krebstreibenden Gene ins Visier zu nehmen, lässt sich die Art und Weise nutzen, wie DNA in Leberzellen verpackt und chemisch markiert ist, um neue, präzisere Behandlungsoptionen zu finden? Die Forschenden konzentrieren sich auf ein wenig bekanntes Protein namens PHF2 und zeigen, wie es helfen könnte, Leberzellen davor zu bewahren, krebsartig zu werden.
Auf der Suche nach Schwachstellen im Kontrollsystem des Krebses
Krebs wird nicht nur von defekten Genen angetrieben; zugrunde liegen oft fehlerhafte „epigenetische“ Kontrollen — die chemischen Markierungen und Proteinkomplexe, die bestimmen, welche Gene an- oder abgeschaltet sind. Beim hepatozellulären Karzinom, der häufigsten Form von Leberkrebs, sind viele solcher Regulatoren gestört. Das Team testete systematisch 497 epigenetische Regulatoren in sechs Leberkrebszelllinien, indem sie RNA-Werkzeuge verwendeten, um jeweils einen Regulator vorübergehend zu reduzieren, und anschließend maßen, wie gut die Krebszellen überlebten. Dieser große Screen sollte offenbaren, auf welche Regulatoren Krebszellen zum Wachsen angewiesen sind und welche normalerweise als Bremse für die Tumorbildung wirken.
Neue Krebsförderer und -schützer finden
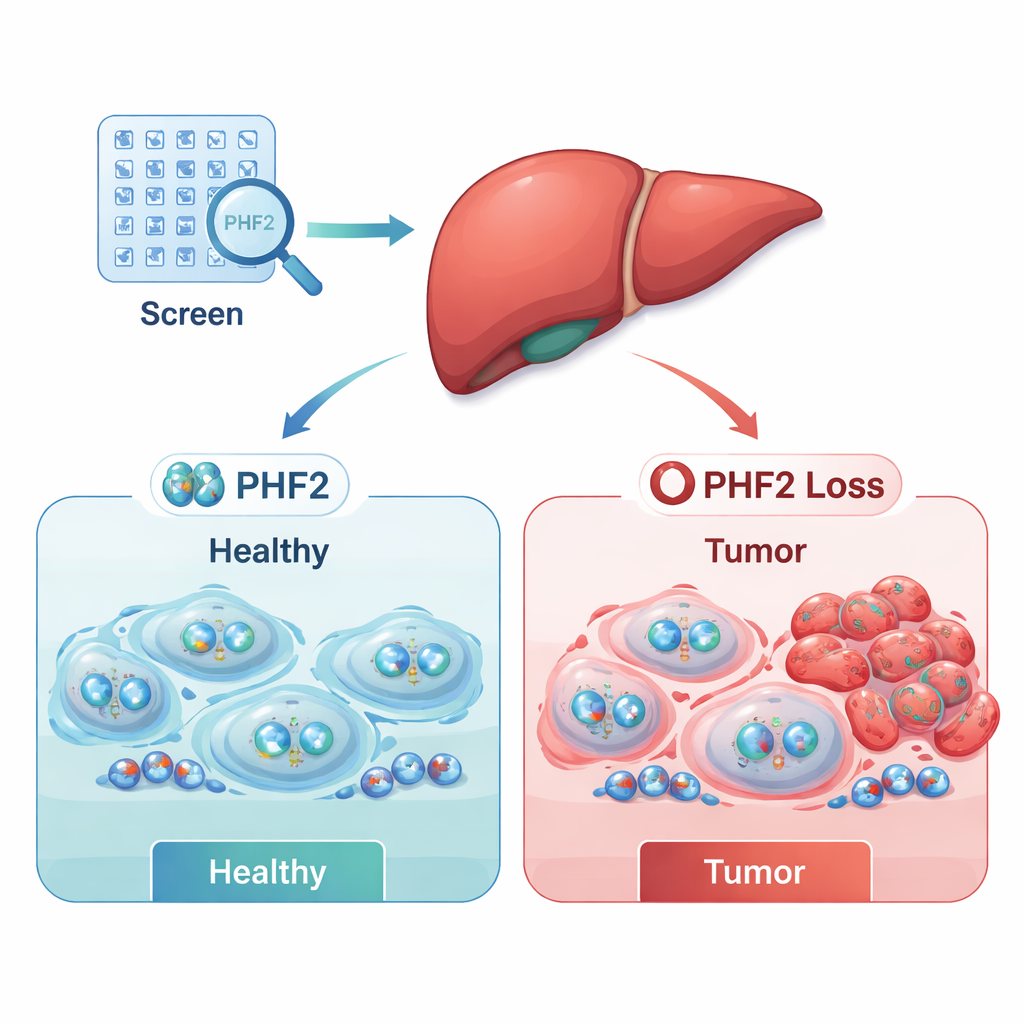
Der Screen zeigte zwei große Gruppen: potenzielle Krebs-„Beschleuniger“ (Onkogene), deren Verlust das Überleben der Krebszellen beeinträchtigte, und potenzielle „Bremsen“ (Tumorsuppressoren), deren Verlust das Zellwachstum förderte. Durch die Kombination ihrer Labordaten mit großen öffentlichen Patientendatensätzen reduzierten die Forschenden die Liste auf einige klinisch relevante Kandidaten. Zwei Regulatoren, SUPT7L und SMARCC1, zeigten in Tumoren tendenziell erhöhte Aktivität und standen mit schlechterer Überlebensprognose in Verbindung. Im Gegensatz dazu war ein Regulator — PHF2 — in Lebertumoren häufig weniger aktiv, und Patientinnen und Patienten, deren Tumoren höhere PHF2-Spiegel aufwiesen, lebten im Allgemeinen länger. Diese Muster deuteten darauf hin, dass PHF2 beim menschlichen Leberkrebs als Tumorsuppressor wirken könnte.
Wie der Verlust von PHF2 Leberkrebszellen verändert
Um PHF2 näher zu untersuchen, erzeugte das Team Leberkrebszellen, die dauerhaft weniger von diesem Protein produzierten, und verfolgte ihr Verhalten über die Zeit. Zellen mit reduziertem PHF2 wuchsen schneller und zeigten höhere Werte des Proliferationsmarkers Ki-67, was darauf hinweist, dass PHF2 normalerweise die Zellteilung hemmt. Diese Effekte waren in bereits aggressiven Leberkrebszelllinien am ausgeprägtesten, was nahelegt, dass der Verlust von PHF2 allein das Krebsentstehen möglicherweise nicht initiiert, aber das Wachstum maligner Zellen nach Tumorbildung beschleunigen kann.
Eine überraschende Verbindung zu zellulären Stressabwehren
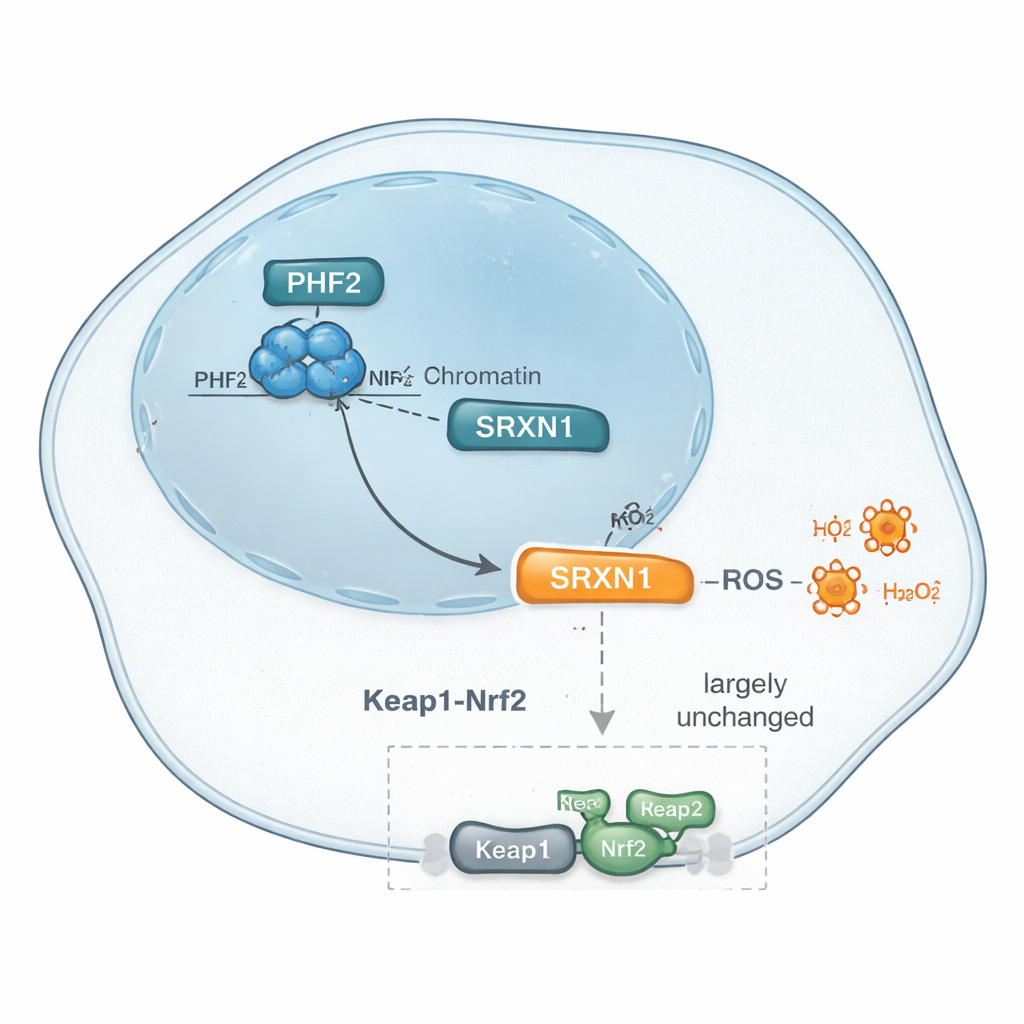
Anschließend nutzten die Forschenden moderne Proteomik-Verfahren, um Tausende von Proteinen zu katalogisieren, deren Mengen sich veränderten, wenn PHF2 reduziert wurde. Zwischen vielen subtilen Verschiebungen stach ein Muster hervor: Die Spiegel eines stressschützenden Proteins namens SRXN1 sanken konsequent, wenn PHF2 verloren ging. SRXN1 hilft Zellen, reaktive Sauerstoffspezies zu managen — chemisch reaktive Nebenprodukte, die DNA und Proteine schädigen können, aber auch Krebszellen zu Anpassungen zwingen. Die Daten deuteten darauf hin, dass PHF2 zur Aufrechterhaltung von SRXN1-Spiegeln beiträgt und dass die Veränderung dieses Gleichgewichts beeinflussen könnte, wie Leberkrebszellen auf inneren Stress reagieren und schließlich wie schnell sie wachsen.
Wirken abseits eines bekannten Stresswegs
SRXN1 wird normalerweise von einem zentralen Stressantwort-Regler namens Nrf2 gesteuert, der viele antioxidative Gene einschaltet, wenn Zellen oxidativem Stress ausgesetzt sind. Da SRXN1 sank, wenn PHF2 unterdrückt wurde, prüfte das Team, ob PHF2 einfach über diesen bekannten Nrf2-Weg wirkt. Sie untersuchten Schlüsselgene und -proteine im Zusammenhang mit Nrf2, behandelten Zellen mit Wirkstoffen, die Nrf2 durch Blockade seines Inhibitors Keap1 aktivieren, und setzten genetische Werkzeuge ein, um Keap1 direkt zu reduzieren. In all diesen Tests verhielt sich die Reaktion von PHF2-defizienten Zellen ähnlich wie die von normalen Zellen, und breit angelegte Pfad- und Transkriptionsfaktoranalysen hoben Nrf2 nicht als Hauptakteur hervor. Stattdessen traten andere Faktoren, darunter ZNF384 und Nrf1 — beide zuvor mit Leberkrebs in Verbindung gebracht — als Kandidaten hervor. Zusammen legen die Befunde nahe, dass PHF2 die Kontrolle über SRXN1 und antioxidative Antworten möglicherweise unabhängig von klassischem Nrf2-Signalweg ausübt und auf eine eigene Stressregulationsroute in diesen Tumoren hinweist.
Was das für künftige Therapien bedeuten könnte
Für Nichtfachleute ist die Kernbotschaft, dass diese Studie PHF2 als vielversprechenden Schutzfaktor bei Leberkrebs identifiziert: Wenn PHF2 vorhanden und aktiv ist, wachsen Tumorzellen langsamer; ist es vermindert, gewinnen sie Wachstumsvorteile und verändern, wie sie mit zellulärem Stress umgehen. Da PHF2 selbst mit konventionellen kleinen Molekül-Wirkstoffen schwer direkt zu beeinflussen sein könnte, weisen die Autoren auf neuere Strategien wie RNA-basierte Therapien oder Wirkstoffe hin, die PHF2 über vorgelagerte Signalkomponenten stärken. Sie betonen auch, dass die Effekte von PHF2 kontextabhängig sind — seine Wirkung kann mit anderen Mutationen wie dem p53-Status variieren — sodass jede künftige Therapie wahrscheinlich eine sorgfältige Auswahl der Patientinnen und Patienten erfordern würde. Insgesamt verfeinert die Arbeit unser Verständnis dafür, wie epigenetische Regulatoren das Verhalten von Leberkrebs prägen, und eröffnet neue Wege, Therapien zu entwickeln, die PHF2s tumorsuppressive Wirkung wiederherstellen oder nachahmen.
Zitation: Thng, D.K.H., Hooi, L., Yong, W.K. et al. The role of histone demethylase PHF2 as a tumour suppressor in hepatocellular carcinoma by regulating SRXN1. Oncogenesis 15, 6 (2026). https://doi.org/10.1038/s41389-026-00597-2
Schlüsselwörter: hepatozelluläres Karzinom, epigenetische Regulation, PHF2, SRXN1, Therapie bei Leberkrebs