Clear Sky Science · de
Rab37-vermittelte OPN-Sekretion reichert SPP1+ Makrophagen durch autokrine–parakrine Signalgebung an und treibt das Fortschreiten von Lungenkrebs voran
Wie Immunzellen heimlich LungenTumoren beim Wachsen helfen können
Lungenkrebs entsteht nicht isoliert. Er wächst in einer belebten Nachbarschaft aus Immunzellen und Bindegewebe, wobei vermeintliche Verteidiger sich manchmal zu Verbündeten wandeln. Diese Studie zeigt, wie ein kleines Transportprotein in Immunzellen, genannt Rab37, bestimmten Makrophagen hilft, ein Molekül namens Osteopontin (OPN) zu sezernieren und so eine tumorfreundliche Umgebung schafft, die Lungenkrebs aggressiver und schwerer behandelbar macht.
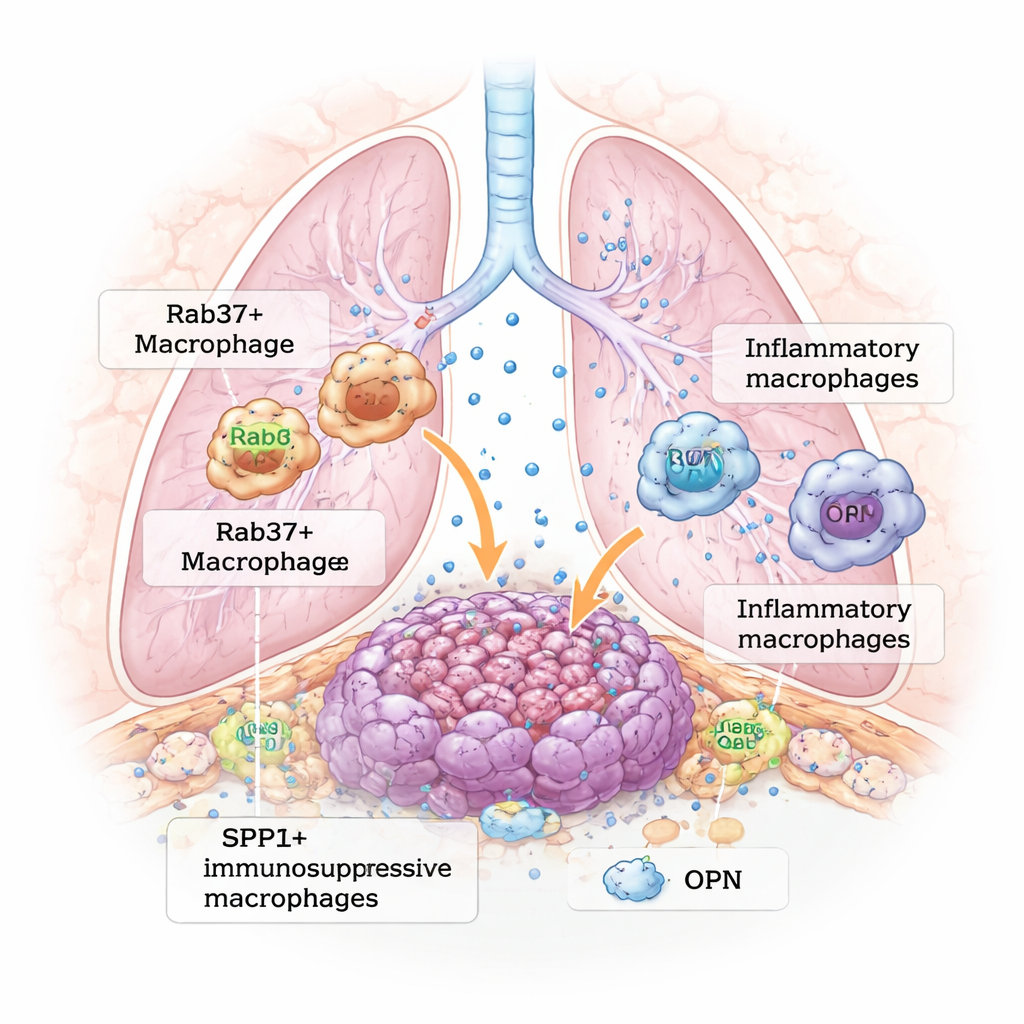
Eine geschäftige Nachbarschaft innerhalb eines LungenTumors
Moderne Krebsforschung zeigt, dass Tumoren eher komplexe Ökosysteme als einfache Ansammlungen entarteter Zellen sind. Um LungenTumoren herum senden Immunzellen, Blutgefäße und Stützgewebe ständig chemische Signale aus. Unter diesen spielen Makrophagen—Immunzellen, die normalerweise Infektionen und Zelltrümmer beseitigen—oft eine Rolle als „tumorassoziierte Makrophagen“. Statt den Krebs anzugreifen, verlagern sich viele dieser Zellen in eine fürsorgliche Funktion: Sie dämpfen Immunreaktionen und unterstützen Tumorwachstum und -ausbreitung. Die zentrale Frage, die dieses Papier angeht, lautet: Was treibt Makrophagen in diesen schädlichen, tumorfördernden Zustand?
Zwei Makrophagen-Typen: Helfer und Hemmer
Die Forscher nutzten Einzelzell-RNA-Sequenzierung, eine Technik, die die Aktivität tausender Gene in einzelnen Zellen erfasst, um die Immunzelllandschaft in MauslungenTumoren zu kartieren. Sie verglichen normale Mäuse mit Mäusen, denen Rab37 fehlte. In Tumoren normaler Mäuse fanden sie viele Makrophagen mit hoher Expression des Gens SPP1, das das Protein Osteopontin (OPN) produziert. Diese SPP1+ Makrophagen bildeten eine immunsuppressive, tumorfördernde Population. Im Gegensatz dazu hatten Tumoren von Rab37-Knockout-Mäusen weniger SPP1+ Makrophagen und mehr Makrophagen, die ein anderes Gen, THBS1, exprimierten — verbunden mit einer entzündlicheren, potenziell tumorhemmenden Reaktion. In humanen Lungenkrebsproben war zu beobachten, dass Patienten, deren Tumoren viele Makrophagen mit CD163-, Rab37- und OPN-Positivität enthielten, eher ein Rezidiv erlitten und eine schlechtere Überlebenswahrscheinlichkeit hatten, was darauf hindeutet, dass dieser spezifische Makrophagen-Typ klinisch gefährlich ist.
Das Geheimversand-Protein, das OPN auflädt
Rab37 gehört zu einer Proteinfamilie, die kontrolliert, wie Zellen Moleküle verpacken und freisetzen. Das Team zeigte, dass Rab37 OPN in kleinen Vesikeln innerhalb von Makrophagen verlädt und dessen Freisetzung nach außen antreibt. Wenn Makrophagen funktionales Rab37 hatten, sekretierten sie deutlich mehr OPN, insbesondere wenn sie Signalen von Lungenkrebszellen ausgesetzt waren. Wurde Rab37 entfernt oder seine Aktivität blockiert, fiel die OPN-Freisetzung stark ab. Die Studie deckte außerdem eine Rückkopplungsschleife auf: freigesetztes OPN aktiviert das Signalkonzeptor-Protein STAT3 in Makrophagen, was wiederum die Aktivität des SPP1-Gens steigert und Makrophagen weiter in einen M2-ähnlichen, tumorfördernden Zustand drängt. Diese Schleife hält die Zellen in einer pro-tumoralen Identität gefangen und sorgt dafür, dass weiterhin mehr OPN produziert wird.
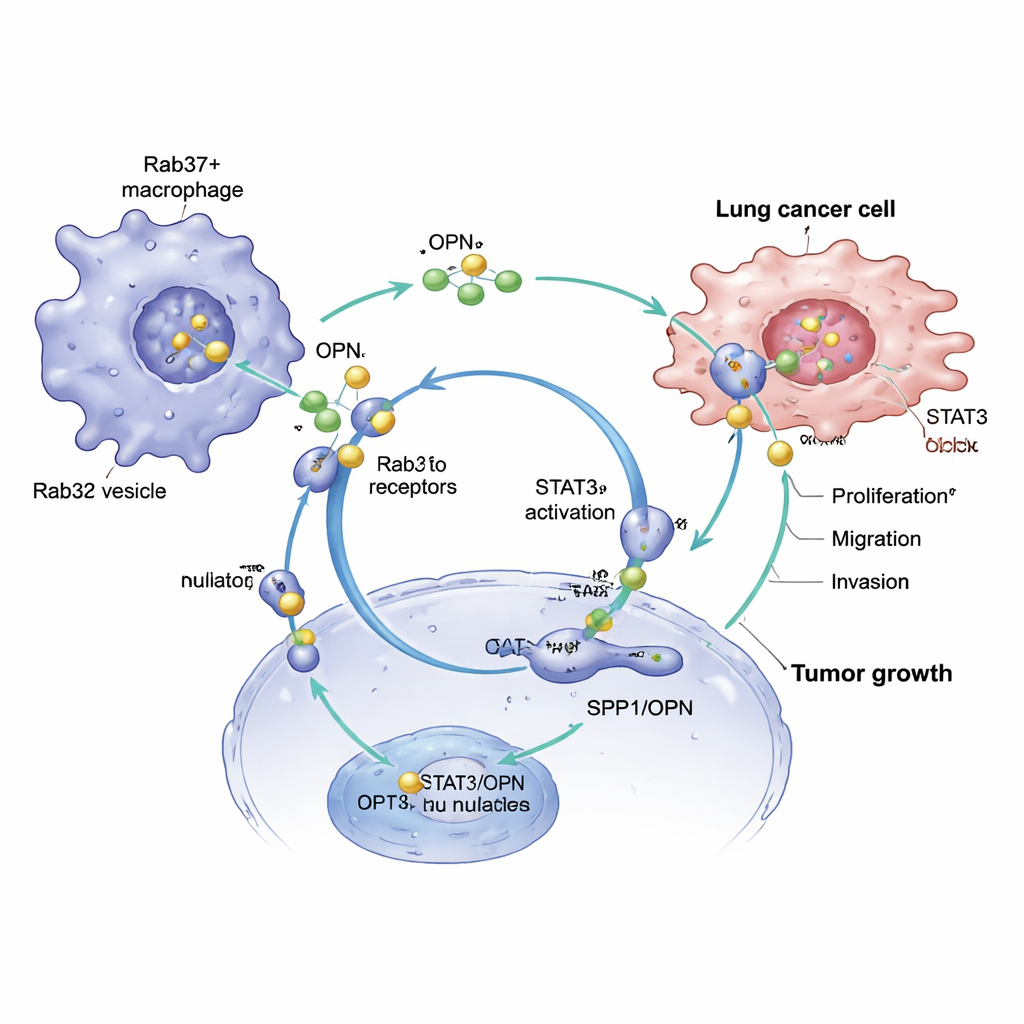
Von ImmunSignalen zu schneller wachsender Tumoren
OPN wirkt nicht nur auf Makrophagen — es kommuniziert auch direkt mit Krebszellen. Wenn Lungenkrebszellen in Medium kultiviert wurden, das von Rab37-positiven Makrophagen stammte, wuchsen sie schneller und wurden beweglicher und invasiver. Das Blockieren von OPN in diesem Medium verringerte diese Effekte, während das Hinzufügen von gereinigtem OPN sie wiederherstellte. Derselbe Rab37–OPN–STAT3-Kreislauf, der Makrophagen umprogrammiert, aktiviert auch Wachstums- und Überlebenswege in Lungenkrebszellen und fördert Proliferation, Migration und Invasion in das umliegende Gewebe. Auf diese Weise hilft ein einzelnes sezerniertes Molekül sowohl, das Verhalten von Immunzellen umzugestalten, als auch das Tumorwachstum zu beschleunigen.
Aus einer Entdeckung eine therapeutische Chance machen
Für Nicht-Spezialisten ist die Kernbotschaft: Einige Immunzellen innerhalb von LungenTumoren werden zu „Doppelagenten“, und Rab37 ist ein zentraler Koordinator ihres Verrats. Indem es Makrophagen hilft, OPN zu sezernieren und eine OPN-getriebene Rückkopplungsschleife aufrechtzuerhalten, fördert Rab37 eine stille, tolerante Umgebung, in der Tumoren gedeihen und sich ausbreiten können. Patienten, deren Tumoren reich an Rab37+/OPN+ Makrophagen sind, haben schlechtere Prognosen, sodass dieser Zelltyp sowohl als Warnsignal als auch als potenzielles Therapieziel dienen könnte. Therapien, die OPN blockieren, STAT3 stören oder Rab37s Transportfunktion hemmen, könnten Makrophagen wieder in eine antitumorale Richtung wenden und Lungenkrebs gegenüber bestehenden Behandlungen, einschließlich Immuntherapien, verwundbarer machen.
Zitation: Yang, YE., Lin, YA., Ling, LL. et al. Rab37-mediated OPN secretion enriches SPP1+ macrophages through autocrine–paracrine signaling to drive lung tumor progression. Oncogenesis 15, 4 (2026). https://doi.org/10.1038/s41389-026-00596-3
Schlüsselwörter: Lungenkrebs, Tumormikroumgebung, Makrophagen, Osteopontin, STAT3-Signalgebung