Clear Sky Science · de
TRIM21-vermittelte Degradation von HILPDA überwindet die Resistenz gegen Anti-PD-1-Immuntherapie bei Brustkrebs durch Begrenzung der Palmitoylierung von PD-L1
Warum einige Krebs-Immuntherapien aufhören zu wirken
Medikamente, die das Immunsystem entfesseln, wie Anti–PD‑1-Therapien, haben die Behandlung mehrerer Krebsarten revolutioniert, darunter auch aggressive Formen von Brustkrebs. Dennoch sprechen viele Tumoren entweder gar nicht an oder finden mit der Zeit Wege, zu entkommen. Diese Studie untersucht eine solche Fluchtroute beim triple-negativen Brustkrebs und zeigt, wie die Umprogrammierung des Tumor-Fettstoffwechsels — und ein umgewidmetes Medikament namens Fenretinid — die Tür für das Immunsystem wieder öffnen könnten, wenn die Standard-Immuntherapie versagt. 
Ein versteckter Helfer, der Tumoren schützt
Die Forschenden konzentrierten sich auf ein wenig bekanntes Protein namens HILPDA, das zuvor mit der Handhabung von Fetten in Zellen unter Stress in Verbindung gebracht wurde. Beim Vergleich von Mäuse-Brusttumoren, die gegenüber Anti‑PD‑1 empfindlich blieben, mit Tumoren, die resistent geworden waren, stellten sie fest, dass die HILPDA-Spiegel in den resistenten Krebsarten deutlich erhöht waren. Analysen großer Patientendatenbanken und Tumorproben von Frauen mit Brustkrebs bestätigten, dass HILPDA in Tumoren stärker vertreten ist als im normalen Brustgewebe, besonders bei triple-negativem Krankheitsverlauf, und dass Patientinnen mit höherer HILPDA-Expression tendenziell schlechtere Prognosen haben. Tumoren von Personen, die keinen Nutzen aus PD‑1‑blockierenden Medikamenten zogen, wiesen ebenfalls mehr HILPDA auf, was dieses Protein direkt mit Therapieversagen verknüpft.
Wie Tumoren die Immunlandschaft gegen uns wenden
Um zu verstehen, was HILPDA in Tumoren tatsächlich bewirkt, veränderte das Team Brustkrebszellen so, dass sie das Protein entweder vermehrt produzierten oder es nicht mehr exprimierten, und kultivierte sie dann mit menschlichen Immunzellen oder in Mäusen. Bei hohen HILPDA-Werten zogen Tumoren vermehrt regulatorische T-Zellen, myeloid-abgeleitete suppressorische Zellen und M2-ähnliche Makrophagen an — Immunzelltypen, die Angriffe abschwächen und dem Krebs helfen, sich zu verbergen. Gleichzeitig nahmen Anzahl und Aktivität von zytotoxischen CD8-T-Zellen und natürlichen Killerzellen ab, und ihre Fähigkeit, toxische Moleküle und entzündliche Signale freizusetzen, war gedämpft. Die Stilllegung von HILPDA kehrte dieses Szenario um: Tumoren zeigten weniger suppressive Zellen, mehr aktive Killerzellen, verlangsamtes Wachstum und weniger Metastasen. Entscheidend war, dass Tiere mit HILPDA-armen Tumoren nach Anti‑PD‑1-Behandlung stärkeres Tumorschrumpfen und längeres Überleben zeigten — ein Beleg dafür, dass HILPDA die Wirksamkeit der Immuntherapie steuert.
Fettproduktion, molekulare Panzerung und Immunflucht
Tiefergehende Untersuchungen enthüllten, wie HILPDA den Tumorstoffwechsel umbaut, um die Immunabwehr zu verfestigen. In Krebszellen bindet HILPDA an ein Chaperon-Protein namens HSP90, um einen Transkriptionsfaktor, KLF5, zu stabilisieren, der die Fettsynthese antreibt. Dieses Trio steigert die Bildung von Fettsäuren, vor allem Palmitat, und füllt Tumorzellen mit Lipidtropfen. Eine dieser Fettsäuren wird dann an PD‑L1 gebunden, das Checkpoint-Protein, das auf der Tumorzelloberfläche sitzt und Immunzellen das Signal „nicht angreifen“ sendet. Die Forschenden zeigten, dass die Anheftung von Palmitat an eine bestimmte Stelle von PD‑L1 wie ein molekularer Klebstoff wirkt: Sie stabilisiert PD‑L1 in der Zellmembran und verhindert seinen Abbau. Die Mutation dieser einzelnen Bindungsstelle beraubte PD‑L1 seiner Stabilität und schwächte seine Schutzfunktion, selbst bei hohem HILPDA. Anders ausgedrückt: HILPDA-getriebene Fettproduktion liefert eine chemische Modifikation von PD‑L1, die den immunhemmenden Schild des Tumors von brüchig zu verstärktem Schutz macht.
Die eingebaute Bremse, die betätigt werden kann
Jeder Beschleuniger braucht eine Bremse — hier ist diese Bremse ein weiteres Protein namens TRIM21. Die Autorinnen und Autoren fanden heraus, dass TRIM21 HILPDA erkennt und es mit molekularen „Markierungen“ versieht, die es zur Abbau-Maschinerie der Zelle schicken. In Brusttumoren von Patientinnen waren die TRIM21-Spiegel tendenziell niedrig, wenn HILPDA hoch war, und niedrige TRIM21-Werte standen mit schlechten Ergebnissen in Verbindung, was darauf hindeutet, dass dieses natürliche Bremssystem in Krebs oft geschwächt ist. Das Team suchte dann nach Wirkstoffen, die TRIM21 stärken könnten, und identifizierte Fenretinid, ein Retinoid, das bereits beim Menschen getestet wurde. In Zell- und Tiermodellen des triple-negativen Brustkrebses steigerte Fenretinid die TRIM21-Aktivität, beschleunigte den Abbau von HILPDA, reduzierte die Fettsynthese und die schützende Modifikation von PD‑L1 und verlangsamte Tumorwachstum und -ausbreitung. Am bemerkenswertesten war, dass die Kombination von Fenretinid mit Anti‑PD‑1-Therapie Tumoren anfälliger für Immunangriffe machte, die Zahl zytotoxischer T‑ und natürlicher Killerzellen erhöhte und zugleich suppressive Zellen im Tumormikromilieu verringerte. 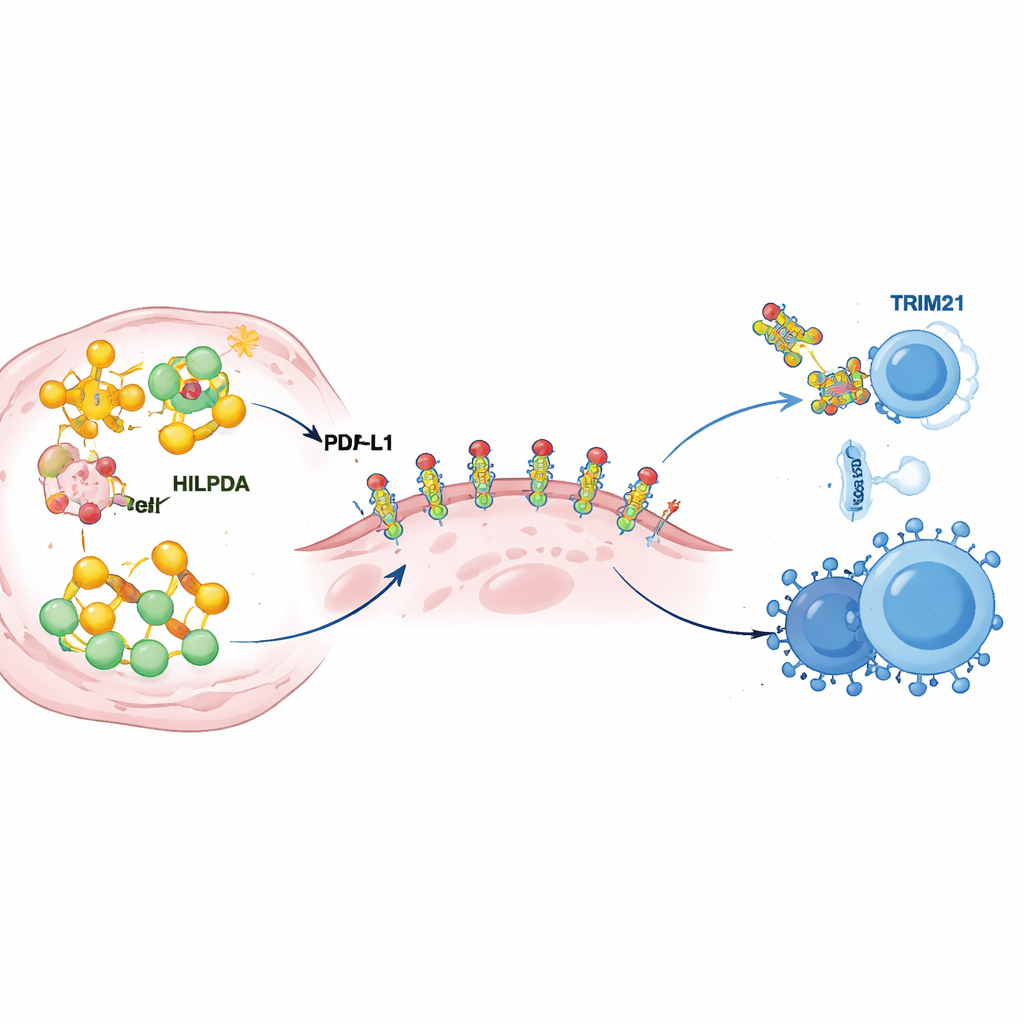
Was das für die zukünftige Krebsbehandlung bedeutet
Diese Arbeit beschreibt eine Abfolge, in der gestresste Brustkrebszellen HILPDA hochregulieren, die Fettproduktion ankurbeln und PD‑L1 chemisch auf ihrer Oberfläche verstärken, sodass sie Immunzellen weiterhin unterdrücken können — selbst gegenüber PD‑1‑blockierenden Wirkstoffen. TRIM21 fungiert als innere Schutzvorrichtung, die HILPDA abbauen kann, ist in Tumoren aber oft zu schwach. Die Erkenntnis, dass Fenretinid dieses Schutzsystem reaktivieren kann, weist auf einen praktischen Weg hin, ein Stoffwechselmedikament mit bestehender Immuntherapie zu kombinieren, um Resistenzen zu überwinden. Wenn dies in klinischen Studien bestätigt wird, könnte die gezielte Beeinflussung der TRIM21–HILPDA–PD‑L1-Achse Patientinnen mit schwer behandelbarem triple-negativem Brustkrebs eine zweite Chance auf Nutzen durch immunbasierte Therapien geben.
Zitation: Wang, X., Li, G., Wu, J. et al. TRIM21-mediated degradation of HILPDA overcomes anti-PD-1 immunotherapy resistance in breast cancer by limiting PD-L1 palmitoylation. Oncogene 45, 1338–1356 (2026). https://doi.org/10.1038/s41388-026-03728-6
Schlüsselwörter: triple-negativer Brustkrebs, Resistenz gegen Immuntherapie, PD-L1-Palmitoylierung, Tumorlipidstoffwechsel, Fenretinid