Clear Sky Science · de
Cereblon (CRBN) hemmt die Metastasierung von Prostatakrebs durch negative Regulation der 6‑Phosphogluconat‑Dehydrogenase (6PGD)
Warum diese Forschung wichtig ist
Wenn Prostatakrebs von der Prostata in andere Organe streut, wird die Behandlung deutlich schwieriger und die Erkrankung ist oft tödlich. Diese Studie zeigt, wie ein wenig bekanntes zelluläres "Qualitätskontroll"‑Protein, Cereblon (CRBN), die Ausbreitung von Prostatakrebs hemmt, indem es ein Stoffwechselenzym abbaut, das aggressives Verhalten antreibt. Das Verständnis dieses eingebauten Bremsmechanismus legt neue Wege nahe, um Metastasen zu verlangsamen oder zu verhindern, insbesondere bei schwer behandelbaren Formen der Erkrankung.
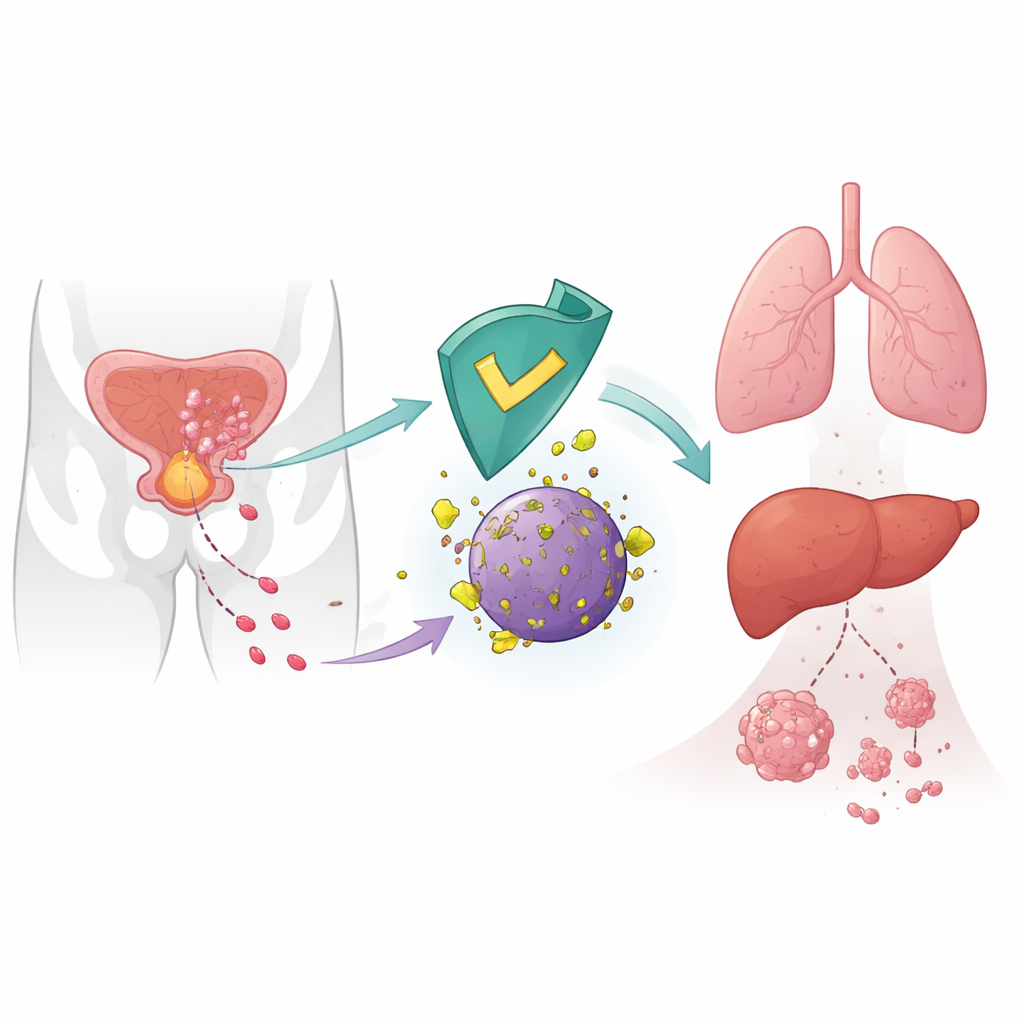
Eine interne Bremse gegen Krebsausbreitung
Krebszellen streuen nicht zufällig; sie verdrahten ihre innere Maschinerie um, um zu wandern, einzudringen und entfernte Organe zu besiedeln. Die Autoren konzentrierten sich auf CRBN, ein Protein, das vor allem als Ziel von Wirkstoffen wie Thalidomid in Blutkrebserkrankungen bekannt ist. In gesunden Zellen ist CRBN Teil einer molekularen Entsorgungseinheit, die bestimmte Proteine zur Zerstörung markiert. Frühere Arbeiten deuteten darauf hin, dass niedrige CRBN‑Spiegel in Tumoren mit schlechteren Ergebnissen verknüpft sind, doch seine direkte Rolle bei der Metastasierung war unklar. Hier zeigen die Forschenden, dass CRBN als natürlicher Unterdrücker der Prostatakrebs‑Ausbreitung wirkt, indem es das Stoffwechselenzym 6‑Phosphogluconat‑Dehydrogenase (6PGD) zum Abbau markiert.
Ein Stoffwechselmotor, den Krebs kapert
6PGD sitzt in einem Stoffwechselweg, der als oxidative Pentosephosphat‑Kaskade bekannt ist und Zellen hilft, NADPH zu erzeugen — ein Molekül, das sowohl Bausteine als auch antioxidative Kapazität liefert. Viele Tumoren steigern diesen Weg, um schneller zu wachsen und Stress besser zu tolerieren. Das Team fand, dass Prostatatumorproben von Patienten tendenziell weniger CRBN und mehr 6PGD aufweisen als normales Prostatasgewebe, und dass dieses Ungleichgewicht besonders ausgeprägt in aggressiven Erkrankungen ist. In Prostatakrebs‑Zelllinien führte das Herunterregeln von CRBN oder dessen Abbau durch eine Designverbindung zu erhöhten 6PGD‑Proteinspiegeln und Enzymaktivität sowie zu gesteigertem NADPH. Die Wiederherstellung von CRBN hatte den gegenteiligen Effekt, senkte 6PGD und NADPH, ohne die zugrunde liegende 6PGD‑Genbotschaft zu verändern, was auf eine Kontrolle auf Proteinebene hinweist.
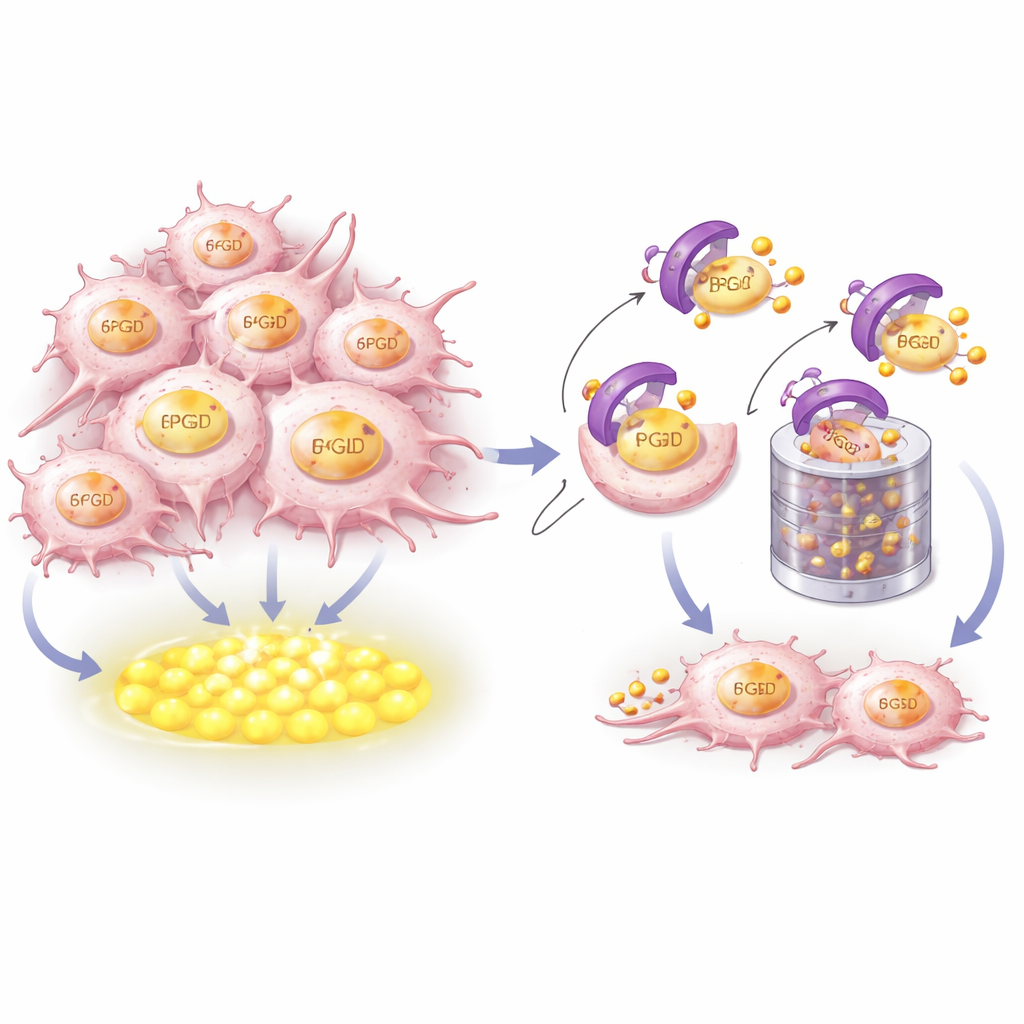
Wie CRBN die Energiequelle erkennt und zerstört
Um zu verstehen, wie CRBN 6PGD kontrolliert, kombinierten die Forschenden Strukturmodellierung mit biochemischen Experimenten. Sie zeigten, dass CRBN physisch ein kurzes, hochkonserviertes helikales Segment nahe dem C‑Ende von 6PGD greift. Schlüsselaminosäuren beider Proteine bilden eine enge Andockstelle. Wenn diese Kontaktpunkte verändert wurden, konnte CRBN 6PGD nicht mehr binden, die kleinen Ubiquitin‑Marken anbringen, die es für den Abbau markieren, oder es zum zellulären Schredder, dem Proteasom, schicken. Bemerkenswerterweise ist diese Erkennungsfläche getrennt von der Tasche, an die immunmodulierende Medikamente CRBN binden, was bedeutet, dass die Kontrolle von 6PGD durch CRBN Teil seiner nativen Haushaltsfunktion ist und nicht durch ein Medikament induziert wird.
Vom veränderten Stoffwechsel zu wandernden Zellen
Die Folgen dieses molekularen Handschlags zeigen sich im Verhalten der Zellen. In Prostatakrebszellen ohne CRBN gingen erhöhte 6PGD‑ und NADPH‑Werte mit gesteigerter Beweglichkeit und Invasion durch künstliche Barrieren einher — Kennzeichen metastatischer Potenz. Als CRBN überexprimiert wurde, wurden die Zellen weniger mobil und invasiv, obwohl sich ihre Wachstumsrate nicht veränderte. Die Genexpressionsanalyse zeigte, dass CRBN die Spiegel von CDH1 erhöhte, das mit eng gepackten epithelialen Zellen assoziiert ist, und die Spiegel von MMP1 senkte, das mit Gewebeabbau und Migration verbunden ist. Wichtig ist, dass diese Änderungen eine direkte CRBN–6PGD‑Bindung erforderten und durch Blockade der 6PGD‑Enzymaktivität umkehrbar waren, wodurch Änderungen im Stoffwechsel mit Änderungen im metastatischen Verhalten verknüpft wurden.
Belege aus Tiermodellen und anderen Krebsarten
Das Team testete diese Konzepte in Mäusen, indem es Prostatakrebszellen in den Blutkreislauf oder die Milz injizierte. Zellen, die so verändert wurden, dass sie zusätzliches CRBN produzierten, bildeten deutlich weniger metastatische Knötchen in Leber und Lunge als Kontrollzellen, was eine antimetastatische Rolle in lebenden Organismen bestätigt. Mäuse, denen CRBN fehlte, zeigten höhere 6PGD‑Proteinspiegel in mehreren Organen. Ähnliche Muster traten in Glioblastom‑, Lungen‑ und Nierenkrebs‑Zelllinien auf: Die Entfernung von CRBN erhöhte 6PGD und förderte Zellbewegung und Invasion, während eine genetische oder medikamentöse Hemmung von 6PGD dieses aggressive Verhalten bremste. Diese Beobachtungen deuten darauf hin, dass die CRBN–6PGD‑Bremse für Metastasen nicht auf Prostatakrebs beschränkt ist.
Was das für künftige Behandlungen bedeuten könnte
Insgesamt schlägt die Studie vor, dass CRBN als metabolischer Torwächter dient, der die Energieversorgung einschränkt, die Krebszellen benötigen, um sich zu lösen, zu wandern und neue Tumoren zu säen. Wenn CRBN verloren geht oder niedrig ist, akkumuliert 6PGD, die NADPH‑Produktion steigt an und Zellen neigen eher zu Veränderungen, die Metastasen begünstigen. Für Patientinnen und Patienten eröffnet dies zwei Möglichkeiten: Die Messung von CRBN‑ und 6PGD‑Spiegeln könnte Tumoren mit hohem Metastasierungsrisiko identifizieren, und Therapien, die CRBN‑Funktion stärken — oder selektiv 6PGD in CRBN‑armen Tumoren dämpfen — könnten neue Ansätze bieten, um das Fortschreiten von Prostata‑ und anderen Krebsarten zu verlangsamen oder zu verhindern.
Zitation: Guchhait, K., Yoon, HS., An, HS. et al. Cereblon (CRBN) inhibits prostate cancer metastasis by negatively regulating 6-phosphogluconate dehydrogenase (6PGD). Oncogene 45, 1234–1246 (2026). https://doi.org/10.1038/s41388-026-03717-9
Schlüsselwörter: Metastasierung von Prostatakrebs, Krebsstoffwechsel, Cereblon, 6PGD‑Enzym, NADPH‑Weg