Clear Sky Science · de
L1TD1 fördert das Fortschreiten des kolorektalen muzinösen Adenokarzinoms durch Erhöhung der Stabilität von ABCC3-mRNA
Warum dieser schleimreiche Krebs wichtig ist
Kolorektales Karzinom ist weltweit eine führende Todesursache durch Krebs. Innerhalb dieser Erkrankung sticht ein besonderer Subtyp hervor: das muzinöse Adenokarzinom, dessen Tumoren mit dickem Schleim gefüllt sind, der mehr als die Hälfte der Tumormasse ausmachen kann. Diese schleimige Barriere kann den Krebszellen helfen, sich vor Chemotherapie und Abwehrmechanismen des Körpers zu verbergen. Die Studie stellt eine grundlegende, aber entscheidende Frage: Was steuert die Schleimbildung, und lässt sie sich stoppen, um das Tumorwachstum zu verlangsamen und Behandlungen wirksamer zu machen?
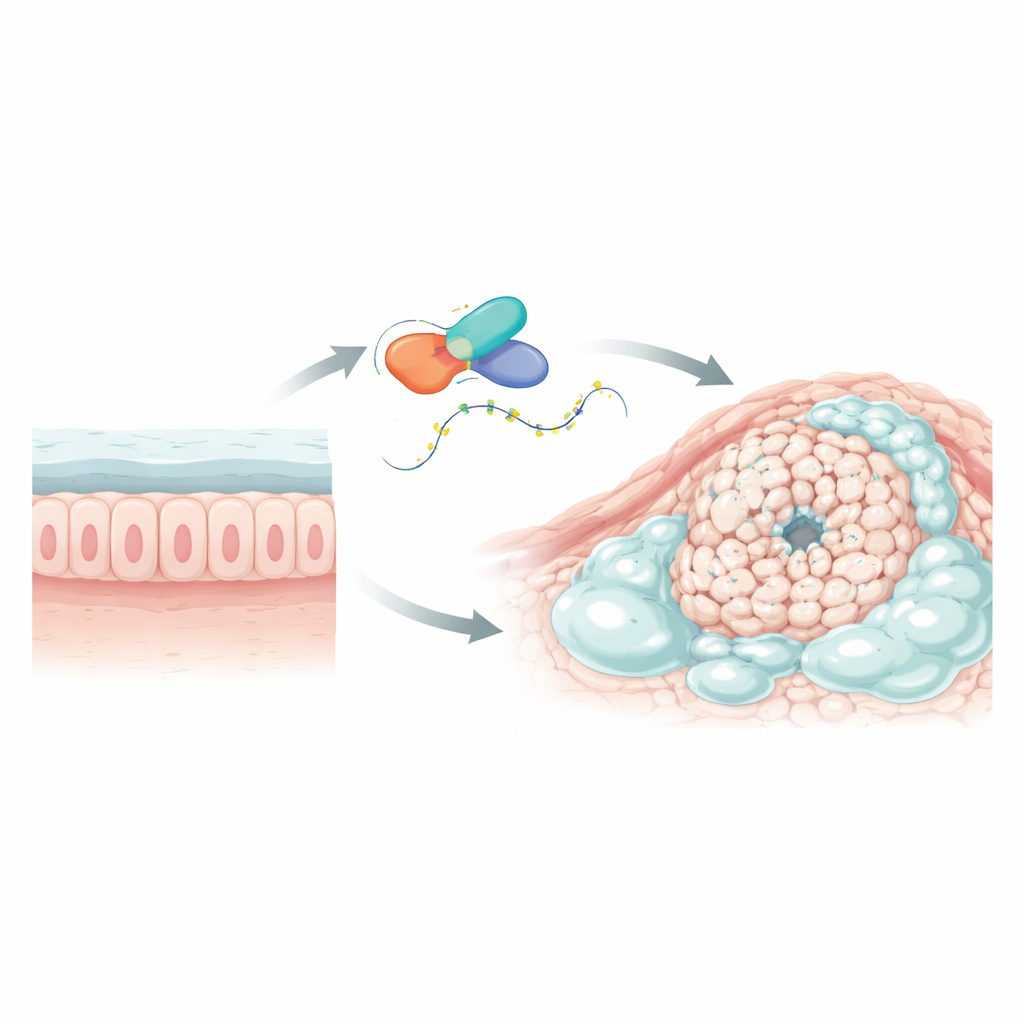
Die Identifizierung eines entscheidenden Störers
Die Forschenden durchsuchten zunächst große Krebsdatenbanken und Einzelzell-Sequenzierungsdaten, um Gene zu finden, die sich in schleimreichen kolorektalen Tumoren anders verhalten als in gewöhnlichen Kolonkarzinomen und im umgebenden gesunden Gewebe. Ein Gen, L1TD1, fiel deutlich auf. Es war in muzinösen Tumoren stark erhöht, nicht jedoch in regulären Tumoren, und in Tumorgewebe höher exprimiert als im angrenzenden normalen Kolon. L1TD1 kodiert ein Protein, das an RNA bindet — die Moleküle, die genetische Anweisungen von der DNA zur Proteinsynthese transportieren. Da RNA-bindende Proteine die Lebensdauer von Nachrichten und deren Auslesung feinregulieren können, war L1TD1 ein plausibler Kandidat für einen zentralen Regulator in diesen schleimdurchsetzten Tumoren.
Wie L1TD1 Tumorwachstum und -ausbreitung vorantreibt
Um die Funktion von L1TD1 zu testen, nutzten die Forschenden Kolonkarzinomzelllinien und Mausmodelle. Eine Erhöhung von L1TD1 in Krebszellen führte zu schnellerer Zellvermehrung, erhöhter Zellbeweglichkeit und stärkerer Invasionsfähigkeit durch gewebsähnliche Barrieren. Eine Reduktion von L1TD1 hatte den gegenteiligen Effekt: verlangsamtes Wachstum und verminderte Invasion. Mäuse, die mit L1TD1-hohen Zellen injiziert wurden, entwickelten größere Tumoren und zeigten häufiger Metastasen in Leber und Bauchraum. In Patienten korrelierten höhere L1TD1-Werte mit größeren, schlechter differenzierten und weiter fortgeschrittenen Tumoren, was das Gen mit aggressiverem klinischem Verhalten verbindet.
Aktivierung von Schleimbildung und Arzneimittelresistenz
Der Schleim selbst erwies sich als zentral für die Wirkung von L1TD1. Zellen mit erhöhtem L1TD1 produzierten größere Mengen wichtiger schleimbildender Proteine, insbesondere MUC2 und MUC5AC, und zeigten Merkmale von Becherzellen, den normalen schleimproduzierenden Zellen des Darms. Dreidimensionale Kulturen und Gewebefärbungen aus Patienten- und Mausproben bestätigten, dass höheres L1TD1 mit dichterem, reichlicherem Schleim einherging. Wichtig ist: Dieser Schleim war kein bloßer Begleiter. Wenn die Forschenden gezielt MUC2 reduzierten, verschwanden der durch L1TD1 verstärkte Zusatzwachstum, die Invasion und die Chemoresistenz größtenteils. L1TD1-reiche Zellen ließen sich schwerer mit dem häufig verwendeten Wirkstoff Oxaliplatin abtöten, und Tumoren mit diesen Zellen schrumpften bei Behandlung in Mäusen weniger — ein Beleg dafür, dass L1TD1 zum Aufbau einer schützenden Schleimbarriere beiträgt.
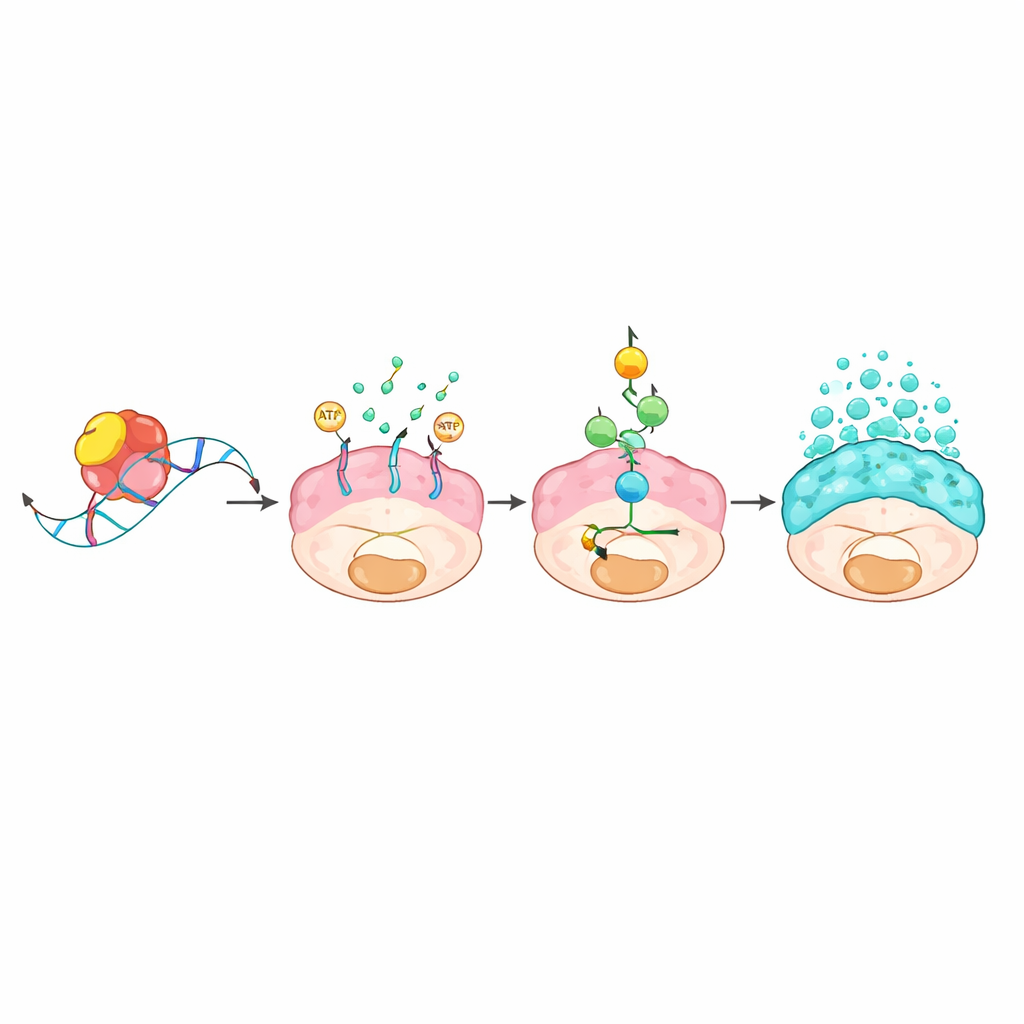
Eine molekulare Kette, die RNA-Kontrolle mit Schleimfluten verbindet
Die Forschenden fragten als Nächstes, wie ein RNA-bindendes Protein so dramatische Veränderungen bewirken kann. Durch das Ausfischen von RNA-Molekülen, die physisch an L1TD1 gebunden sind, und durch den Vergleich der Genaktivität mit und ohne L1TD1 identifizierten sie das Transportergen ABCC3 als Hauptziel. L1TD1 heftete sich an ein kurzes "GUGU"-Motiv im 3'-Abschnitt der ABCC3-mRNA und stabilisierte diese so, dass die Zelle mehr des ABCC3-Proteins (bekannt als MRP3) herstellte. Dieser Transporter sitzt in der Zellmembran und verbraucht Energie, um Substanzen aus der Zelle zu pumpen. Der dadurch entstehende Energieverbrauch aktivierte ein Stoffwechsel-Alarmsystem um den Sensor AMPK, das wiederum einen klassischen Wachstums- und Stressweg, die MAPK-Signalkaskade, einschaltete. Einmal aktiviert, förderte diese Kaskade die Produktion und Freisetzung von Schleimproteinen und verstärkte die Fähigkeit der Tumorzellen zu wachsen, zu migrieren und Arzneimitteln zu widerstehen. Eine genetische Blockade von ABCC3, die Behandlung mit einer experimentellen Verbindung gegen ABCC3 oder die Hemmung des MAPK-Wegs dämpften die Schleimproduktion und schwächten die Tumoren ab.
Was das für Patientinnen und Patienten bedeutet
In der Summe offenbart die Studie ein stufenweises Kontrollsystem für schleimreiche kolorektale Tumoren: L1TD1 stabilisiert die ABCC3-mRNA, ABCC3 entzieht der Zelle Energie, der AMPK–MAPK-Weg wird aktiviert, und der Tumor reagiert mit übermäßiger Schleimproduktion, Aggressivität und Arzneimittelresistenz. Für Patientinnen und Patienten eröffnen sich mehrere vielversprechende Ansatzpunkte. Die Messung von L1TD1- und ABCC3-Spiegeln könnte Tumoren identifizieren, die zu aggressivem Verhalten oder Chemoresistenz neigen. Noch wichtiger: Wirkstoffe, die die L1TD1–ABCC3-Interaktion stören, die Pumpaktivität von MRP3 blockieren oder die nachgeschalteten Signalwege hemmen, könnten die Schleimbarriere abschwächen, das Tumorwachstum verlangsamen und bestehende Behandlungen bei diesem schwierigen Subtyp des kolorektalen Karzinoms wirksamer machen.
Zitation: He, H., Yuan, J., Wang, H. et al. L1TD1 promotes colorectal mucinous adenocarcinoma progression by enhancing ABCC3 mRNA stability. Oncogene 45, 1071–1086 (2026). https://doi.org/10.1038/s41388-026-03716-w
Schlüsselwörter: mukinäres kolorektales Karzinom, L1TD1, ABCC3 MRP3, Schleimproduktion, Chemoresistenz