Clear Sky Science · de
Die multifunktionale RNA-Helikase DDX39A treibt das Fortschreiten von Glioblastomen voran, indem sie das alternatives Spleißen von WISP1 moduliert, das eine immunsuppressive Makrophagenpolarisation induziert
Warum diese Studie zu Hirntumoren wichtig ist
Das Glioblastom gehört zu den tödlichsten Hirntumoren; es zeichnet sich durch häufiges Wiederauftreten nach Behandlung und starke Medikamentenresistenz aus. Diese Studie zeigt, wie ein einzelner molekularer „Schalter“ in Tumorzellen nicht nur das Krebswachstum fördert, sondern auch benachbarte Immunzellen dazu bringt, ihre angreifende Rolle aufzugeben und stattdessen den Tumor zu schützen. Indem die Forschenden diese Ereigniskette zurückverfolgen, identifizieren sie außerdem ein bereits zugelassenes antipsychotisches Medikament, das potenziell umgenutzt werden könnte, um dieses schädliche Netzwerk zu stören.
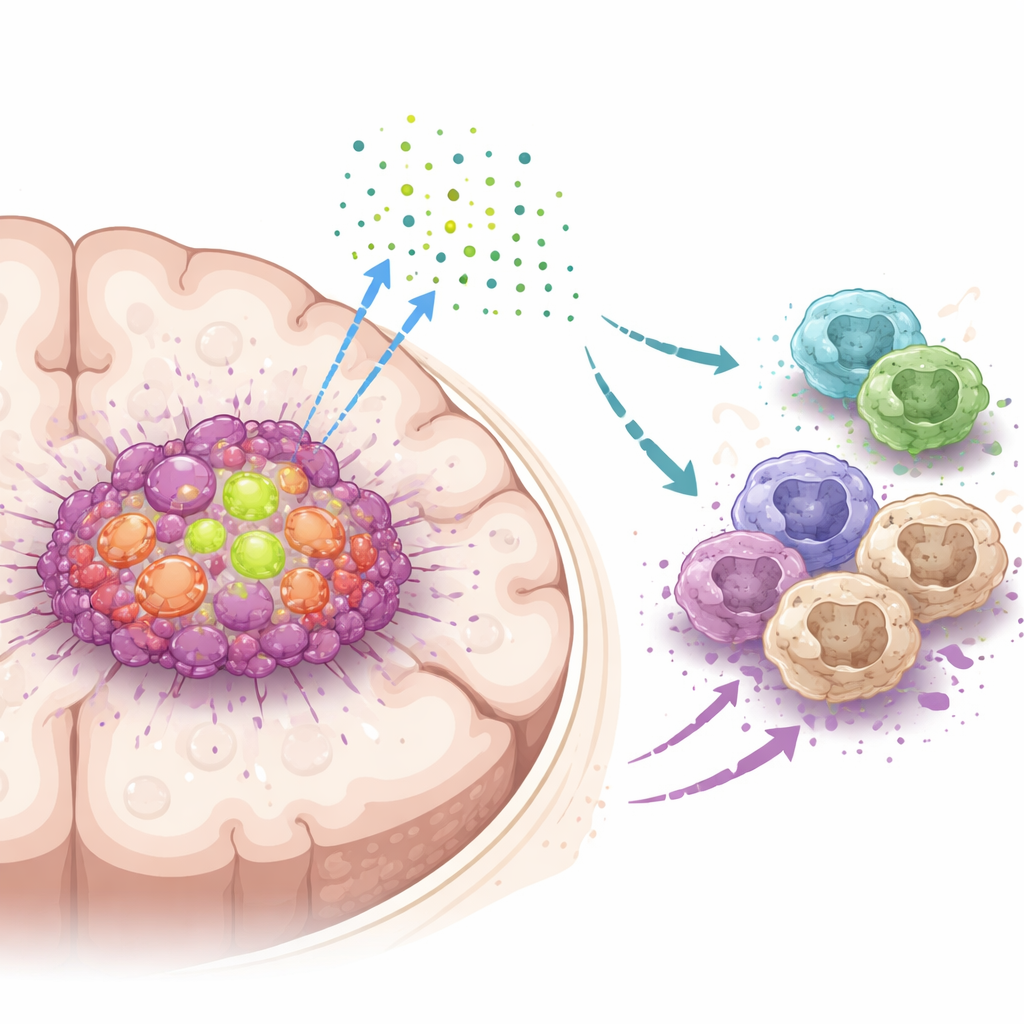
Ein zentraler Helfer in Hirntumorzellen
Das Team konzentrierte sich auf ein Protein namens DDX39A, eine molekulare Maschine, die Zellen beim Verarbeiten von RNA unterstützt, der Arbeitskopie genetischer Information. Anhand großer Patientendatensätze und Tumorproben stellten sie fest, dass DDX39A in Glioblastomen deutlich aktiver ist als im normalen Hirngewebe und mit dem Tumorgrad zunimmt. Einzelzellanalysen zeigten, dass DDX39A besonders reichlich in schnell teilenden Tumorzellen und in bestimmten Immunzellen, den Makrophagen innerhalb der Tumormasse, vorkommt. Patienten, deren Tumoren höhere DDX39A-Werte aufwiesen, hatten tendenziell schlechtere Verläufe, was darauf hindeutet, dass dieses Protein eng mit aggressiver Erkrankung verknüpft ist.
Wie dieser Helfer Wachstum und Ausbreitung antreibt
Um die Funktion von DDX39A zu prüfen, setzten die Forschenden genetische Werkzeuge ein, um das Protein in glioblastom-ähnlichen Stammzellen im Labor und in Mausmodellen von Hirntumoren herunterzufahren. Bei reduzierter DDX39A-Aktivität wuchsen die Tumorzellen langsamer, drangen weniger effektiv in umliegendes Gewebe ein und unterlagen häufiger dem programmierten Zelltod. Die krebsstammzellenähnlichen Zellen verloren zudem weitgehend ihre Fähigkeit, neue Tumorkugeln zu bilden, ein Zeichen für eingeschränkte Selbst-Erneuerung. In Mäusen waren Tumoren mit erniedrigtem DDX39A kleiner und die Tiere lebten länger, was bestätigt, dass dieses Protein aktiv das Tumorwachstum fördert und nicht nur ein passiver Marker ist.
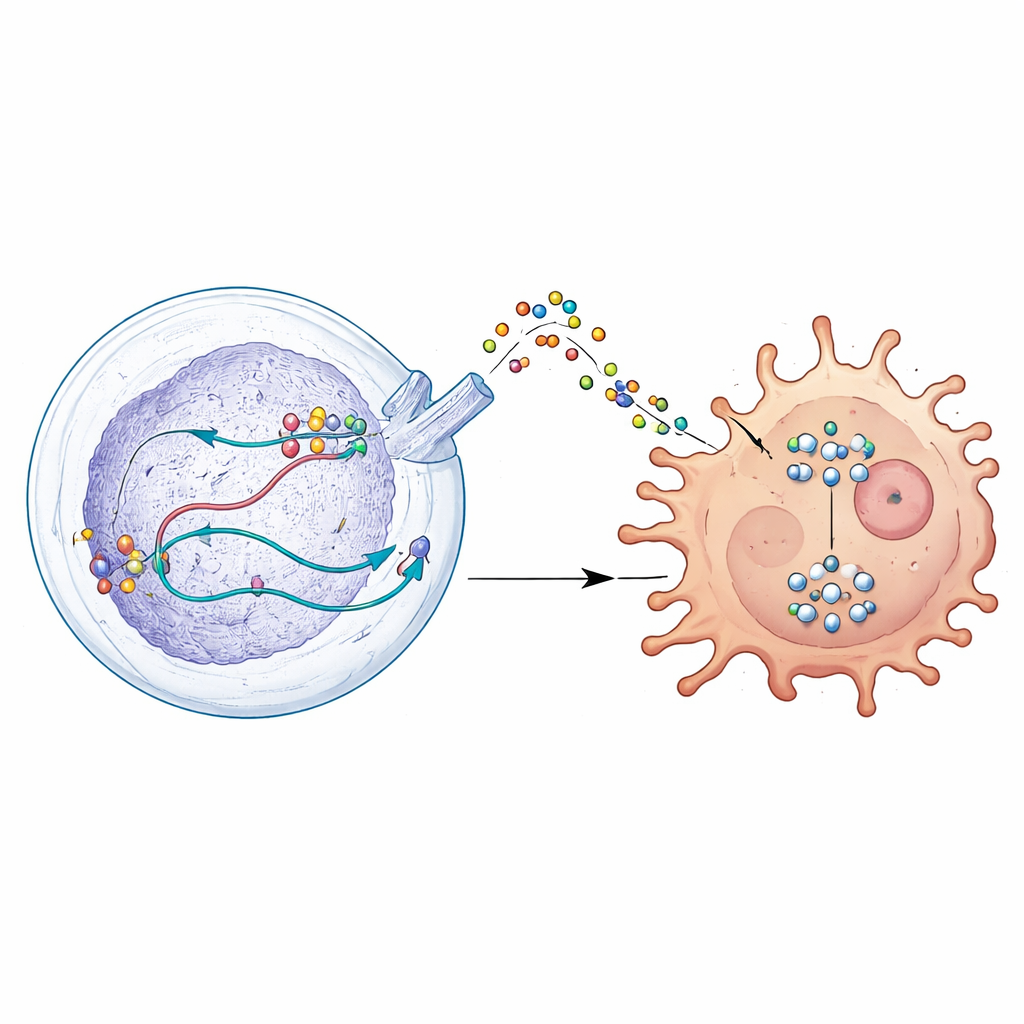
Ein geheimes Signal, das Immunverteidiger entwaffnet
Bei tiefergehenden Untersuchungen entdeckten die Wissenschaftler, dass DDX39A beeinflusst, wie das Gen WISP1 verarbeitet wird. Statt WISP1 einfach ein- oder auszuschalten, formt DDX39A dessen RNA so, dass die Botschaft stabilisiert und die Produktion des WISP1-Proteins gesteigert wird. Tumorzellen setzen WISP1 in ihre Umgebung frei, wo es wie ein trügerisches Signal wirkt. Nahegelegene Makrophagen, die Tumoren entweder angreifen oder unterstützen können, reagieren auf dieses Signal, indem sie in einen immunsuppressiven, tumorfördernden Zustand umschalten. Dieser Wechsel wird durch die Aktivierung eines wachstumssteuernden Signalwegs innerhalb der Zellen, bekannt als AKT, angetrieben. Werden DDX39A oder WISP1 reduziert, beruhigt sich dieser Weg, Tumorzellen werden weniger aggressiv und Makrophagen kehren zu einem eher tumorkämpfenden Profil zurück.
Ein Psychopharmakon als Krebswaffe
Mit dieser Wegkarte suchten die Forschenden in Arzneimitteldatenbanken nach Molekülen, die DDX39A stören könnten. Sie identifizierten Fluphenazin, ein seit Langem verwendetes antipsychotisches Medikament, das ins Gehirn gelangt. Computermodelle und Bindungstests zeigten, dass Fluphenazin direkt an DDX39A andocken kann. In Tumorzellen schwächte das Medikament die Bindung von DDX39A an WISP1-RNA, senkte die WISP1-Spiegel und reduzierte die AKT-Signalgebung. Behandelte Zellen wuchsen weniger, drangen seltener ein, bildeten weniger Tumorkugeln und neigten stärker zum Zelltod. In Mausmodellen verlangsamte Fluphenazin das Wachstum von Hirntumoren, verringerte die Zahl tumorfördernder Makrophagen und verlängerte das Überleben — und das bei Dosen, die denen ähneln, die bereits beim Menschen für andere Indikationen verwendet werden.
Was das für zukünftige Therapien bedeutet
Anschaulich zeigt diese Studie, dass Glioblastomzellen DDX39A nutzen, um eine Botschaft (WISP1) fein abzustimmen, die sowohl ihre eigene Widerstandskraft stärkt als auch benachbarte Immunzellen in Beschützer statt Kämpfer verwandelt. Das Blockieren dieses Helfers, entweder genetisch oder mit einem Medikament wie Fluphenazin, schwächt den Krebs auf zwei Ebenen: die Tumorzellen selbst und den schützenden Schild immunsuppressiver Makrophagen. Obwohl vor einer Anwendung beim Menschen noch umfangreiche Tests nötig sind, eröffnet die Arbeit einen vielversprechenden Weg, ein bekanntes Medikament umzunutzen, um eine neu entdeckte Schwachstelle in einem der hartnäckigsten Hirntumoren zu treffen.
Zitation: Zhang, Y., Xue, Z., Zhang, N. et al. The multifunctional RNA helicase DDX39A drives glioblastoma progression by modulating WISP1 alternative splicing that induces an immunosuppressive macrophage polarization. Oncogene 45, 1026–1041 (2026). https://doi.org/10.1038/s41388-026-03715-x
Schlüsselwörter: Glioblastom, RNA-Spleißen, Tumormikroumgebung, Makrophagenpolarisation, Arzneimittel-Repositionierung