Clear Sky Science · de
ULK1 fördert die metastatische Progression in experimentellen Modellen des epithelialen Ovarialkarzinoms
Warum diese Forschung wichtig ist
Das epitheliale Ovarialkarzinom wird häufig erst entdeckt, nachdem es sich still im Bauchraum ausgebreitet hat, weshalb es zu den tödlichsten Krebserkrankungen bei Frauen zählt. Ein entscheidender Schritt dieser Ausbreitung ist die Bildung winziger Tumorzellcluster, so genannter Sphäroide, die in der Bauchhöhlenflüssigkeit treiben, Chemotherapien überstehen und neue Tumoren begründen. Diese Studie stellt eine präzise Frage mit großen Folgen: Unterstützt ein zellulärer „Überlebensschalter“ namens ULK1 das Durchhaltevermögen und die Ausbreitung dieser Cluster, und könnte das Abschalten dieses Schalters neue Behandlungswege für fortgeschrittenen Eierstockkrebs eröffnen?
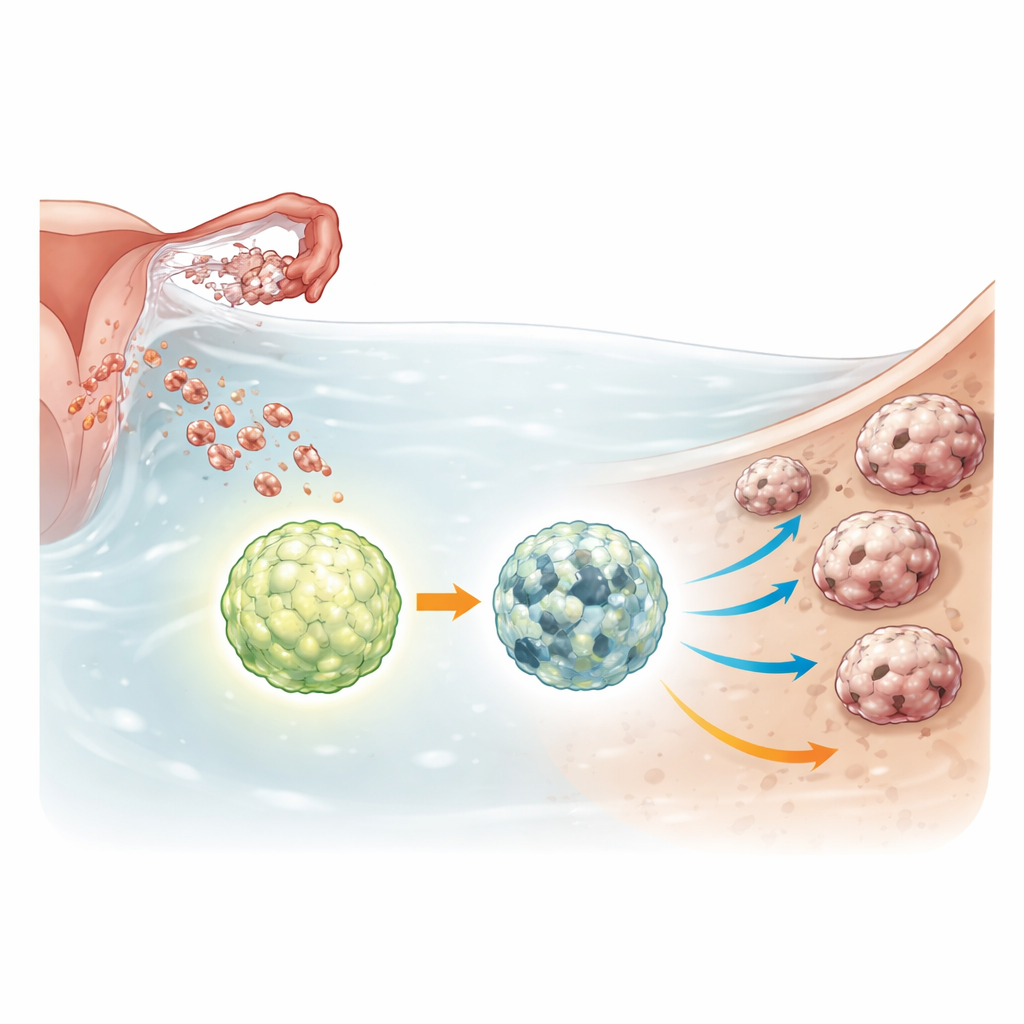
Ein Überlebensschalter in Tumorzellclustern
Ovarialkarzinom-Sphäroide trotzen harten Bedingungen: geringe Nährstoffversorgung, fehlende Verankerung und Chemotherapieeinwirkung. Um damit fertigzuwerden, steigern sie einen Recyclingprozess, die Autophagie, die interne Bestandteile abbaut und wiederverwertet, damit Zellen unter Stress überleben. ULK1 ist der Hauptschalter, der dieses Recycling aktiviert. Die Forschenden nutzten Geneditierung, um ULK1 in mehreren Ovarialkarzinom-Zelllinien sowie in einer nichtkrebsartigen Eileiter-Zelllinie, die frühe, präneoplastische Stadien repräsentiert, vollständig zu entfernen. Anschließend verglichen sie das Verhalten normaler und ULK1-defizienter Zellen, wenn diese als freischwebende Sphäroide oder als dreidimensionale Mini-Tumoren, so genannte Organoide, kultiviert wurden.
Was passiert, wenn der Schalter abgeschaltet wird
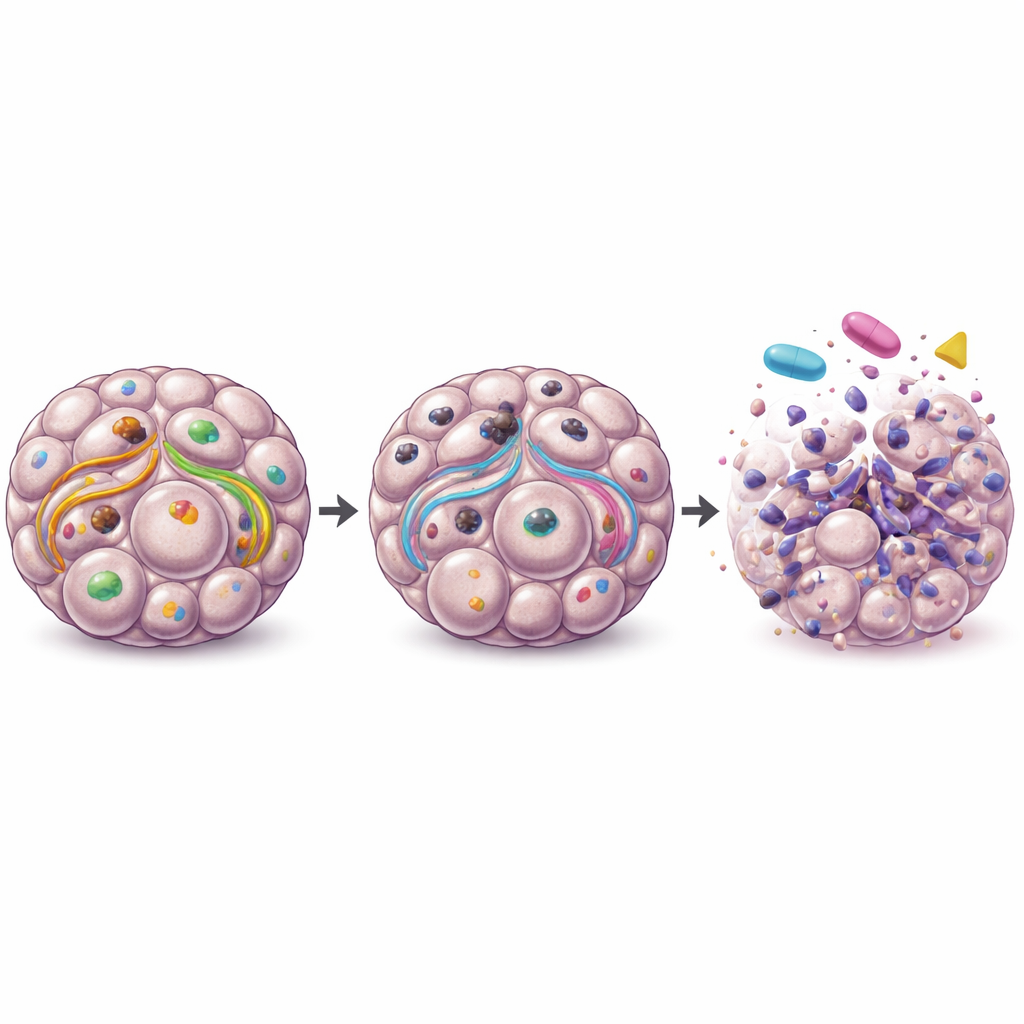
Wurde ULK1 in Ovarialkarzinomzellen entfernt, war ihre Fähigkeit zur Autophagie in Sphäroiden stark beeinträchtigt, was sich in Veränderungen zentraler Recycling-Proteine zeigte. Diese ULK1-losen Sphäroide enthielten weniger lebende Zellen und zeigten vermehrt Anzeichen programmierter Zellsterblichkeit, was darauf hindeutet, dass die Tumorcluster Stressbedingungen nicht mehr so effektiv überstehen konnten. Interessanterweise schaltete die Entfernung von ULK1 in den nichtkrebsartigen Vorläuferzellen deren Recycling-System nicht im gleichen Ausmaß aus, was darauf hindeutet, dass Krebszellen stärker von ULK1 abhängig sind als gesunde Gegenstücke. Diese cancerspezifische Abhängigkeit macht ULK1 zu einem attraktiven therapeutischen Ziel.
Ausbreitung verlangsamen und Tumorvorposten schwächen
Über das Überleben in Suspension hinaus müssen Sphäroide anhaften und in die glatte Auskleidung der Bauchhöhle eindringen, um neue Tumoren zu bilden. In Labor-Modellen, die diesen frühen Schritt der Metastasierung nachbilden, zeigten ULK1-defiziente Sphäroide deutlich geringere Fähigkeit, eine Schicht von Mesothelzellen zur Seite zu schieben und zu durchdringen, die normalerweise Bauchorgane bedeckt. Als Organoide in einer gelartigen Matrix kultiviert, bildeten ULK1-lose Krebszellen außerdem kleinere und weniger robuste Tumorstrukturen. In Mausmodellen, in denen menschliche Ovarialkrebszellen in die Bauchhöhle injiziert wurden, führte der Verlust von ULK1 zu weniger Tumorherden und weniger Flüssigkeitsansammlungen – beides Kennzeichen fortgeschrittener Erkrankung –, obwohl das Gesamtüberleben der Tiere sich nicht verbesserte.
Wichtige Signale schwächen und die Wirkung gezielter Medikamente verstärken
Um zu verstehen, wie ULK1 das Krebswachstum über die Autophagie hinaus unterstützt, kartierten die Forschenden Proteinveränderungen in ULK1-losen Sphäroiden. Sie fanden Störungen in wichtigen Wachstums- und Überlebenswegen innerhalb der Zelle – insbesondere in den MEK–MAPK- und PI3K–AKT–mTOR-Signalwegen. Diese Signalwege helfen Krebszellen normalerweise, dem Zelltod zu entgehen und weiter zu proliferieren. Wenn das Team ULK1-defiziente Sphäroide mit Wirkstoffen behandelte, die MEK oder mTOR blockieren, wurden die Tumorcluster deutlich verwundbarer, mit stark reduzierter Vitalität und geringerer Fähigkeit zur Wiederanhaftung. Im Gegensatz dazu verbesserte das Entfernen von ULK1 nicht die Wirkung gängiger Chemotherapeutika wie Carboplatin, Paclitaxel oder des PARP-Inhibitors Olaparib und schien unter bestimmten Bedingungen deren Nutzen sogar zu verringern.
Hinweise aus Patiententumoren und miniaturisierten Patientenmodellen
Bei der Auswertung großer öffentlicher Datensätze zu Ovarialtumoren stellten die Autorinnen und Autoren fest, dass erhöhte ULK1-Genaktivität mit schlechterer Langzeitüberlebensprognose verbunden war und in metastatischen Proben besonders höher war als in Primärtumoren und normalem Gewebe. Um die Relevanz für die Klinik zu prüfen, testeten sie eine klinische ULK1-blockierende Tablette, DCC-3116, an patienten-abgeleiteten Organoiden aus metastatischen Tumorproben. In einer Teilmenge dieser Patientenmodelle reduzierte die Blockade von ULK1 allein oder die Gabe von MEK- bzw. mTOR-Inhibitoren allein das Überleben der Organoide, obwohl eine Kombination der Wirkstoffe nicht durchgängig zusätzlichen Nutzen brachte. Andere Patientenorganoide waren gegen alle Behandlungen resistent, was die Vielfalt des Ovarialkarzinoms und den Bedarf an Biomarkern unterstreicht, um diejenigen zu identifizieren, die profitieren könnten.
Was das für die zukünftige Versorgung bedeutet
In der Summe zeichnen die Ergebnisse ein Bild von ULK1 als zentralem Unterstützer der Ovarialkrebs‑Ausbreitung: Es treibt das interne Recycling an, das Sphäroid‑Cluster am Leben erhält, fördert ihre Invasionsfähigkeit und trägt zur Aufrechterhaltung starker Wachstumssignale bei. Das Abschalten von ULK1 schwächt diese Prozesse, verkleinert experimentelle Tumoren und macht Tumorcluster empfindlicher gegenüber bestimmten zielgerichteten Wirkstoffen, wenn auch nicht gegenüber Standardchemotherapien. Für Patientinnen deutet diese Arbeit darauf hin, dass ULK1 Teil einer präzisionsmedizinischen Strategie werden könnte – insbesondere bei ULK1-hohem, metastasiertem Krankheitsverlauf – in der ULK1-Inhibitoren mit MEK‑ oder mTOR‑Blockern kombiniert werden, um Tumorwachstum und -ausbreitung zu begrenzen, vorausgesetzt, geeignete Tests können diejenigen Tumoren identifizieren, die am ehesten ansprechen.
Zitation: Webb, J.D., Buensuceso, A., Tomas, E.J. et al. ULK1 promotes metastatic progression in experimental models of epithelial ovarian cancer. Oncogene 45, 1111–1127 (2026). https://doi.org/10.1038/s41388-026-03702-2
Schlüsselwörter: Eierstockkrebs, Metastasen, Autophagie, ULK1, gezielte Therapie