Clear Sky Science · de
Zusammenhang von Retinoiden, Retinoinsäurerezeptoren und Epigenetik beim Brustkrebs
Warum Vitamin A für Brustkrebs wichtig ist
Die meisten Menschen kennen Vitamin A als einen Nährstoff, der für das Sehen wichtig ist, doch seine aktive Form im Körper, die Retinsäure, hilft Zellen auch dabei zu entscheiden, ob sie sich teilen, sich spezialisieren oder bei Schäden selbst zerstören sollen. Dieser Übersichtsartikel untersucht, wie Retinsäure und ihre zellulären „Andockstationen“ beim Brustkrebs verändert sind, warum vielversprechende Laborergebnisse noch nicht in erfolgreiche Medikamente für Patientinnen übersetzt wurden und wie neue Einsichten in die „Software“ der Krebszelle – ihren epigenetischen Code – diese Behandlungsstrategie wiederbeleben könnten.
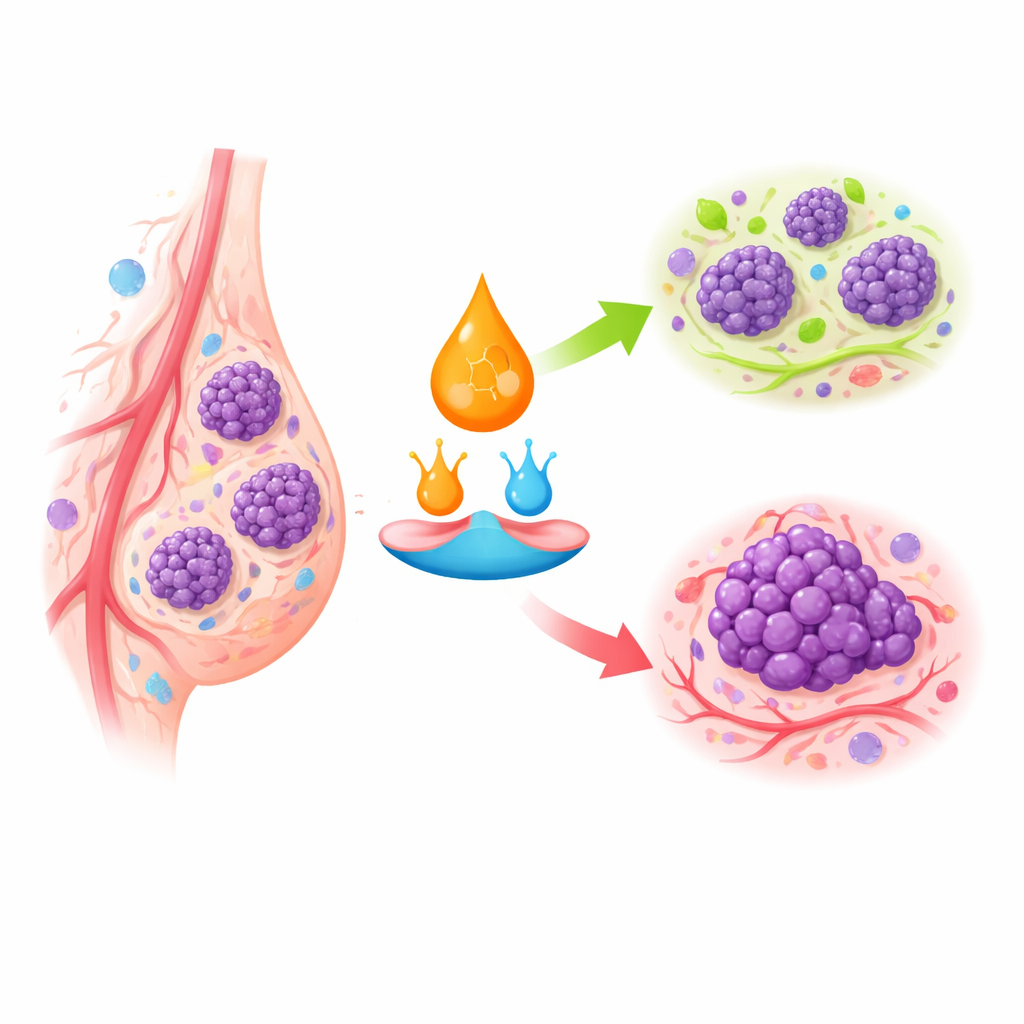
Zellulare Ampeln für Wachstum und Selbstzerstörung
Retinsäure wirkt, indem sie an spezifische Rezeptoren innerhalb der Zelle bindet, die dann ganze Genprogramme an- oder ausschalten. Im gesunden Brustgewebe fördert dieses System, dass Zellen die Teilung einstellen, zu stabilen Zelltypen heranreifen oder absterben, wenn sie auffällig werden. Beim Brustkrebs, besonders bei den aggressiveren Subtypen, fehlen wichtige Rezeptoren oder sind stillgelegt, und der intrazelluläre Transport der Retinsäure wird umgelenkt. Statt zu Rezeptoren zu gelangen, die das Wachstum bremsen, kann sie auf Wege gelenkt werden, die Überleben und Proliferation fördern. Dies erklärt, warum einige Brusttumoren kaum auf Retinoid‑Medikamente ansprechen, obwohl dieselben Wirkstoffe in bestimmten Blutkrebsarten sehr wirksam sind.
Versteckte Schalter in der Software der Krebszelle
Die Autoren konzentrieren sich auf die Epigenetik – chemische Markierungen auf DNA und ihren Verpackungsproteinen, die wie Softwareeinstellungen für das Genom funktionieren. In vielen Brustkrebserkrankungen verriegeln diese Markierungen wichtige Retinsäurerezeptoren, insbesondere einen namens RARβ2, in einer „aus“-Position, ohne die zugrunde liegende DNA‑Sequenz zu verändern. Zusätzliche Methylgruppen auf der DNA und das Verengen der umliegenden Proteinspule schalten diesen Rezeptor ab, während andere Enzyme die Chromatinlandschaft so umgestalten, dass Wachstum und Migration gefördert werden. Nichtkodierende RNAs, die keine Proteine herstellen, aber die Genaktivität beeinflussen, verzerren die Signalgebung zusätzlich weg von Zellsterben und Differenzierung. Zusammengenommen geben diese Veränderungen Krebszellen die Flexibilität, Behandlungen zu widerstehen und sich Stress anzupassen.
Umschaltung der Signalwege
Wichtig ist, dass diese epigenetischen Verriegelungen reversibel sind. In Labormodellen können Medikamente, die DNA‑Methylierung entfernen oder das Chromatin lockern, RARβ2 und andere Komponenten des Retinsäurewegs wiederherstellen. In Kombination mit Retinsäure selbst und konventioneller Chemotherapie verkleinern diese „primenden“ Wirkstoffe Tumoren effektiver und reduzieren den Bestand an stammzellähnlichen Zellen, die als Auslöser für Rückfälle gelten. Auch die Art und Weise, wie Retinsäure innerhalb der Zelle transportiert wird, ist relevant: Ein Trägerprotein dirigiert sie zu wachstumshemmenden Rezeptoren, während ein anderes sie zu pro‑wachstums Wege liefert. Das Gleichgewicht zwischen diesen Transportern zu verändern, kann Retinsäure von einem "Dünger" in eine "Bremse" verwandeln.
Über den Tumor hinaus: Der Nachbarschaftseffekt
Retinsäure wirkt nicht nur auf Krebszellen; sie formt auch die umgebende „Nachbarschaft“ des Tumors aus Blutgefäßen, Immunzellen und Stützgeweben um. In experimentellen Systemen kann sie neues Gefäßwachstum reduzieren, Immunzellen in einen aktiveren, tumorbekämpfenden Zustand bringen und unterdrückende Zellen begrenzen, die normalerweise die Abwehrkräfte des Körpers dämpfen. Die Geschichte ist jedoch nicht ausschließlich positiv: In bestimmten Stromazellen, die den Tumor umgeben, kann die Aktivierung der Retinsäure‑Signalgebung tatsächlich das Krebswachstum fördern, indem sie chemische Kommunikationskanäle stärkt, die maligne Zellen anziehen und unterstützen. Diese gegensätzlichen Effekte bedeuten, dass jede zukünftige Therapie sorgfältig darauf abgestimmt sein muss, die richtigen Zelltypen in der richtigen Weise zu treffen.
Schlaueres Design für zukünftige Studien
Frühe klinische Studien mit Retinoid‑Medikamenten beim Brustkrebs sind weitgehend gescheitert, wurden aber durchgeführt, bevor das heutige Verständnis von Subtypen, Biomarkern und komplexer Pharmakologie vorlag. Die Autoren plädieren dafür, dass neue Studien Patientinnen auswählen sollten, deren Tumoren molekulare Merkmale der Retinoid‑Empfindlichkeit zeigen, etwa erhaltene Rezeptorexpression oder spezifische DNA‑Methylierungsmuster, und Retinoide mit Wirkstoffen kombinieren sollten, die epigenetische Blockaden öffnen, Wachstumswege anvisieren oder die Immunabwehr stärken. Verbesserte Formulierungen, die die Arzneispiegel im Körper stabil halten, zusammen mit engmaschiger Überwachung von Tumor und umliegendem Gewebe, werden entscheidend sein. Wenn diese Hürden überwunden werden können, könnten retinsäurebasierte Behandlungen als präzise Werkzeuge gegen ausgewählte Formen des Brustkrebses noch eine Rolle spielen.
Zitation: Szymański, Ł., Schenk, T., Ławiński, M. et al. Association of retinoids, retinoic acid receptors and epigenetics in breast cancer. Oncogene 45, 961–970 (2026). https://doi.org/10.1038/s41388-026-03699-8
Schlüsselwörter: Retinsäure, Brustkrebs, Epigenetik, Differenzierungstherapie, Tumormikroumgebung