Clear Sky Science · de
Modellierung des Gesprächs zwischen Fettgewebe und Krebs: Eine dreidimensionale Perspektive
Warum Fett und Krebs näher sind, als Sie denken
Die meisten von uns sehen Körperfett als Polster oder Energiespeicher, doch Forschungsarbeiten zeigen inzwischen, dass es ein aktives, kommunizierendes Organ ist, das unsere Gesundheit auf überraschende Weise beeinflussen kann. Dieser Review-Artikel untersucht, wie Fettgewebe und Krebszellen miteinander kommunizieren und wie neue dreidimensionale (3D) Labormodelle Wissenschaftlern helfen, diesen Dialog realistischer als je zuvor nachzubilden. Das Verständnis dieses verborgenen Austauschs könnte Prävention, Medikamententests und Therapien verbessern — besonders in einer zunehmend übergewichtigen Welt. 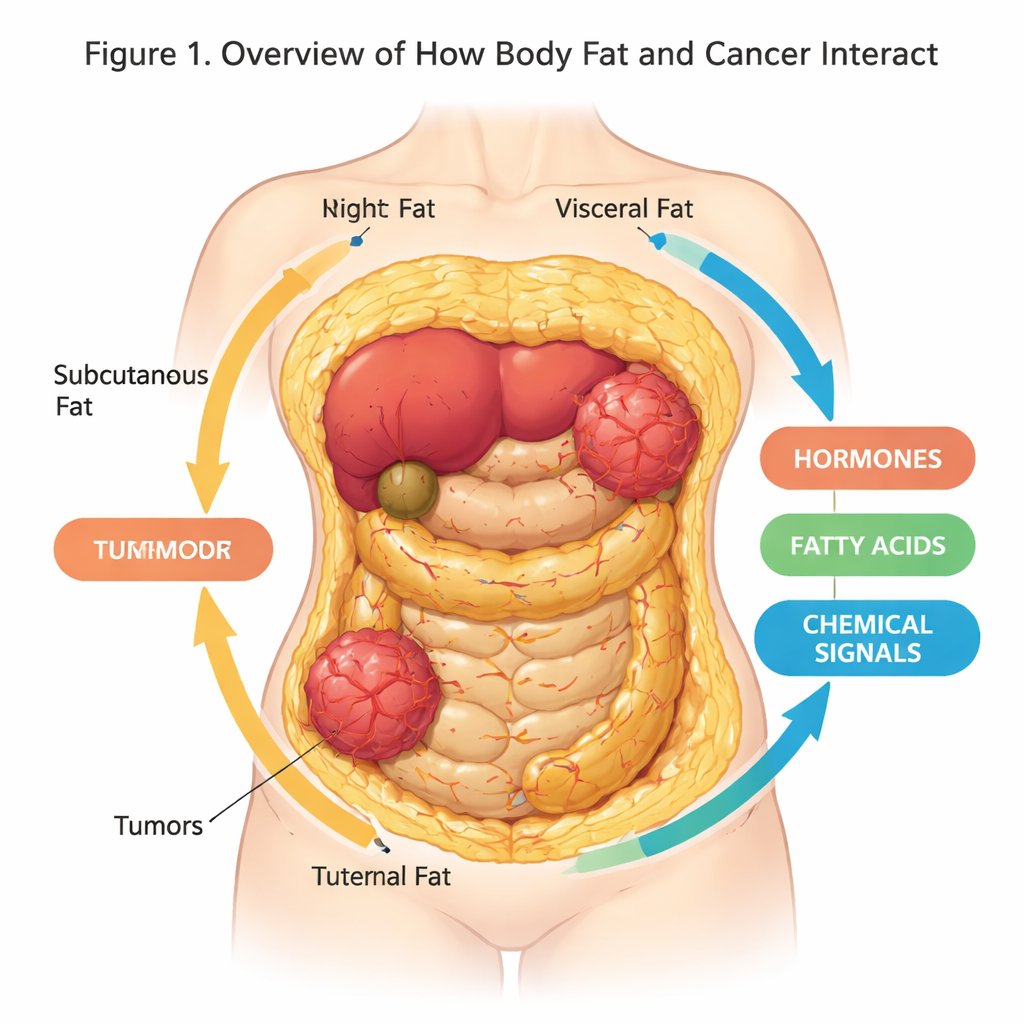
Fett als lebendes, sprechendes Organ
Adipöses Gewebe — unser Körperfett — ist nicht nur ein passiver Speicher. Es ist ein komplexes Organ, das aus Fettzellen, Immunzellen, Blutgefäßen und Stütz-zellen besteht, eingebettet in ein strukturelles Netzwerk, die extrazelluläre Matrix. Verschiedene Fettarten kommen an unterschiedlichen Stellen vor: subkutanes Fett unter der Haut, viszerales Fett um innere Organe sowie weiße, braune und beige Fettzellen, die sich darin unterscheiden, wie sie Energie speichern oder als Wärme verbrennen. Diese Zellen geben ständig ein Gemisch aus Hormonen, Fettsäuren und Signaleiweißen ab, das Stoffwechsel, Entzündungen und — wie wir heute wissen — das Krebsrisiko und -verhalten beeinflusst.
Adipositas, Entzündung und Krebsrisiko
Wenn wir zu viel an Gewicht zulegen, werden weiße Fettzellen größer und zahlreicher, und das Gewebe gerät unter Stress und entzündet sich. Dieses „ungesunde“ Fett setzt mehr entzündungsfördernde Moleküle und Fettsäuren ins Blut frei und verarbeitet Zucker und Lipide weniger effizient. Große epidemiologische Studien haben Adipositas mit einem höheren Risiko und schlechteren Prognosen für viele Krebsarten verbunden, darunter Brust-, Darm-, Bauchspeicheldrüsen- und Gebärmutterkrebs. Der Review erklärt, wie dysfunktionales Fett Tumoren zusätzliche Energie liefern, das umgebende Gewebe versteifen und andere Zelltypen anziehen kann, die gemeinsam ein krebsfreundlicheres Milieu schaffen.
Ein zweiseitiges Gespräch zwischen Fett und Tumoren
Krebs wird zunehmend als Krankheit eines ganzen Ökosystems verstanden, nicht nur als Problem entarteter Zellen. Tumorzellen zapfen benachbartes Fett als Unterstützung an und programmieren Fettzellen, Immunzellen und Fibroblasten um, damit diese Wachstum und Ausbreitung fördern. Im Gegenzug reagieren Fettzellen, indem sie gespeicherte Lipide abbauen und Fettsäuren sowie Hormone freisetzen, die Krebszellen unmittelbar nutzen können. Dieser Austausch kann über zirkulierende Signale aus der Distanz erfolgen oder lokal, dort wo Tumoren direkt neben Fett wachsen, etwa in Brust oder Bauchraum. Tumorzellen können Fettzellen sogar dazu bringen, ihre ursprüngliche Identität zu verlieren und eher narbenbildenden oder immunähnlichen Zellen zu ähneln, die das Gewebe umgestalten und die Invasion fördern. 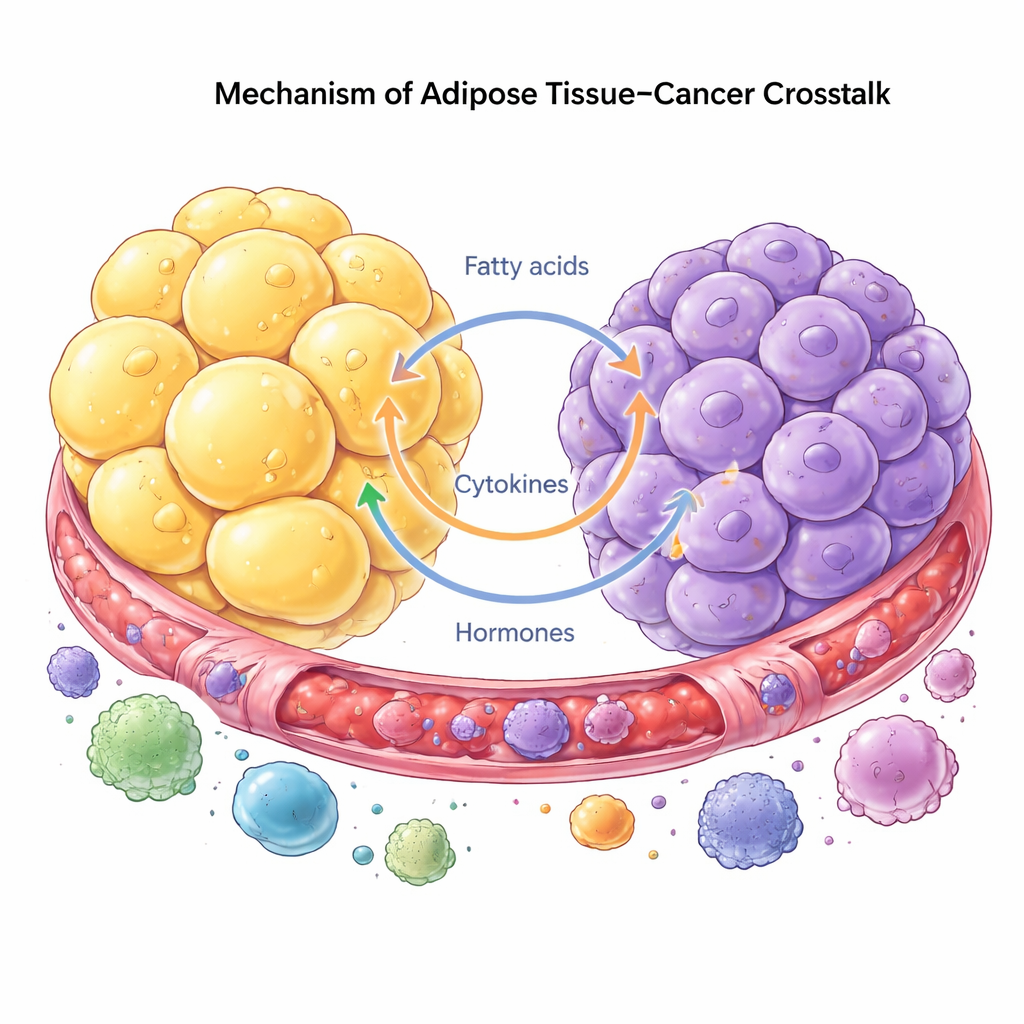
Mini-Gewebe in 3D aufbauen
Traditionelle flache (2D) Zellkulturen und Tiermodelle erfassen diese komplexen Wechselwirkungen oft nicht ausreichend. Die Autoren beschreiben eine neue Generation von 3D-Systemen, die realem Gewebe stärker ähneln. Sphäroide sind einfache Zellansammlungen, die sich zu kleinen Kugeln zusammenlagern; Gerüste sind künstliche Materialien, die eine 3D-Unterlage für das Zellwachstum bieten; Organoide sind miniaturisierte, selbstorganisierende Gewebeversionen; und Assembloide kombinieren mehrere Organoide oder Sphäroide zu zusammengesetzten „Mini-Organen“. Forschende nutzen diese 3D-Ansätze zunehmend, um Fett- und Krebszellen gemeinsam zu kultivieren, zu untersuchen, wie adipositasähnliche Zustände ihr Verhalten verändern, und zu testen, wie Medikamente den schädlichen Dialog zwischen ihnen stören könnten.
Potentiale und derzeitige Lücken
Jedes Modell bringt Kompromisse mit sich. Sphäroide sind günstig und für Hochdurchsatz geeignet, aber relativ einfach. Gerüste erlauben eine präzise Kontrolle physikalischer Eigenschaften wie Steifigkeit, die die Krebsausbreitung beeinflussen kann, sind jedoch technisch anspruchsvoller. Organoide und Assembloide erreichen die höchste Realitätsnähe mit mehreren interagierenden Zelltypen, sind jedoch kostspielig, schwer zu standardisieren und fehlen oft vollständige Gefäßnetze oder Immunkomponenten. Der Review betont, dass heutige Systeme noch nicht ausreichen, um menschliches Fett- und Tumorgewebe perfekt zu reproduzieren, insbesondere bezüglich der vollständigen extrazellulären Matrix, reifer Fettzellen und der Beteiligung von Immunzellen.
Wohin sich diese Forschung entwickelt
Die Autoren schließen, dass die Verbesserung von 3D-Modellen der Fett–Krebs-Interaktionen entscheidend für genauere Medikamententests und das Aufdecken, wie Adipositas Krebs fördert, ist. Wenn diese „Mini-Gewebe“ lebensechter werden — indem realistisches Fett, Tumorzellen, Blutgefäße und Immunzellen kombiniert werden —, könnten sie Forschern helfen, vorherzusagen, welche Behandlungen bei bestimmten Patientinnen und Patienten wirken, bessere Strategien zu entwickeln, um zu verhindern, dass Krebs Körperfett als Treibstoff nutzt, und letztlich Therapien zu lenken, die nicht nur Tumore, sondern auch die ungesunden Umgebungen angreifen, die ihr Wachstum begünstigen.
Zitation: Strusi, G., Suelzu, C.M. & Stebbing, J. Modelling adipose tissue-cancer crosstalk: a three-dimensional perspective. Oncogene 45, 905–913 (2026). https://doi.org/10.1038/s41388-026-03697-w
Schlüsselwörter: Fettgewebe, Adipositas, Tumormikroumgebung, 3D-Zellkultur, Tumorstoffwechsel