Clear Sky Science · de
POM121 O-GlcNAcylierung fördert Knochenmetastasen beim nicht-kleinzelligen Lungenkrebs durch verstärkte c-MYC-Nuklearimport und ECM-Umprogrammierung
Warum diese Forschung wichtig ist
Wenn Lungenkrebs in die Knochen streut, verursacht er starke Schmerzen, Brüche und deutlich verkürzte Überlebenszeiten; dennoch stehen Ärzten nur wenige Mittel zur Verfügung, um diesen tödlichen Schritt aufzuhalten. Diese Studie untersucht die inneren Mechanismen von Lungenkrebszellen, um zu enthüllen, wie einige von ihnen einen speziellen Vorteil erlangen, der ihnen erlaubt, von der Lunge in den Knochen zu wandern und dort zu gedeihen. Indem die Autorinnen und Autoren diesen Prozess bis hin zu winzigen Veränderungen an einem einzelnen, als Torwächter wirkenden Protein am Rand des Zellkerns zurückverfolgen, identifizieren sie eine neue Ereigniskette, die genutzt werden könnte, um Knochenmetastasen bei Patienten mit nicht-kleinzelligem Lungenkrebs besser vorherzusagen, zu verhindern oder zu behandeln.
Ein Zuckeranhang, der das Krebsverhalten verändert
Die Forschenden konzentrierten sich auf posttranslationale Modifikationen, winzige chemische Veränderungen, die Proteine nach ihrer Synthese erwerben. Eine solche Modifikation, die O-GlcNAcylierung, ist die Anfügung eines kleinen Zuckers an bestimmte Stellen von Proteinen. Anhand von Lungenkrebszelllinien und Mausmodellen verglich das Team gewöhnliche Tumorzellen mit Unterpopulationen, die wiederholt anhand ihrer Fähigkeit ausgewählt worden waren, Knochen zu besiedeln. Sie stellten fest, dass diese knochenahnenden Zellen deutlich höhere Gesamtspiegel an O-GlcNAcylierung aufwiesen, getrieben durch eine erhöhte Aktivität des Enzyms OGT, das das Zuckeretikett anbringt. Unter hundertfach modifizierten Proteinen stach eines besonders hervor: POM121, ein Kernelement des Kernporenkomplexes, der den Verkehr in und aus dem Zellkern steuert.
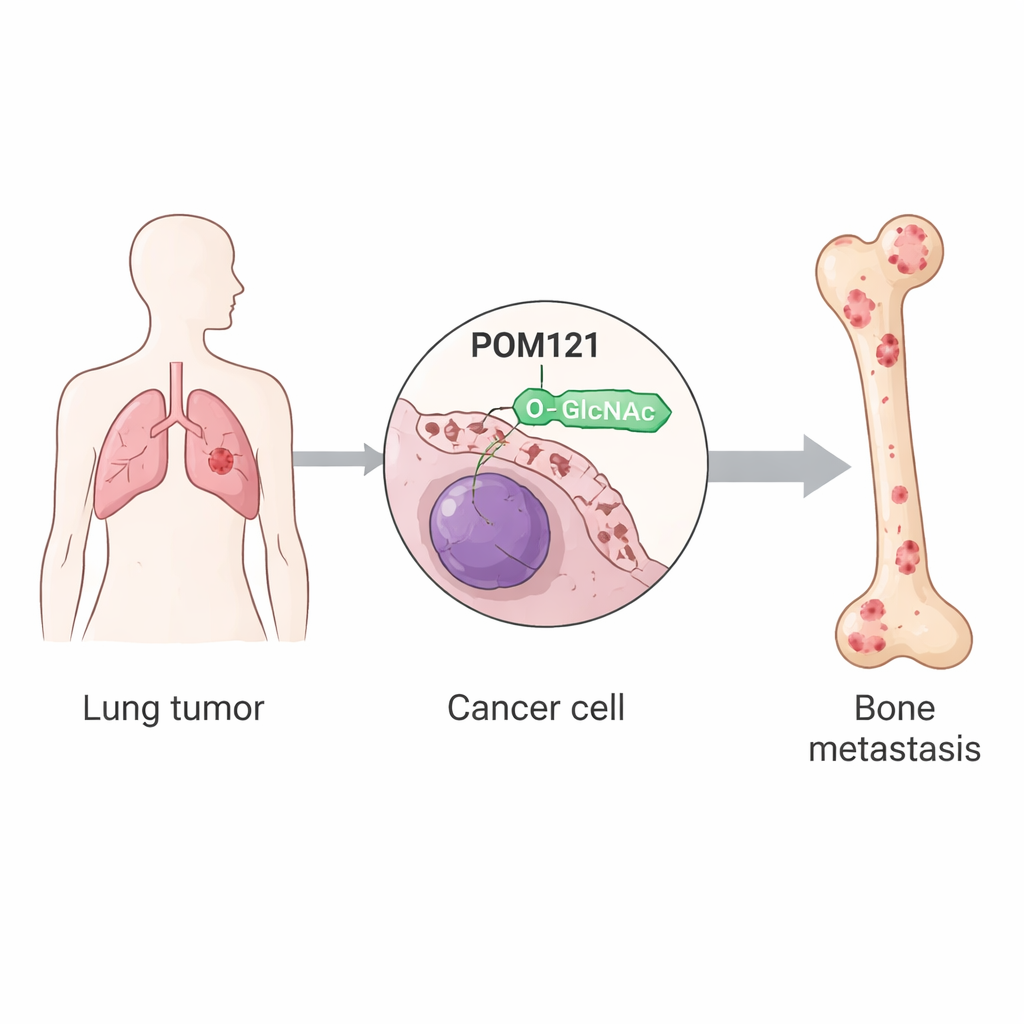
Der nukleare Torwächter POM121 wird stabilisiert
POM121 sitzt in der Membran, die den Zellkern umgibt, und bildet einen Teil des Kanals, durch den viele Signalproteine passieren müssen. In lungentumorbedingten, knochenmetastatischen Zellen trug POM121 eine starke O-GlcNAc-Beladung an einer einzelnen Aminosäureposition, der Serin-199. Wenn diese Stelle so verändert wurde, dass sie nicht mehr modifiziert werden konnte, wurde das Protein instabil und schnell vom zellulären Abbausystem zerlegt. Die Studie zeigt, dass der Zuckeranhang POM121 davor schützt, von einem Enzym namens TRIM21 für den Abbau markiert zu werden, das normalerweise Ubiquitin-“Entsorgungs”-Etiketten anbringt. Mit O-GlcNAc besetzt, kann TRIM21 nur schlecht binden, die Ubiquitinierung sinkt und POM121 reichert sich am Kernporenkomplex an, ohne seinen Ort zu verändern.
Die Tür öffnen für einen starken Krebsantreiber
Welchen Unterschied macht das extra-stabile POM121? Der Schlüssel liegt in einem bekannten krebsfördernden Protein, dem Transkriptionsfaktor c-MYC. c-MYC muss in den Zellkern gelangen, um Gene zu aktivieren, doch sein Durchgang hängt von Kernporenkomponenten wie POM121 ab. Die Autorinnen und Autoren zeigten, dass bei reichlich vorhandenem und O-GlcNAc-modifiziertem POM121 mehr c-MYC im Zellkern nachweisbar war; wurden POM121-Spiegel reduziert oder seine Zucker-Modifikation entfernt, fiel der nukleare Import von c-MYC deutlich ab. In Mäusen bildeten Lungenkrebszellen mit dem nicht-modifizierbaren POM121-Mutanten wesentlich weniger und kleinere Knochenmetastasen, während die Wiederherstellung von c-MYC in POM121-defizienten Zellen einen Großteil ihrer knochenkolonisierenden Fähigkeit zurückbrachte. Damit steht POM121 stromaufwärts von c-MYC in einem kritischen metastatischen Pfad.
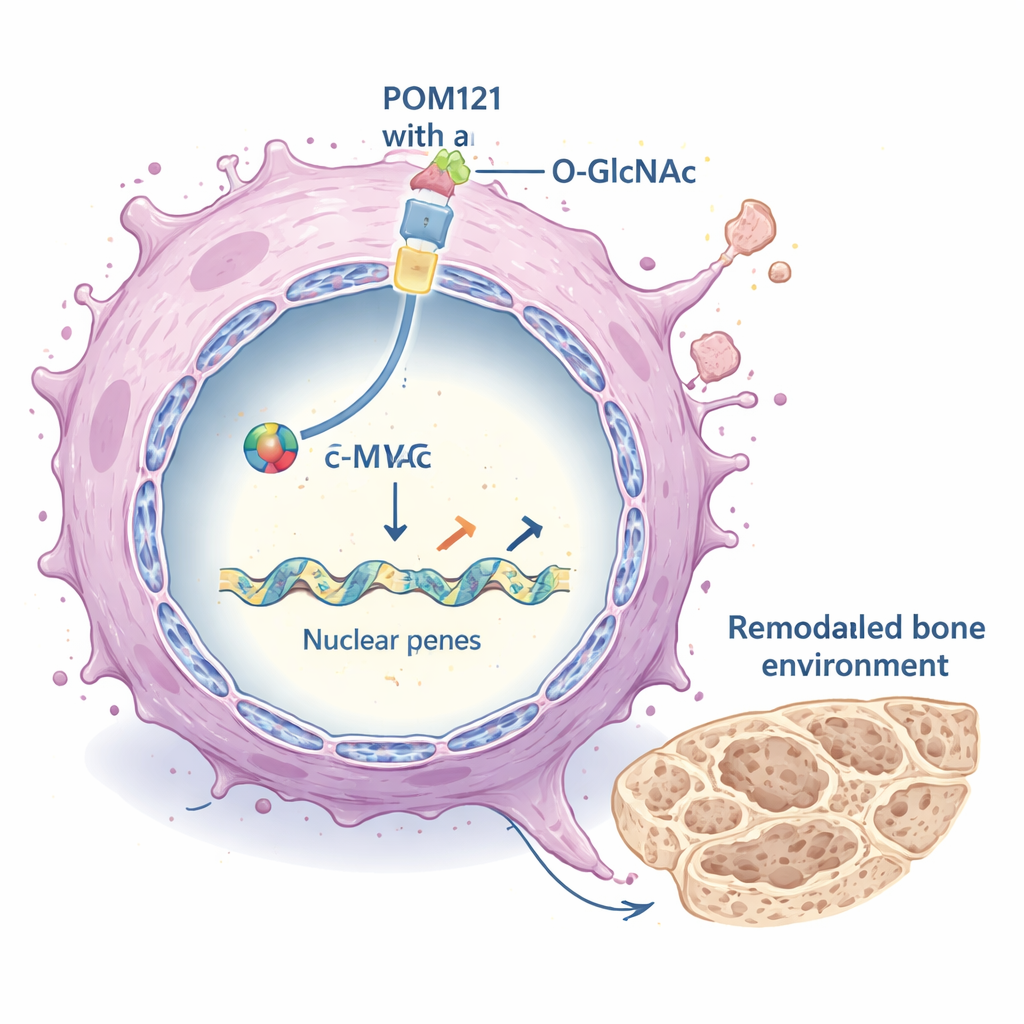
Umpolung der Tumorumgebung
Einmal im Kern agiert c-MYC als Hauptschalter für viele Gene. Hier zeigte sich, dass es eine Gruppe von Genen stark aktiviert, die die extrazelluläre Matrix (ECM) formen – das Gerüst aus Proteinen, das Zellen umgibt. Zu diesen ECM-Genen gehören verschiedene Kollagene und Enzyme, die die Gewebestruktur umgestalten; sie wurden herunterreguliert, wenn POM121 oder c-MYC blockiert wurden, und hochreguliert, wenn O-GlcNAcylierung und POM121 erhöht waren. Die veränderte ECM verstärkte wiederum wichtige Wachstumswege innerhalb der Krebszellen, insbesondere die PI3K–AKT–mTOR-Signalkaskade, die Überleben, Wachstum und Ausbreitung unterstützt. Ähnliche Muster traten in mehreren verschiedenen Lungenkrebsmodellen auf, was darauf hindeutet, dass dieser Mechanismus nicht auf eine einzelne Zelllinie beschränkt ist.
Von der Laborentdeckung zur Auswirkung für Patienten
Beim Blick auf Patientendaten fanden die Forschenden, dass hohe Spiegel von OGT, POM121 und c-MYC sowie der von ihnen regulierten ECM-Gene mit schlechteren Prognosen und mit Lungen tumoren, die bereits in den Knochen gestreut hatten, verbunden waren. Zusammengefasst skizziert die Arbeit eine OGT–POM121–c-MYC–ECM-Achse: vermehrte O-GlcNAcylierung stabilisiert den nuklearen Torwächter POM121, der mehr c-MYC in den Kern bringt, was dann das Gewebegerüst und Wachstumssignale umprogrammiert und so Knochenmetastasen begünstigt. Für Patientinnen und Patienten deutet dies auf neue Biomarker hin, um Risikopersonen für Knochenstreuung zu identifizieren, sowie auf neue therapeutische Ansätze – vom Blockieren von OGT- oder POM121-Funktionen bis hin zur Abschwächung von c-MYC oder ECM-Remodelling – die eines Tages helfen könnten, zu verhindern, dass Lungenkrebs das Skelett erreicht.
Zitation: Ren, YZ., Zhao, MN., Du, FL. et al. POM121 O-GlcNAcylation facilitates bone metastasis in non-small cell lung cancer through enhanced c-MYC nuclear import and ECM reprogramming. Oncogene 45, 728–743 (2026). https://doi.org/10.1038/s41388-026-03687-y
Schlüsselwörter: Lungenkrebs Knochenmetastasen, POM121, O-GlcNAcylierung, c-MYC, extrazelluläre Matrix