Clear Sky Science · de
Störung der Interaktionen zwischen Androgenrezeptor und Cofaktoren durch das RNA‑bindende Protein FUS/TLS verändert die Androgen‑Signalgebung beim Prostatakrebs
Warum diese Forschung für die Männergesundheit wichtig ist
Prostatakrebs ist stark von männlichen Hormonen, den Androgenen, und von einem Protein, das diese wahrnimmt — dem Androgenrezeptor — abhängig. Die meisten modernen Therapien zielen darauf ab, diese Hormone zu entziehen oder den Rezeptor zu blockieren. Dennoch entkommen viele Tumoren schließlich der Kontrolle und kehren in einer schwerer behandelbaren Form zurück. Diese Studie zeigt, wie ein anderes Protein, FUS/TLS, in frühen Stadien des Prostatakrebses als wirkungsvolle Bremse für die Androgen‑Signalgebung fungiert — und wie diese Bremse offenbar versagt, wenn die Krankheit aggressiver wird.
Ein Verkehrslotsen für Hormon‑Signale
Der Androgenrezeptor wirkt wie ein molekularer Schalter. Wenn Androgene an ihn binden, wandert der Rezeptor in den Zellkern, bindet an DNA und schaltet Gene an, die das Wachstum von Prostatazellen fördern. Er arbeitet nicht allein: Helferproteine können seine Aktivität verstärken oder abschwächen. Die Autoren konzentrierten sich auf FUS/TLS (kurz FUS), ein Protein, das für seine Rolle im RNA‑Handling und in der Genregulation bekannt ist und zuvor mit verlangsamtem Tumorwachstum in Verbindung gebracht wurde. An Prostatakrebszellen im Labor zeigten sie, dass viele der von FUS regulierten Gene mit denen des Androgenrezeptors überlappen, was nahelegt, dass FUS direkt beeinflusst, wie Hormon‑Signale in Wachstumsanweisungen übersetzt werden.
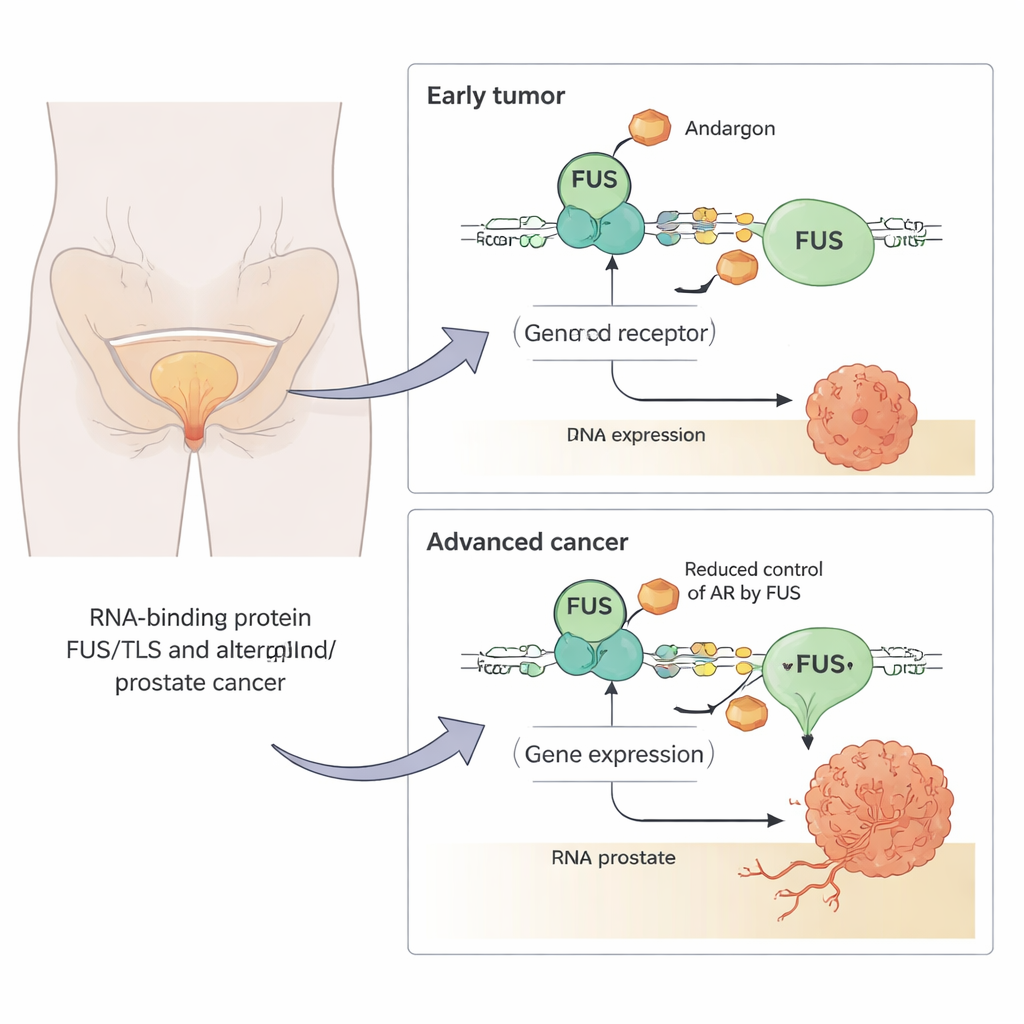
Wie FUS die treibenden Gene des Tumors bremst
Um zu untersuchen, was FUS bewirkt, erhöhten oder verringerten die Forschenden künstlich dessen Gehalt in Prostatakrebszellen und verfolgten, welche Gene auf ein wirksames androgenähnliches Medikament reagierten. Sie fanden heraus, dass FUS androgenabhängige Gene in beide Richtungen beeinflussen kann — mal verstärkend, mal abschwächend. Der vorherrschende Effekt war jedoch Repression: klassische androgen‑aktivierte Gene wie PSA (KLK3) und TMPRSS2 wurden bei hohem FUS‑Spiegel abgesenkt und bei Entfernung von FUS hochreguliert. Reporter‑Assays — einfache Messgrößen für die Aktivität des Androgenrezeptors — bestätigten, dass eine Erhöhung von FUS die Rezeptoraktivität in mehreren Zelltypen auf etwa die Hälfte bis zwei Drittel reduzierte.
Eine physische Blockade der Hormon‑Maschinerie
Die Forschenden fragten dann, wie FUS diese Kontrolle ausübt. Mikroskopie und Interaktionstests zeigten, dass FUS und der Androgenrezeptor im Zellkern aufeinandertreffen und physisch binden. FUS heftet sich über seine RNA‑Erkennungsdomäne an einen spezifischen Bereich des Rezeptors. Es bindet außerdem an mehrere wichtige Cofaktoren, die normalerweise die Rezeptoraktivität steigern würden. Detaillierte Experimente an einem gut untersuchten androgenresponsiven Gen zeigten, dass FUS den Rezeptor nicht daran hindert, DNA zu binden; vielmehr verhindert es, dass das vollständige Helfer‑Ensemble und die grundlegende Transkriptionsmaschinerie dort zusammenkommen. Anders ausgedrückt: FUS lässt den „Schalter“ auf der DNA, entzieht ihm aber die Teile, die nötig wären, um die Genexpression vollständig hochzufahren.
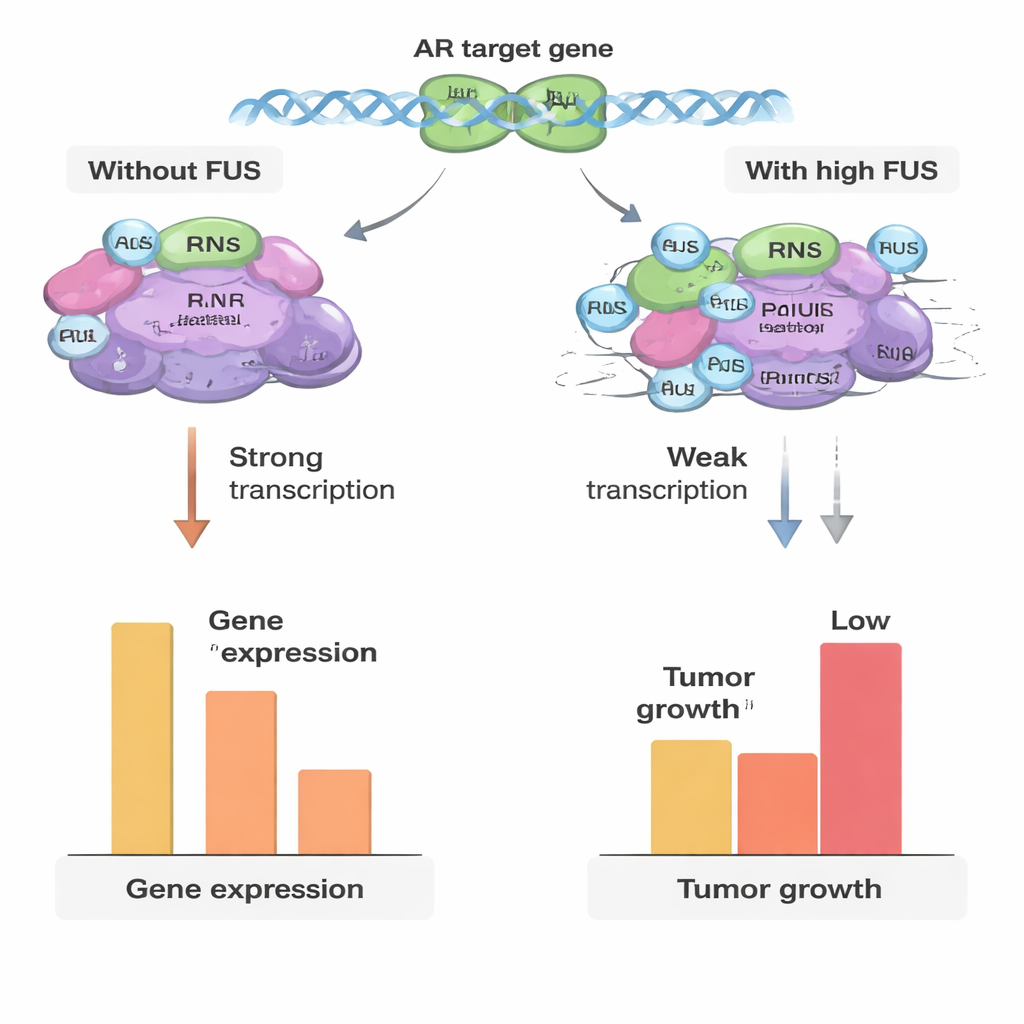
Eine wechselnde Rolle, wenn der Krebs voranschreitet
Da Resistenz gegen Therapien beim Prostatakrebs oft mit Veränderungen dieser Cofaktoren einhergeht, untersuchten die Autoren FUS‑Niveaus in Zelllinien und in Patientenproben aus benignem Gewebe, Primärtumoren und fortgeschrittenem kastrationsresistentem Prostatakrebs (CRPC). In frühen Tumoren waren die FUS‑Proteinwerte im Allgemeinen niedriger als in benignen Proben, was mit der Vorstellung übereinstimmt, dass Tumoren diese natürliche Bremse herunterregeln, um leichter zu wachsen. Überraschenderweise stiegen die FUS‑Werte im fortgeschrittenen CRPC wieder an und lagen höher als in Primärtumoren. In einem CRPC‑ähnlichen Zellmodell veränderte eine Erhöhung von FUS jedoch nicht mehr stark die androgenabhängigen Gene, obwohl das Zellwachstum insgesamt weiterhin gebremst war. Das deutet darauf hin, dass sich das Androgennetzwerk mit der Evolution des Krebses so umgestaltet, dass FUS einen Großteil seines Einflusses auf den Rezeptor verliert und möglicherweise über andere wachstumsbezogene Wege wirkt.
Was das für künftige Behandlungen bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft: FUS verhält sich wie eine eingebaute Sicherheitsvorrichtung, die normalerweise verhindert, dass Androgen‑Signale Prostatazellen übermäßig antreiben. In frühen Stadien fördert ein Absenken von FUS das Tumorwachstum; in fortgeschrittenen Stadien ändert sich das Hormonsystem so grundlegend, dass FUS zwar reichlich vorhanden sein kann, den Androgenrezeptor aber nicht mehr wirksam bremst. Zu verstehen, wie diese Bremse genau funktioniert — und warum sie versagt —, könnte neue Strategien inspirieren, die entweder ihre Kontrolle wiederherstellen oder ihre Fähigkeit nachahmen, die hormongetriebene Wachstumsmaschinerie zu entwaffnen, und so potenziell die Therapien für Männer mit fortgeschrittenem Prostatakrebs verbessern.
Zitation: Brooke, G.N., Leach, D.A., Culley, R.L. et al. Disruption of androgen receptor-cofactor interactions by the RNA-binding protein FUS/TLS alters androgen signalling in prostate cancer. Oncogene 45, 757–773 (2026). https://doi.org/10.1038/s41388-026-03682-3
Schlüsselwörter: Prostatakrebs, Androgenrezeptor, Resistenz gegen Hormontherapie, RNA‑bindende Proteine, FUS TLS