Clear Sky Science · de
Sortilin zeigt tumorhemmende Aktivität, indem es die Signalübertragung von EGFR begrenzt
Warum das für die Krebsbehandlung wichtig ist
Lungenkrebs ist die häufigste krebsbedingte Todesursache weltweit; viele moderne Wirkstoffe zielen auf ein Molekül namens EGFR, das das Tumorwachstum antreibt. Diese Medikamente wirken anfangs oft gut, doch Tumoren entwickeln häufig Resistenzen. Diese Studie deckt eine natürliche „Bremse“ in Lungenkrebszellen auf — eine unerwartete Rolle des Proteins Sortilin — die die krebsfördernden Signale von EGFR abschwächen kann. Das Verständnis dieser Beziehung könnte erklären, warum einige Patientinnen und Patienten besser auf EGFR‑gerichtete Therapien ansprechen, und neue Ansätze nahelegen, um diese Behandlungen länger wirksam zu halten. 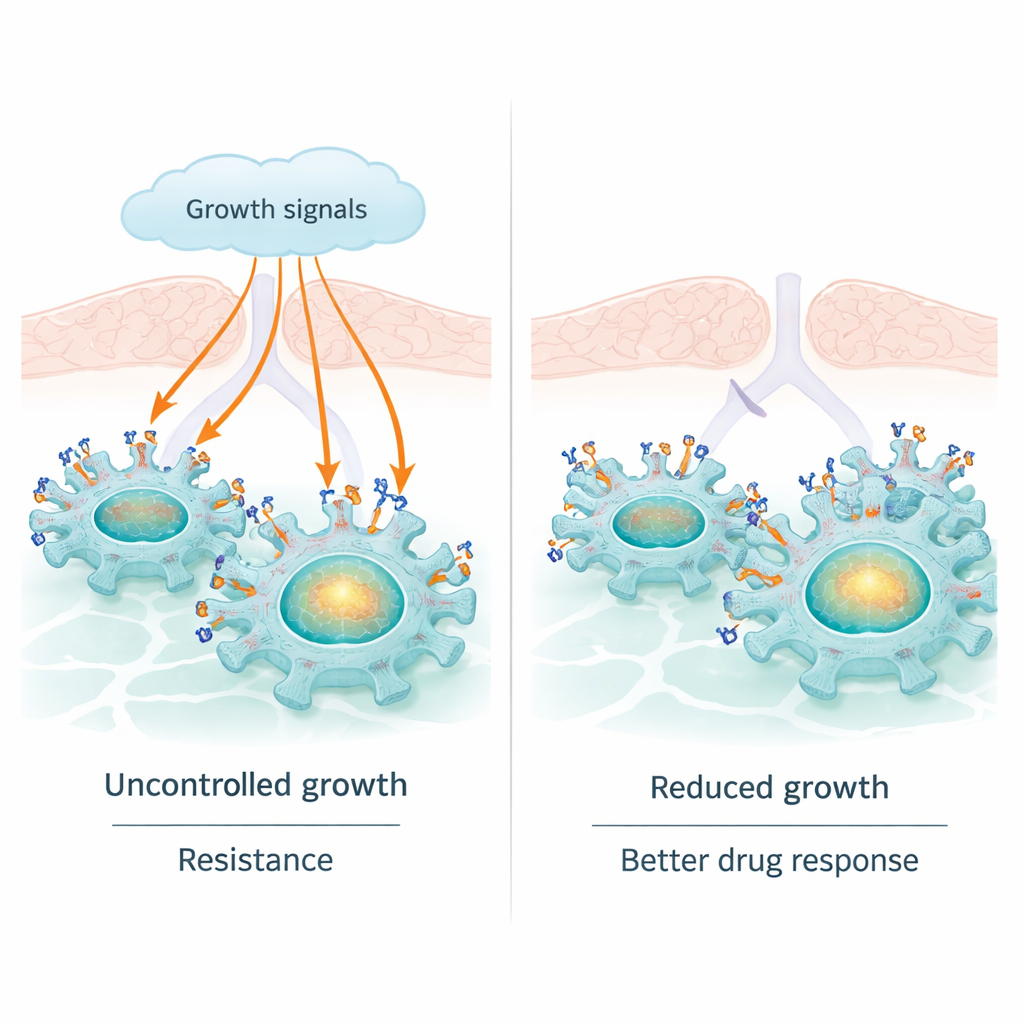
Ein Wachstumsschalter, der außer Kontrolle gerät
EGFR ist ein Rezeptor an der Zelloberfläche, der Wachstums‑Signale aus der Umgebung erkennt. In einem großen Anteil der Lungenadenokarzinome ist EGFR so verändert, dass es dauerhaft eingeschaltet ist. Das fördert ständiges Wachstum und Teilung und erklärt, warum EGFR‑blockierende Tabletten, sogenannte Tyrosinkinaseinhibitoren, Tumoren verkleinern können. EGFR hat jedoch eine weniger beachtete Seite: Es kann in den Zellkern gelangen und dort direkt auf die DNA wirken, Gene wie cMYC und CCND1 aktivieren, die Wachstum, Überleben und Therapie‑Resistenz weiter steigern. Diese nukleäre Rolle von EGFR kann Tumoren helfen zu entkommen, selbst wenn seine Aktivität an der Oberfläche chemisch blockiert ist.
Sortilin zieht in den Zellkern nach
Sortilin war zuvor hauptsächlich als Sortierprotein bekannt, das hilft, EGFR von der Zelloberfläche zu internalisieren und zur Degradation zu führen und so seine Wachstums‑Signale abzuschwächen. In dieser Arbeit zeigen die Autorinnen und Autoren, dass Sortilin EGFR auch in den Zellkern folgt, wenn Lungenkrebszellen stimuliert werden. Mithilfe hochaufgelöster Mikroskopie und biochemischer Fraktionierung beobachteten sie Komplexe aus EGFR und Sortilin, die kurz nach der Aktivierung im Zellkern entstanden. Wichtig ist: Wenn EGFR nicht in den Kern gelangen konnte, blieb auch Sortilin außen, was darauf hinweist, dass EGFR gewissermaßen das „Ticket“ von Sortilin in dieses Kompartiment ist. Dort fanden sich EGFR–Sortilin‑Komplexe gebunden an DNA‑Abschnitte in der Nähe von Startstellen wichtiger wachstumskontrollierender Gene, darunter cMYC und CCND1.
Eine eingebaute Bremse für Krebsgene
Um herauszufinden, was diese Komplexe bewirken, kartierten die Forschenden ihre Bindung im gesamten Genom und maßen Änderungen in der Genaktivität. Sie fanden, dass EGFR allein tendenziell die Aktivierung wachstumsbezogener Gene fördert, während das Vorhandensein von Sortilin an denselben DNA‑Regionen diese Wirkung dämpft. Wenn Sortilin künstlich reduziert wurde, nahm die EGFR‑Bindung an Zielgenen zu und krebsfördernde Gene wie cMYC und CCND1 wurden aktiver. Umgekehrt führte eine Erhöhung der Sortilinmengen dazu, dass sich EGFR weniger fest an die DNA heftete, die Rekrutierung der Transkriptionsmaschinerie abnahm und die Expression dieser onkogenen Gene sank. In Mausmodellen wuchsen Lungentumoren, die so verändert waren, dass sie vermehrt Sortilin produzierten, langsamer und zeigten niedrigere Spiegel von cMYC und CCND1. 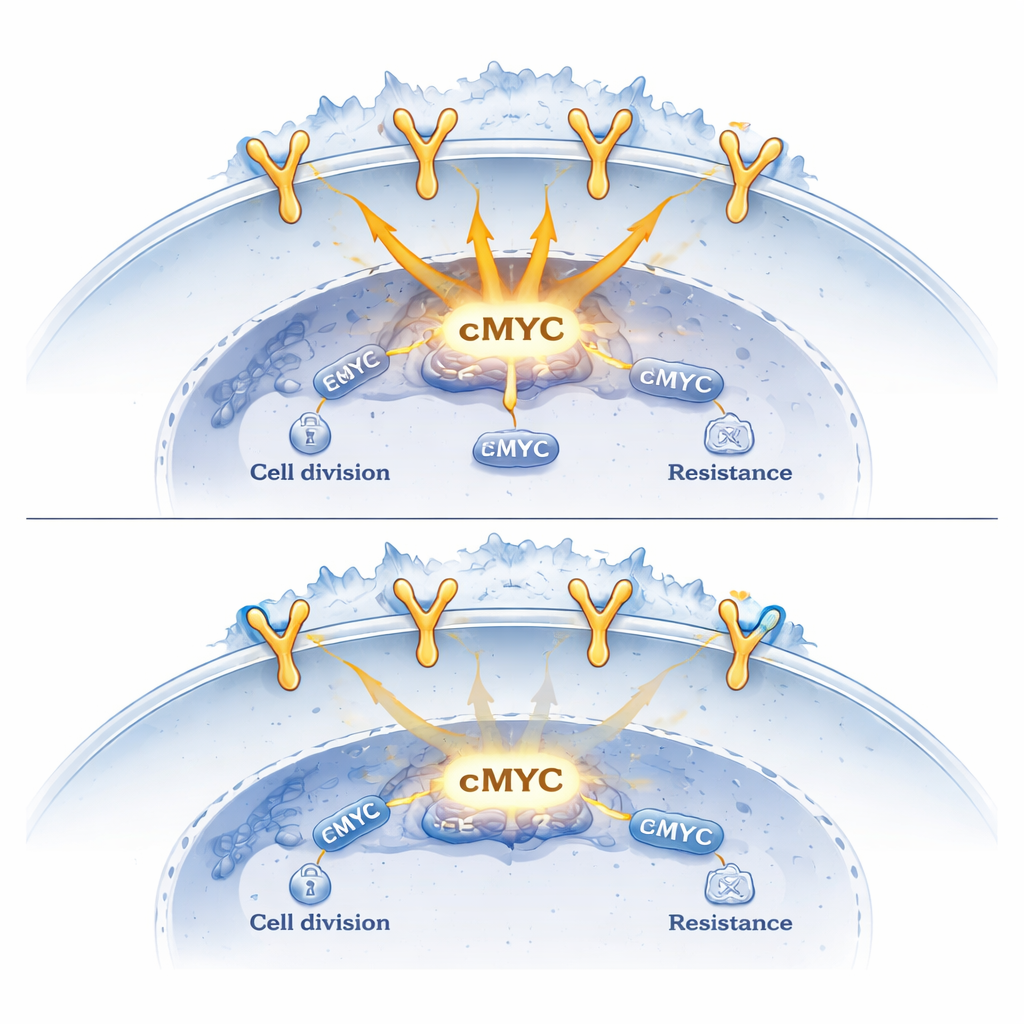
Wechselwirkung mit EGFR‑Medikamenten
Die Studie untersuchte außerdem, wie dieser Mechanismus mit Osimertinib interagiert, einem weit verbreiteten EGFR‑gerichteten Medikament, das darauf ausgelegt ist, problematische EGFR‑Mutationen zu blockieren. Überraschenderweise wanderte der Rezeptor auch dann noch in den Zellkern, wenn Osimertinib die Enzymaktivität von EGFR abschaltete. Dort band er weiterhin an DNA, besonders in der Nähe des cMYC‑Gens. Sortilin sammelte sich unter diesen Bedingungen ebenfalls im Kern an. Wenn Sortilin reichlich vorhanden war, fielen die cMYC‑Werte als Reaktion auf Osimertinib stärker, und Krebszellen waren weniger überlebensfähig. Analysen von Patiententumoren und großen öffentlichen Krebsdatensätzen zeigten, dass Sortilinspiegel in Lungenadenokarzinomen häufig niedriger sind als im normalen Lungengewebe und dass eine höhere Sortilin‑Expression konsistent mit einer geringeren cMYC‑Expression verbunden ist.
Was das für Patientinnen und Patienten bedeutet
In der Zusammenfassung zeichnen die Befunde ein Bild von Sortilin als eine art tumorunterdrückender Partner, der mit EGFR in den Zellkern reist und dieses dort bremst. Indem es EGFRs Fähigkeit einschränkt, mächtige Wachstumsgene wie cMYC zu aktivieren, kann Sortilin das Tumorwachstum verlangsamen und die Wirkung EGFR‑blockierender Medikamente verstärken. Da viele Lungentumoren reduzierte Sortilinwerte haben, fehlt ihnen diese interne Bremse, was erklären könnte, warum einige Krebsarten besonders aggressiv sind oder schnell medikamentenresistent werden. Die Messung von Sortilin in Tumoren könnte helfen, vorherzusagen, wie gut eine Patientin oder ein Patient auf EGFR‑gerichtete Therapien anspricht, und Strategien zur Erhöhung der Sortilinaktivität könnten neue Wege bieten, EGFR‑getriebene Krebserkrankungen langfristig besser zu kontrollieren.
Zitation: Lapeyronnie, E., Granet, C., Tricard, J. et al. Sortilin exhibits tumor suppressor-like activity by limiting EGFR transduction function. Oncogene 45, 875–888 (2026). https://doi.org/10.1038/s41388-026-03680-5
Schlüsselwörter: Lungenkrebs, EGFR, Sortilin, cMYC, Resistenz gegenüber gezielter Therapie