Clear Sky Science · de
Synaptische Effekte von Interleukin‑6 auf menschliche, aus iPS-Zellen abgeleitete dopaminerge Neurone
Warum Entzündungen für die Stimmung wichtig sind
Viele Menschen mit Depression zeigen gleichzeitig Hinweise auf eine niedriggradige Entzündung im Blut, und diese immunologischen Veränderungen stehen in engem Zusammenhang mit Symptomen wie Verlust von Freude, Müdigkeit und verlangsamter Bewegung. Diese Studie stellt eine gezielte Frage: Wie beeinflusst ein zentraler Entzündungsbotenstoff, das Molekül Interleukin‑6, direkt menschliche Gehirnzellen, die Dopamin verwenden — die Chemikalie, die Motivation und Belohnung antreibt? Indem die Forschenden dopaminproduzierende menschliche Neurone aus Stammzellen im Labor züchteten, konnten sie beobachten, wie diese Zellen auf Entzündung reagieren und ob diese Reaktion bei Frauen und Männern verschieden ist.
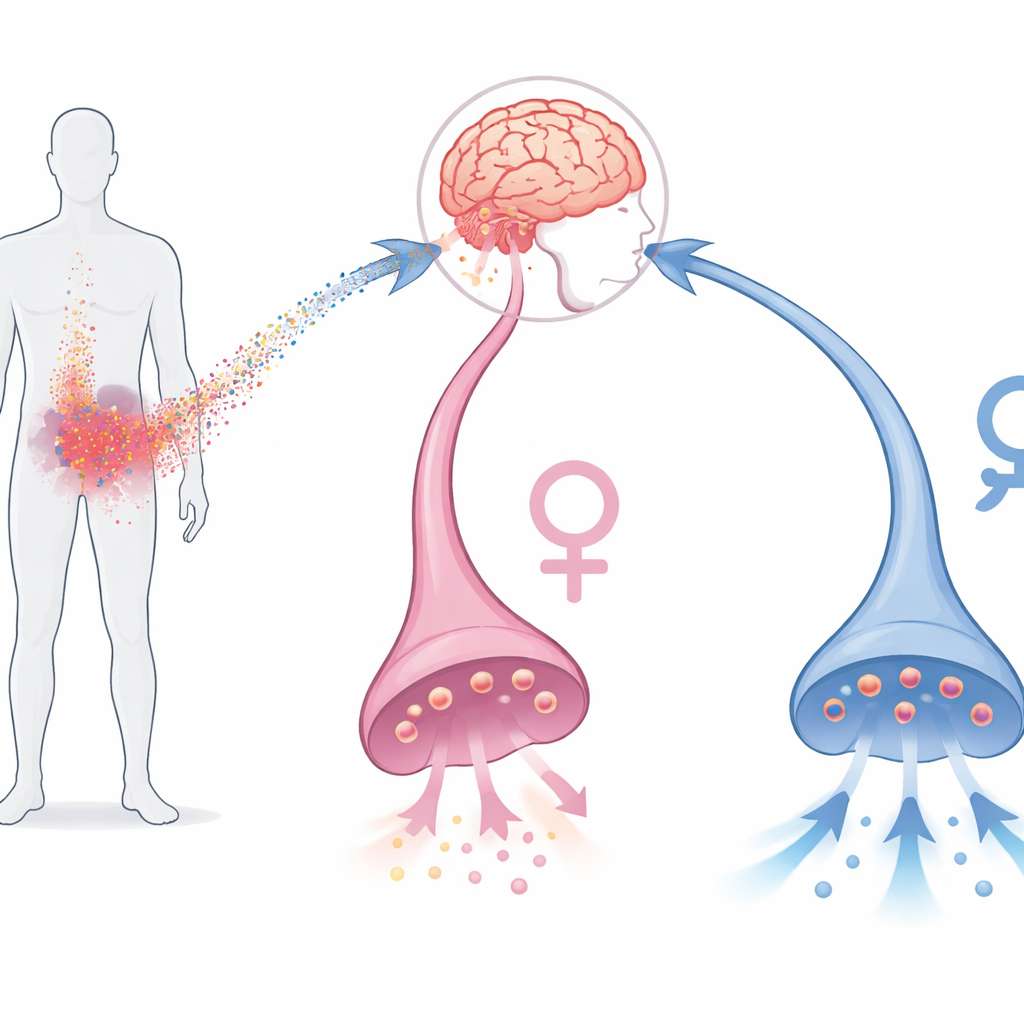
Von Blut‑Signalen zur Motivation im Gehirn
Depression ist verbreitet, einschränkend und häufig resistent gegenüber Standardantidepressiva, insbesondere bei Menschen mit hohen Entzündungswerten im Blut. Frühere Arbeiten an Menschen und Tieren haben gezeigt, dass entzündliche Reize die Aktivität der Belohnungsschaltkreise des Gehirns dämpfen können, insbesondere in einer Region namens ventrales Striatum, die stark auf Dopamin angewiesen ist. Wenn die Konzentration entzündlicher Moleküle experimentell erhöht wird, zeigen Menschen und Tiere typischerweise weniger Antrieb, für Belohnungen zu arbeiten. Interleukin‑6 ist ein solches Molekül und kann unter Stress Dopaminneurone im Gehirn erreichen. Dennoch blieben die genauen Mechanismen, wie es dopaminfreisetzende Zellen verändert, insbesondere in menschlichen Neuronen und im Vergleich der Geschlechter, unklar.
Herstellung menschlicher Dopaminneurone in der Schale
Um diese Mechanismen zu untersuchen, reprogrammierten die Forschenden Haut‑ oder Blutzellen gesunder Männer und Frauen zu induzierten pluripotenten Stammzellen und leiteten diese dann zu midbrain‑Dopaminneuronen, dem für Motivation relevanten Typ, weiter. Nach etwa acht Wochen Reifung zeigten diese Neurone die erwarteten Marker und elektrische Aktivität. Die Wissenschaftler setzten die Zellen anschließend für 24 Stunden Interleukin‑6 aus und maßen drei Schlüsselfunktionen: wie viel Dopamin sie freisetzten, wie häufig sie elektrische Impulse abgaben und wie effizient winzige, mit Dopamin gefüllte Pakete — sogenannte synaptische Vesikel — sich bewegten und am Nervenende andockten, um ihre Ladung freizugeben.
Verschiedene Befunde in Zellen weiblicher und männlicher Herkunft
Die Ergebnisse zeigten eine deutliche Trennung zwischen aus Frauen und aus Männern stammenden Neuronen. In Zellen von Frauen schwächte Interleukin‑6 das Dopaminsystem klar: die Dopaminfreisetzung sank, die elektrische Aktivität verlangsamte sich, und die synaptischen Vesikel bewegten sich träger und waren seltener am Nervenende bereit zur Freisetzung. In Zellen von Männern führten dieselben entzündlichen Signale nur zu geringfügigen Verlangsamungen, lösten jedoch eine offenbar eingebaute Kompensation aus. Vesikel bewegten sich schneller und wurden an den Enden zahlreicher, und die Zahl der präsynaptischen Kontaktpunkte nahm zu — Veränderungen, die helfen könnten, die Dopaminausgabe trotz Entzündung zu erhalten. Genexpressionsanalysen stützten diese funktionellen Unterschiede und zeigten, dass Interleukin‑6 in weiblichen Neuronen stärkere entzündliche Programme aktivierte als in männlichen.
Eine lange nicht‑kodierende RNA als versteckter Schalter
Bei tieferer Analyse konzentrierten sich die Forschenden auf ein regulatorisches Molekül namens MIAT, eine lange nicht‑kodierende RNA, die kein Protein erzeugt, aber die Genaktivität feinjustieren kann. Männliche Dopaminneurone wiesen von vornherein höhere MIAT‑Spiegel auf als weibliche Neurone, und Interleukin‑6 lenkte MIAT in entgegengesetzte Richtungen in den beiden Geschlechtern. Als das Team MIAT in männlichen Neuronen per Geneditierung löschte, gingen die schützenden, kompensatorischen Reaktionen verloren. Nach Interleukin‑6‑Exposition zeigten diese MIAT‑defizienten männlichen Neurone nun reduzierte Dopaminfreisetzung, verlangsamte Aktivität und weniger angedockte Vesikel — sehr ähnlich wie die weiblichen Neurone. MIAT beeinflusste zudem Gene, die die Dopaminwiederverwertung und die Empfindlichkeit gegenüber Interleukin‑6 steuern, was darauf hindeutet, dass sie als molekularer Knotenpunkt wirkt, der bestimmt, wie Dopaminneurone entzündlichem Stress standhalten.
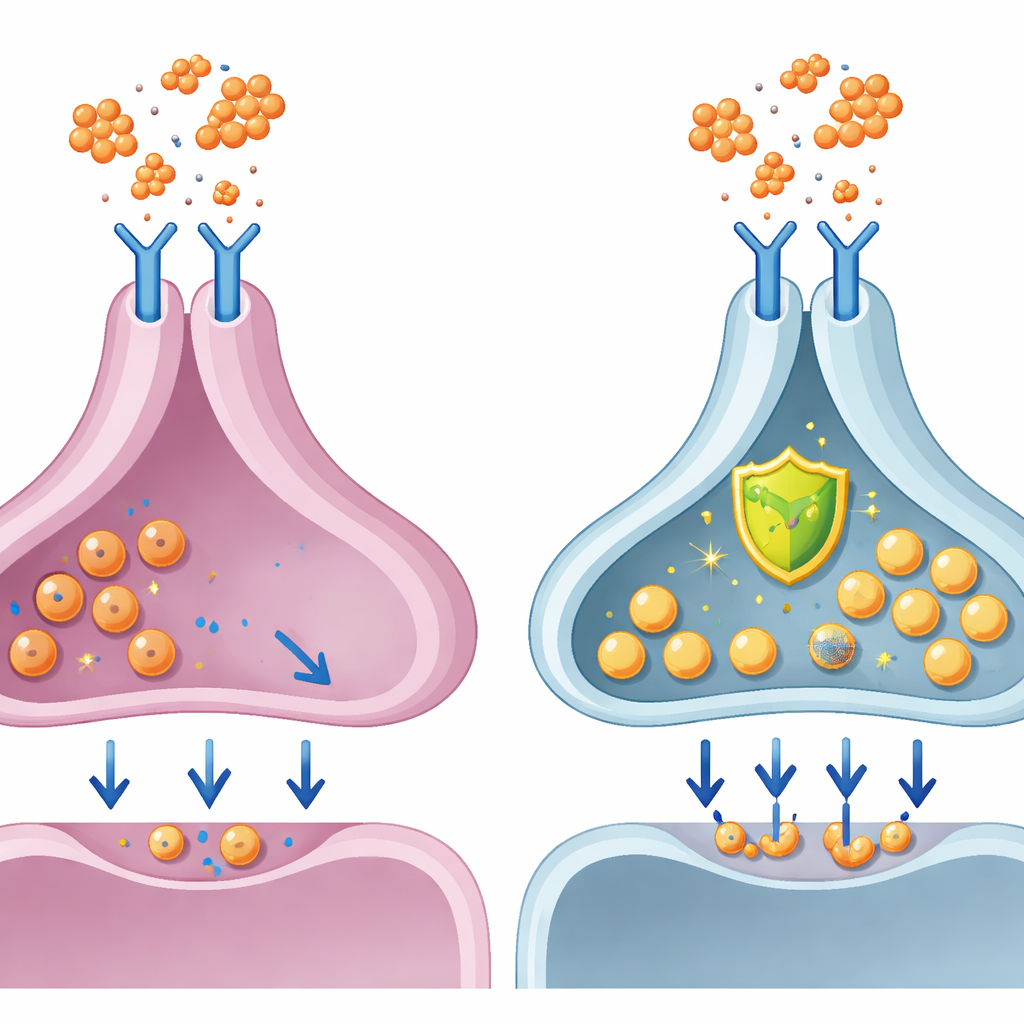
Blockieren des schädlichen Signalwegs
Da Interleukin‑6 über eine bekannte Proteinkette namens JAK‑STAT signalisiert, prüften die Wissenschaftler, ob ein vorhandenes Medikament, das diese Route blockiert, Dopaminneurone schützen kann. Sie gaben Baricitinib, einen bereits für entzündliche Erkrankungen zugelassenen JAK‑Inhibitor, zusammen mit Interleukin‑6 hinzu. In aus Frauen gewonnenen Dopaminneuronen hob Baricitinib weitgehend den Rückgang der Dopaminfreisetzung, die Verlangsamung der elektrischen Aktivität und die Probleme mit synaptischen Vesikeln auf. Dies legt nahe, dass die Zielrichtung dieses Signalwegs menschliche Dopaminzellen direkt vor entzündungsbedingter Dysfunktion schützen kann — zumindest in der Zellkultur — und erklärt möglicherweise, warum solche Medikamente bei einigen Patienten mit Verbesserungen von Stimmung und Motivation in Verbindung gebracht wurden.
Was das für Menschen mit Depression bedeutet
Zusammengefasst zeigt diese Arbeit, dass entzündliche Signale menschliche Dopaminneurone geschlechtsspezifisch schwächen können: Weibliche Neurone neigen zu deutlichen Schäden an der Dopaminfreisetzungs‑Maschinerie, während männliche Neurone zu adaptiven Veränderungen tendieren, die die Funktion erhalten. Eine nicht‑kodierende RNA, MIAT, scheint ein wichtiger Bestandteil dieses Unterschieds zu sein, und das Blockieren der nachgeschalteten Signalübertragung mit Baricitinib kann empfindliche Zellen retten. Für betroffene Menschen stützen diese Befunde die Idee, dass entzündungszielgerichtete Behandlungen besonders hilfreich für depressive Patienten mit hohen Entzündungsmarkern sein könnten und dass Geschlecht sowie individuelle molekulare Profile bei der Auswahl solcher Therapien eine Rolle spielen sollten.
Zitation: Huang, Y., Michalski, C., Zhou, Y. et al. Synaptic effects of interleukin-6 on human iPSC-derived dopaminergic neurons. Neuropsychopharmacol. 51, 934–945 (2026). https://doi.org/10.1038/s41386-025-02320-y
Schlüsselwörter: Entzündung und Depression, Dopaminerge Neurone, Geschlechtsunterschiede, Interleukin‑6, antientzündliche Behandlungen