Clear Sky Science · de
RO4938581, ein negativer allosterischer Modulator von GABAA-α5, rettete Verhaltens- und EEG-Phänotypen in einem Mausmodell des Dup15q-Syndroms
Warum diese Gehirnforschung wichtig ist
Das Dup15q-Syndrom ist eine seltene genetische Erkrankung, die häufig Autismus, Anfälle und erhebliche Lernschwierigkeiten verursacht. Familien haben wenig mehr als unterstützende Pflege zur Verfügung, und es gibt keine Behandlung, die die zugrundeliegende Biologie direkt adressiert. Diese Studie nutzte Mäuse mit demselben zusätzlichen DNA-Abschnitt wie Menschen mit Dup15q, um zu untersuchen, was im Gehirn schiefgeht — und um zu testen, ob ein hochspezifisches experimentelles Medikament dieses Problem abschwächen kann. Die Arbeit macht eine bestimmte Art von Gehirnrezeptor als vielversprechendes, testbares Ziel für künftige Präzisionsmedikamente aus.
Zu viel Bremsen im Gehirn
Unsere Gehirne beruhen auf einem empfindlichen Gleichgewicht zwischen "Go"-Signalen, die Neurone erregen, und "Stopp"-Signalen, die sie beruhigen. Beim Dup15q-Syndrom ist ein Abschnitt auf Chromosom 15 dupliziert. Diese Region enthält drei Gene, die Teile eines wichtigen "Stopp"-Rezeptors im Gehirn bauen, genannt GABAA-Rezeptor, insbesondere eine Variante mit einer Komponente namens alpha‑5. Die Forschenden erzeugten Mäuse mit derselben Art von Duplikation und stellten fest, dass diese Tiere in für Gedächtnis, Emotion und Bewegung wichtigen Hirnregionen — einschließlich Hippocampus und Kortex — etwa 50 % mehr alpha‑5‑haltige Rezeptoren produzierten. Mehrere Methoden — von Genexpressionsmessungen bis zur Rezeptorbildgebung — kamen zu demselben Schluss: Dieses spezielle Bremssystem ist im Dup15q-Modell übermäßig ausgeprägt.
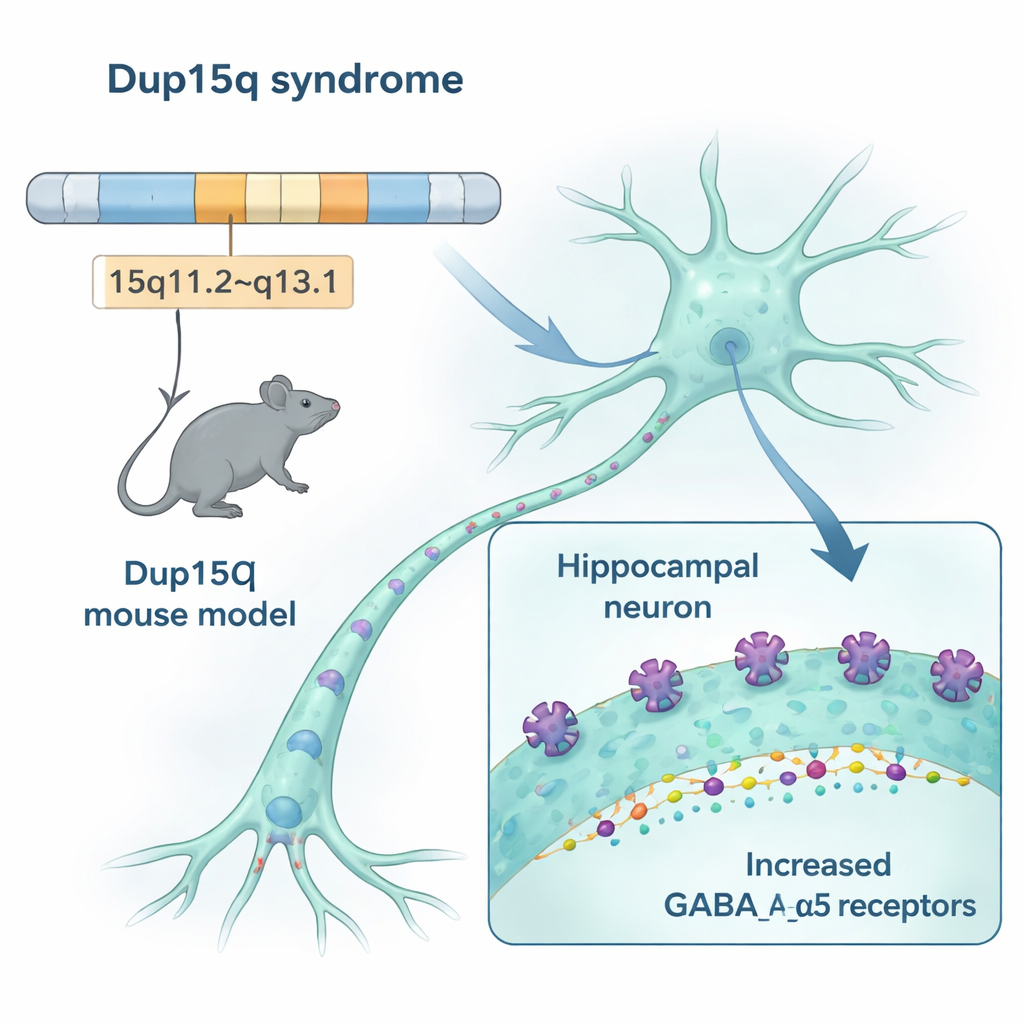
Wie zusätzliche Rezeptoren Gehirnsignale verändern
Mehr Bremsrezeptoren sind nur relevant, wenn sie tatsächlich beeinflussen, wie Schaltkreise feuern. In dünnen Hirnschnitten aus dem Hippocampus maßen die Forschenden die winzigen elektrischen Ströme, die inhibitorische Neurone an andere Zellen senden. Bei den Dup15q-Mäusen traten diese inhibitorischen Ströme häufiger auf, was darauf hindeutet, dass die Neurone einem stärkeren andauernden Bremsen ausgesetzt waren, obwohl die Größe jedes einzelnen Signals unverändert blieb. Ein separater Test der Netzwerkfunktion, genannt gepaarte Pulshemmung (paired-pulse inhibition), zeigte ebenfalls, dass Netzwerke in diesen Mäusen stärker gedämpft waren als die ihrer gesunden Wurfgeschwister. Zusammengenommen deuten die Daten darauf hin, dass die zusätzlichen Rezeptoren inhibitorische Schaltkreise dominanter machen und das Gleichgewicht weg von flexibler Informationsverarbeitung verschieben.
Verhalten und Hirnwellen bei betroffenen Mäusen
Die Forschenden fragten als Nächstes, ob diese veränderte Verschaltung sich in Verhaltensweisen niederschlägt, die menschlichen Symptomen ähneln. In einer Reihe von Tests zeigten die Dup15q-Mäuse Hinweise auf soziale und Kommunikationsunterschiede und vor allem Probleme mit kognitiver Flexibilität. In einer Wasserlabyrinth-Aufgabe lernten sowohl normale als auch Dup15q-Mäuse, wo eine versteckte Plattform lag. Als die Plattform jedoch verschoben wurde, zögerten die Dup15q-Tiere, den alten Ort aufzugeben und sich an die neue Position anzupassen — ein Laborparallele zu den starren Routinen, die häufig bei Autismus beobachtet werden. Das Team zeichnete außerdem Elektroenzephalographie(EEG)-Signale auf, die summierten Rhythmen vieler Neurone. Wie bei Menschen mit Dup15q zeigten die Mäuse ungewöhnlich starke Beta‑Band-Aktivität, einen schnellen Rhythmus, der oft durch Substanzen verstärkt wird, die GABAA-Rezeptoren aktivieren, was die Vorstellung stützt, dass ihr inhibitorisches System überaktiv ist.
Ein zielgerichtetes Medikament, das die Bremse lockert
Um zu prüfen, ob sie dieses Überbremsen normalisieren können, verwendeten die Forschenden RO4938581, eine experimentelle Verbindung, die alpha‑5‑Typ GABAA-Rezeptoren selektiv schwächt, ohne andere Formen zu beeinflussen. In Hippocampus-Schnitten reduzierte das Medikament die Menge des inhibitorischen Ladungstransfers in Dup15q-Neuronen und wirkte so dem Überbremsen entgegen. Bei täglicher oraler Gabe über mehrere Wochen verbesserte dieselbe Verbindung die Leistung der Tiere in der Reversal‑Phase des Wasserlabyrinths, sodass sie sich an die verschobene Plattform ähnlich wie gesunde Mäuse anpassen konnten. Sie normalisierte auch weitgehend ihre sozialen Interaktionen. In EEG-Aufzeichnungen verringerte eine akute Dosis teilweise die überhöhte Beta‑Leistung bei Dup15q-Mäusen und lenkte ihre Hirnrhythmen in Richtung des typischen Musters.
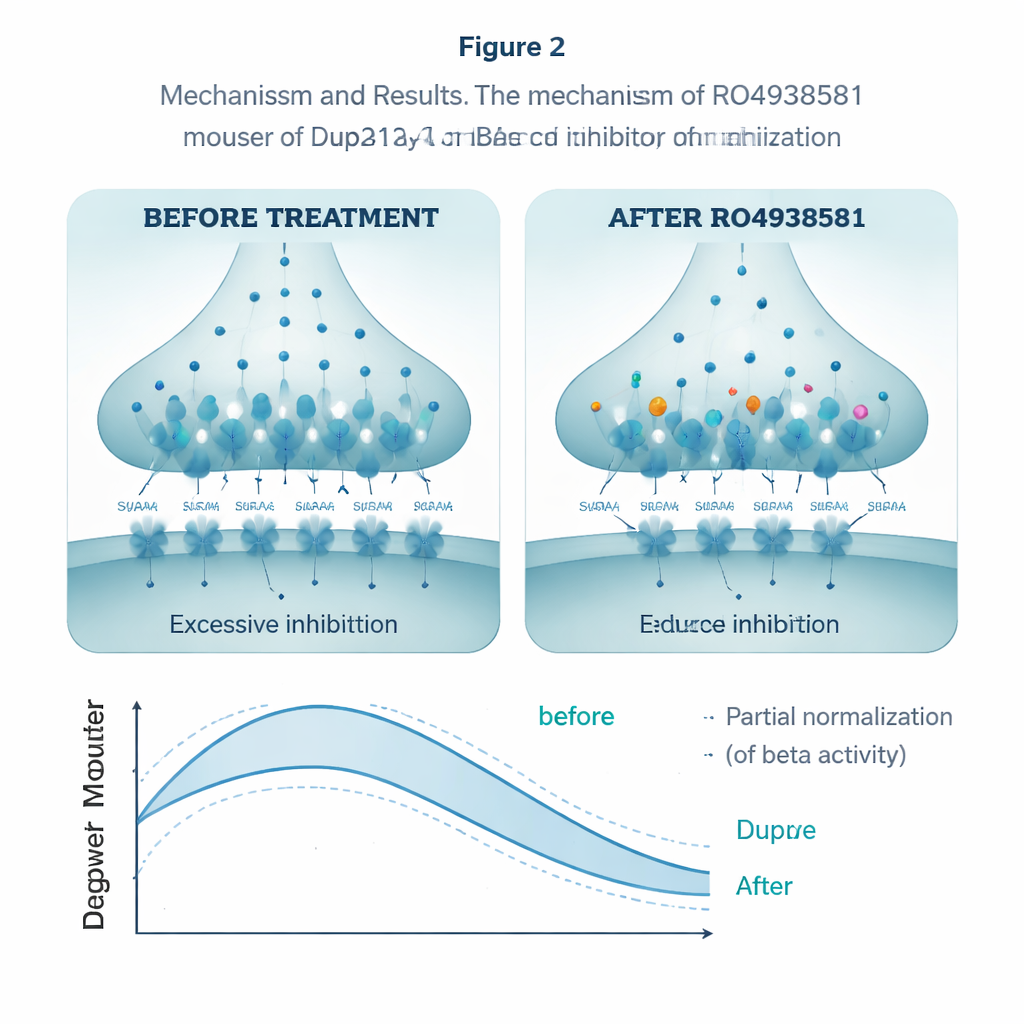
Was das für zukünftige Behandlungen bedeuten könnte
Für Familien mit Dup15q-Syndrom stellen diese Ergebnisse keine sofortige Heilung dar, aber sie liefern eine konkrete Spur. Die Arbeit macht einen bestimmten Rezeptor‑Subtyp — GABAA‑Rezeptoren, die die alpha‑5‑Untereinheit enthalten — als sowohl überproduziert als auch funktional wichtig in einem relevanten Tiermodell aus. Eine moderate Herabregulierung dieses Rezeptors mit einem negativen Modulator wie RO4938581 beseitigte nicht alle Probleme, verbesserte jedoch flexibles Lernen, soziales Verhalten und ein wichtiges EEG‑Biomarker. Diese Kombination aus Veränderungen auf Gehirn‑, Verhaltens‑ und Biomarker‑Ebene stärkt die Argumentation dafür, sicherere, für den Menschen geeignete alpha‑5‑gerichtete Wirkstoffe als Präzisionsbehandlungen für Dup15q und möglicherweise verwandte neuroentwicklungsbedingte Erkrankungen zu testen.
Zitation: Nakagawa, R., Nani, F., Hipp, J.F. et al. RO4938581, a GABAA-α5 negative allosteric modulator rescued behavioral and EEG phenotypes of a mouse model of Dup15q syndrome. Mol Psychiatry 31, 1351–1360 (2026). https://doi.org/10.1038/s41380-025-03247-y
Schlüsselwörter: Dup15q-Syndrom, GABAA-α5-Rezeptor, neuroentwicklungsstörung, EEG Beta‑Leistung, Mausmodell