Clear Sky Science · de
Kaskadierende inertiale Mikrofluidik zur hochdurchsatzfähigen, multiskaligen Anreicherung von Tumorzellen und intakten Clustern zur verbesserten Malignitätsdiagnostik
Warum das Sortieren von Krebszellen in Flüssigkeiten wichtig ist
Wenn Krebs sich ausbreitet, gelangen Tumorzellen häufig in die Flüssigkeiten, die unsere Organe umgeben. Bei Lungenkrebspatienten gehört dazu die sich um die Lungen ansammelnde Flüssigkeit, der Pleuraerguss. In dieser Flüssigkeit verbergen sich seltene einzelne Tumorzellen und dichte Zellverbände. Diese Cluster gelten als besonders gefährlich, da sie stark mit aggressivem Krankheitsverlauf und schlechten Prognosen verknüpft sind. Aktuelle Labormethoden tun sich jedoch schwer damit, sowohl einzelne Zellen als auch intakte Cluster schonend und effizient aus großen Patientenproben zu gewinnen. Die hier vorgestellte Studie führt eine neue chipbasierte Technologie ein, die solche Zellen schnell und behutsam aus Pleuraergüssen sortieren kann und damit die Tür zu verlässlicherer Krebsdiagnostik und besserem Verständnis der Tumorausbreitung öffnet.
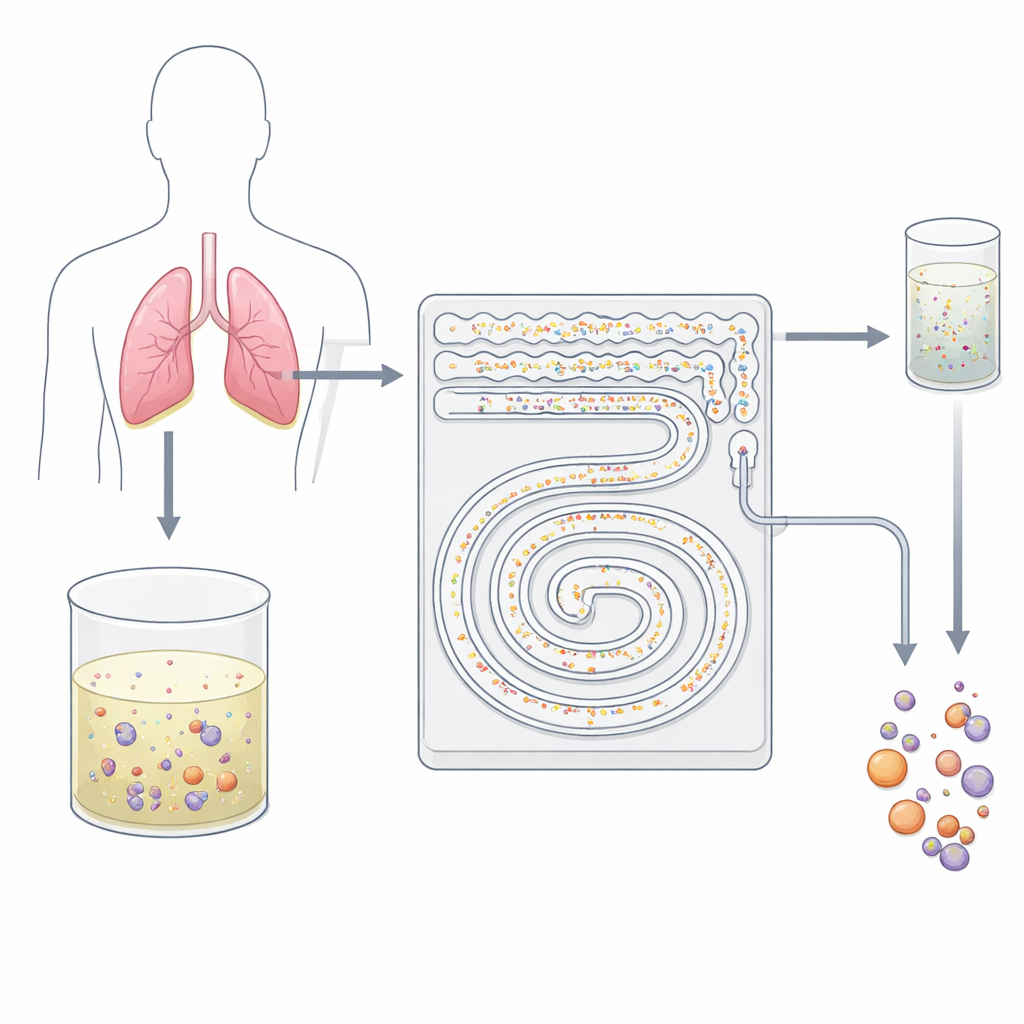
Ein schonendes Zellsieb auf einem Chip
Die Forscher entwickelten ein handtellergroßes Kunststoffgerät mit winzigen Kanälen, die wie ein intelligenter, zweistufiger Filter wirken. Statt klebender Antikörper oder grober Siebverfahren nutzt der Chip das Verhalten von Zellen in schnell fließender Flüssigkeit. Wenn Fluid durch gekrümmte Mikrokanäle strömt, treiben unsichtbare Kräfte Partikel unterschiedlicher Größe in verschiedene Stromlinien. Das Team nutzt diesen Effekt, allgemein als inertiale Mikrofluidik bezeichnet, um kleine Hintergrundblutzellen von größeren Tumorzellen und deren Clustern zu trennen, ohne sie zu berühren oder zu markieren. Weil alles in einem kontinuierlichen, geschlossenen Fluss abläuft, kann das Gerät innerhalb von Minuten mehrere zehn Milliliter Flüssigkeit verarbeiten — ein Tempo, das herkömmliche zytologische Präparate kaum erreichen.
Erster Schritt: Die Mengen reduzieren
Im ersten Abschnitt des Geräts wird der Pleuraerguss — nach Entfernen überschüssiger Flüssigkeit und Wiederaufbereitung der Zellen — durch ein Feld aus parallelen, geschlängelten Kanälen geleitet. Dort drängt die wirbelnde, gekrümmte Strömung kleine weiße Blutkörperchen Richtung Kanalwände, während größere Tumorzellen und Cluster in der Nähe der Strommitte verbleiben. Die kleinen Zellen werden zu Abflusskanälen geleitet und reduzieren so den Hintergrund drastisch. Dieser hochdurchsatzfähige Schritt arbeitet bei etwa 8 Millilitern pro Minute, sodass eine typische klinische Probe von 50 Millilitern in rund sechseinhalb Minuten ohne Verstopfung bearbeitet werden kann. Aus dieser ersten Stufe kommt ein deutlich saubereres Gemisch heraus, angereichert an potenziell malignen Zellen und bereit für eine feinere Trennung.
Zweiter Schritt: Einzelzellen von Clustern trennen
Die teilweise angereicherte Probe gelangt dann in einen schräg verlaufenden Spiralkanal mit einem wiederkehrenden Muster aus engen und weiten Abschnitten. In dieser Phase gleichen sich verschiedene Strömungskräfte für Objekte unterschiedlicher Größe unterschiedlich aus und lenken sie in separate Bahnen in der Nähe der inneren oder äußeren Wand der Spirale. Einzelne, tumorumartige Zellen, die kleiner sind, reihten sich an einer lateralen Position auf, während voluminösere Cluster zu einer anderen Position näher an der Innenwand wandern. Durch strategisch platzierte Ausgänge teilt der Chip diese Ströme physisch auf: Ein Ausgang sammelt hauptsächlich Einzel-Tumorzellen, ein anderer intakte Cluster, und weitere Ausgänge entfernen die verbleibenden kleinen Zellen. Wichtig ist, dass die Cluster intakt bleiben und so Schäden und Aufspaltungen vermieden werden, wie sie bei herkömmlichen Filtrationsmethoden häufig auftreten.
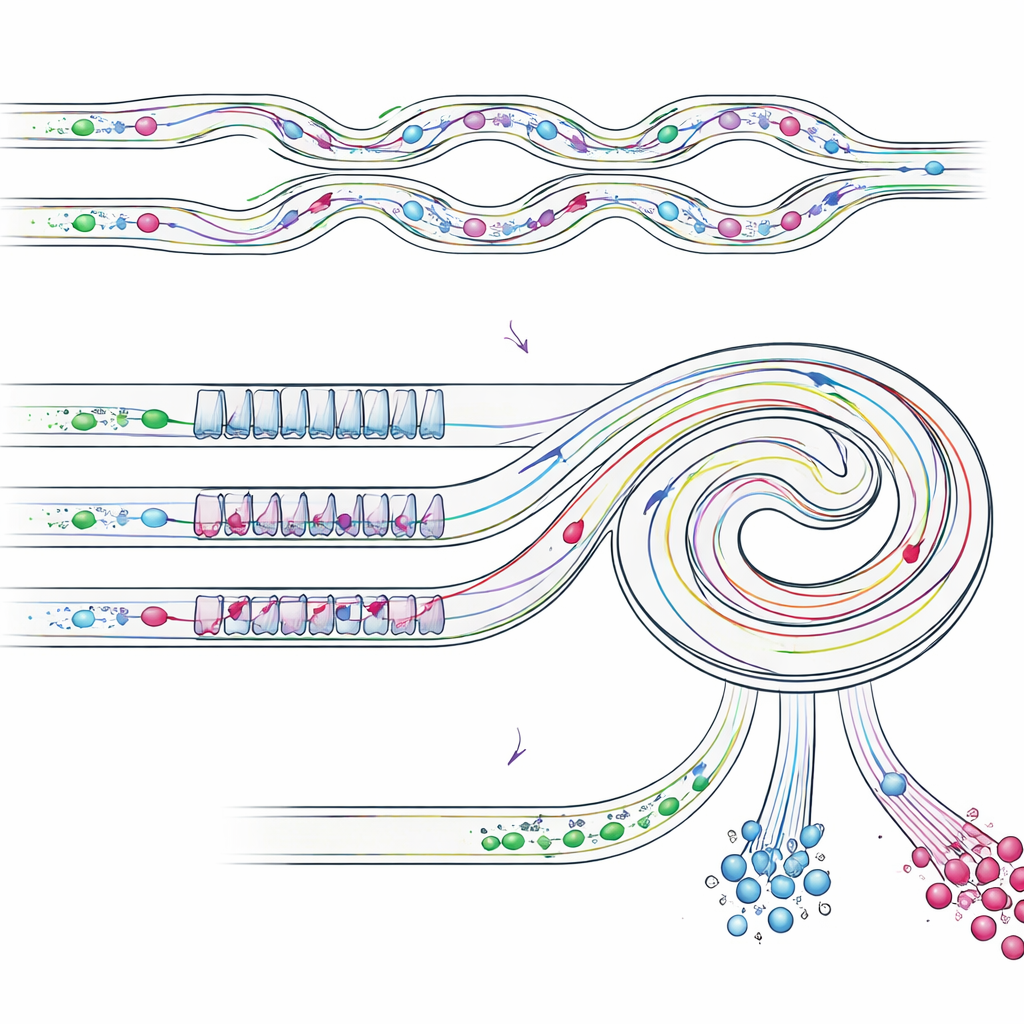
Das Gerät auf die Probe gestellt
Um die Leistungsfähigkeit ihres Designs zu prüfen, verwendete das Team zunächst Kunststoffkügelchen bekannter Größen als Modell für Blutzellen, einzelne Tumorzellen und Cluster. Sie zeigten, dass der kaskadierte Chip mehr als 87 % der „Einzelzell“-Kügelchen und etwa 92 % der „Cluster“-Kügelchen zurückgewann, während die meisten kleineren „Blutzell“-Kügelchen entfernt wurden. Anschließend testeten sie echte Lungenkrebszellen (A549-Zellen) gemischt mit weißen Blutkörperchen. In diesen Versuchen gewann das Gerät insgesamt etwa 82 % der Krebszellen zurück, mit rund 76 % Reinheit im angereicherten Fraktion und nahezu 80 % Reinheit für Zellcluster. Schließlich verarbeiteten sie tatsächliche Pleuraergussproben von drei Lungenkrebspatienten. Ausgehend von Flüssigkeiten, in denen Tumorzellen und Cluster weniger als 1 % aller Zellen ausmachten, erzeugte der Chip Fraktionen, in denen Einzelmalignomzellen etwa 68 % aller Zellen erreichten und Cluster in einem dedizierten Ausgangsstrom ungefähr 35 % der Zellen ausmachten.
Was das für Patienten bedeuten könnte
Indem es ausschließlich Strömung und Kanalgeometrie nutzt, kann dieses Gerät schnell und schonend sowohl einzelne Tumorzellen als auch intakte Cluster aus großen Volumina von Patientenflüssigkeiten gewinnen, ganz ohne chemische Marker oder komplexe Geräte. Die angereicherten Zellen bleiben für Standardtests wie immunfluoreszenzbasierte Färbung und Mikroskopie geeignet und lassen sich nahtlos in bestehende Krankenhausabläufe integrieren. Obwohl die aktuelle Studie nur wenige Patienten umfasste und größere Studien benötigt werden, um den Einfluss auf Diagnose und Prognose zu belegen, demonstriert die Arbeit ein starkes Konzept: einen schnellen, markierungsfreien „Zellkonzentrator“, der sowohl die Anzahl als auch den Clusterzustand von Tumorzellen in Pleuraergüssen sichtbar macht. Langfristig könnten solche Werkzeuge die Einschätzung der Malignität schärfen, personalisierte Therapieentscheidungen unterstützen und einen klareren Einblick in die Mechanismen der Metastasierung geben.
Zitation: Zhu, Z., Ren, H., Zhang, Z. et al. Cascading inertial microfluidics for high-throughput, multi-scale enrichment of tumor cells and intact clusters towards enhanced malignancy diagnosis. Microsyst Nanoeng 12, 101 (2026). https://doi.org/10.1038/s41378-026-01235-y
Schlüsselwörter: Liquid Biopsy, Mikrofluidische Zellseparation, Tumorzellcluster, Pleuraerguss, Krebsdiagnostik