Clear Sky Science · de
Entwurf eines automatisierten Zell-Chargen-Mikroinjektionssystems auf Basis von Magnetpinzetten für Zebrafisch-Embryonen
Warum winzige Fische wichtig sind
Bevor neue Medikamente oder Gentherapien beim Menschen eingesetzt werden, testen Wissenschaftler sie oft in kleinen, schnell wachsenden Tieren. Zebrafisch-Embryonen sind beliebt, weil sie transparent sind und sich rasch entwickeln, sodass Forschende die Organbildung in Echtzeit beobachten können. Um jedoch Gene zu verändern oder Wirkstoffe zu verabreichen, muss jedes empfindliche Ei mit einer mikroskopischen Nadel injiziert werden — eine Aufgabe, die in der Regel langsam, ermüdend und stark von der menschlichen Fertigkeit abhängig ist. Diese Arbeit stellt ein neues robotisches System vor, das Chargen von Zebrafisch-Embryonen automatisiert injizieren kann – schneller, schonender und zuverlässiger als ein Mensch – und so größere und konsistentere Experimente ermöglicht.
Eine neue Art, fragile Zellen zu handhaben
Bei der traditionellen Mikroinjektion steuert ein geschulter Bediener eine Glasnadel unter einem Mikroskop, findet jedes Embryo, dreht es in die richtige Orientierung und durchsticht es, ohne lebenswichtige Strukturen zu beschädigen. Das ist besonders schwierig, weil Embryonen weiche Kugeln sind mit Bereichen, die unbedingt geschont werden müssen. Bestehende robotische Systeme haben Transport und Durchstechen teilweise automatisiert, können aber typischerweise nicht die Rotation jedes Embryos in drei Dimensionen kontrollieren. Dadurch kann die Nadel in einem risikoreichen Winkel eindringen, was die Überlebensraten senkt und die zuverlässige Verarbeitung vieler Embryonen begrenzt. Das Team dieser Studie entwickelte eine vollständig integrierte Plattform, die Embryonen nacheinander transportiert, rotiert, injiziert und freigibt — ohne ständige Objektivwechsel oder manuelle Anpassungen.
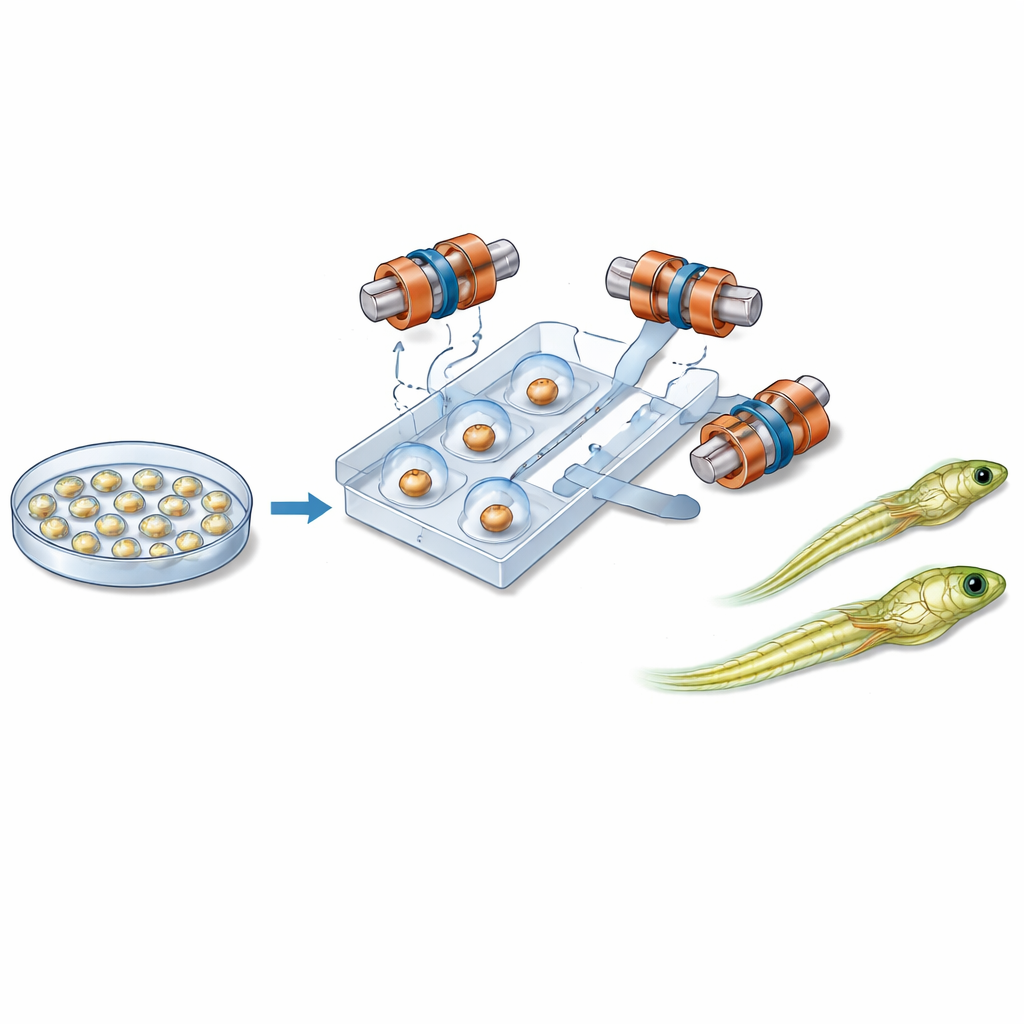
Magnete, Mikrokanäle und sanfte Steuerung
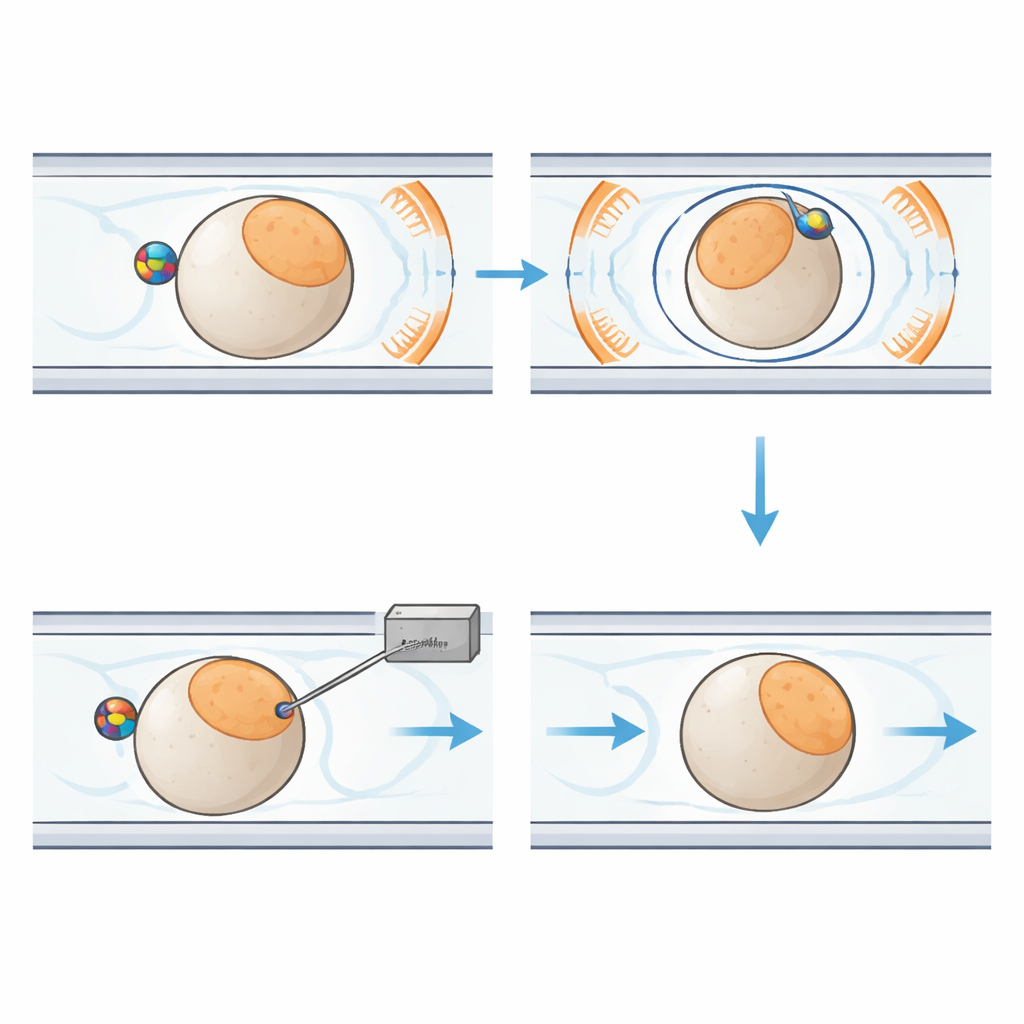
Im Zentrum des neuen Systems steht ein handflächengroßer Kunststoffchip mit schmalen Kanälen, die einzelne Embryonen entlang eines festen Pfads führen. Neben jedem Embryo sitzt eine kleine magnetische Kugel. Um den Chip herum erzeugen sechs sorgfältig angeordnete Spulen ein dreidimensional gleichmäßiges Magnetfeld. Durch zeitliche Änderung der Feldrichtung bringt das System die Magnetkugel in Rotation. Dank der Reibung zwischen Kugel und Embryooberfläche dreht sich die ganze Zelle mit, wie zwei ineinander greifende Zahnräder. So kann der Roboter das Embryo aus der Bildebene neigen oder innerhalb der Ebene drehen, bis die empfindliche Region sicher von der eintreffenden Nadel weg positioniert ist. Flüssigkeit und sanfter Luftdruck bewegen und positionieren die Embryonen, während ein separates Modul die Injektionsnadel und den winzigen Fluss des genetischen Materials steuert.
Klar sehen im winzigen Sichtfeld
Damit diese präzise Choreografie möglich wird, entwickelten die Forschenden außerdem ein fortgeschrittenes Computer-Vision-System, das microscopic manipulation perception network. Es analysiert Mikroskopkamerabilder in Echtzeit, um jedes Embryo zu erkennen, die feine Nadelspitze zu detektieren und die beiden gegenüberliegenden „Pole“ des Eis zu unterscheiden, an denen wichtige Entwicklungsstrukturen liegen. Das Netzwerk nutzt moderne Deep-Learning-Techniken — etwa doppelte Merkmalsextraktionswege, Aufmerksamkeitsmodule, die wichtige Details hervorheben, und Multiskalenfusion von Bildinformationen —, um sich in der überfüllten, schwach beleuchteten Welt innerhalb eines microfluidischen Chips zurechtzufinden. In Tests an tausenden Bildern erkannte es Objekte und segmentierte Embryobereiche mit etwa 98–99 % Genauigkeit und lieferte so die zuverlässige Rückmeldung, die nötig ist, um sowohl magnetische Drehung als auch Nadelausrichtung zu steuern.
Nachweis der Wirksamkeit in lebenden Zebrafischen
Das Team verglich sein automatisiertes System mit erfahrenen menschlichen Bedienern, jeweils anhand von 100 Zebrafisch-Embryonen. Der Roboter führte die Injektionen in etwa 33,8 Sekunden pro Embryo durch — mehr als doppelt so schnell wie manuelle Arbeit — und durchstach jede Zelle erfolgreich. Er orientierte außerdem jedes Embryo mit einem mittleren Winkelabweichungsfehler von nur 2,1 Grad, ungefähr halb so groß wie bei menschlichen Bedienern. Am wichtigsten: 88 % der robotergestützten Embryonen überlebten bis zum Schlüpfen als Larven, verglichen mit 66 % nach manueller Injektion. Unter dem Fluoreszenzmikroskop leuchteten die Larven aus dem automatisierten System grün, was zeigt, dass das eingeführte genetische Material aufgenommen und wie geplant exprimiert wurde. Indem Embryonen magnetisch rotiert statt mechanisch gequetscht wurden, minimierte das System Verformung und Schäden bei gleichzeitig hoher Durchsatzrate.
Was das für künftige Studien bedeutet
Kurz gesagt zeigt diese Arbeit, dass eine sorgfältig konstruierte Kombination aus Mikrokanälen, magnetischer Steuerung und intelligenter Bildanalyse fragile Fischembryonen schneller und mit besserer Überlebensrate injizieren kann als ein erfahrener Mensch mit traditionellen Werkzeugen. Da Zebrafische eine Schlüsselplattform zur Untersuchung von Entwicklung, Krankheit und Medikamentenwirkung sind, könnte ein zuverlässiger Hochdurchsatz-Injektor große genetische Screens und langfristige biologische Studien beschleunigen, die bisher durch manuelle Arbeit begrenzt waren. Mit geeigneten Anpassungen am Chipdesign und den Steuerparametern ließe sich die gleiche Strategie auf andere Zelltypen und kleine Organismen übertragen und so empfindliche zelluläre Eingriffe von einer Kunst weniger Spezialisten in einen automatisierten, standardisierten Prozess überführen.
Zitation: Guo, X., Wang, F., Zhao, A. et al. Design of an automated cell batch microinjection system based on magnetic tweezers for zebrafish embryos. Microsyst Nanoeng 12, 113 (2026). https://doi.org/10.1038/s41378-026-01230-3
Schlüsselwörter: Zebrafisch-Embryonen, Mikroinjektion, magnetische Pinzetten, Microfluidik, robotische Zellmanipulation