Clear Sky Science · de
Extrem empfindliche, labelfreie Biosensorplattform basierend auf topologisch störender Phasen-Nanooptik
Warum es wichtig ist, das Unsichtbare zu sehen
Viele Krankheiten, darunter Krebs und neurodegenerative Erkrankungen, setzen lange vor dem Auftreten von Symptomen charakteristische Moleküle in unser Blut frei. Heutige Diagnosetests übersehen diese frühen Anzeichen oft, weil die Moleküle zu klein oder zu selten sind, um zuverlässig nachgewiesen zu werden. Dieser Beitrag beschreibt einen neuen optischen Sensor, der winzige Mengen solcher Biomoleküle ohne fluoreszierende Markierungen oder chemische Labels erkennen kann. Durch das Gestalten von Materialien im Bereich weniger Atomschichten nutzen die Autoren subtile Verschiebungen des Lichts, um winzige biochemische Ereignisse in große, leicht messbare Signale zu verwandeln.
Licht in einen hochempfindlichen Detektor verwandeln
Konventionelle plasmonische Biosensoren arbeiten, indem Licht auf eine dünne Metallschicht gestrahlt wird und man beobachtet, wie sich das reflektierte Licht verändert, wenn Moleküle an der Oberfläche anlagern. Diese Geräte sind bereits empfindlich, haben jedoch Schwierigkeiten mit sehr kleinen Molekülen oder extrem niedrigen Konzentrationen. Anstatt Helligkeit oder Farbe zu messen, konzentriert sich die neue Plattform auf die Phase des Lichts — den genauen Zeitpunkt seiner Wellenfront. Unter besonderen Bedingungen verschwindet das reflektierte Licht nahezu und seine Phase ändert sich extrem schnell. Diese Punkte, bekannt als optische „dunkle“ Zustände oder Phasensingularitäten, machen das System außerordentlich reaktionsschnell gegenüber selbst geringfügigen Veränderungen in der Nähe der Metalloberfläche.
Ein nanoskaliger Lichtfallen-Aufbau
Um diese Singularitäten zu erzeugen, entwarf das Team eine geschichtete Struktur von nur wenigen Dutzend Nanometern Dicke. Eine Glasbasis trägt eine 12-Nanometer-Schicht Aluminiumoxid, die ultrakleine Silbernanopartikel mit weniger als 3 Nanometern Durchmesser enthält, alles bedeckt von einer glatten, 48-Nanometer-dicken Goldschicht. Die Silberpartikel werden so erzeugt und eingebettet, dass sie kristallin, nahezu kugelförmig und gleichmäßig im Abstand von weniger als einem Nanometer verteilt bleiben. Diese Anordnung erlaubt es, dass die lokalisierten Plasmonenmoden der Partikel stark miteinander und mit den laufenden Plasmonwellen in der Goldschicht koppeln. Das Ergebnis ist eine Art nanoskaliger optischer Resonator, in dem Lichtenergie stark eingeschlossen wird und dessen Phase extrem empfindlich auf das umgebende Medium reagiert.
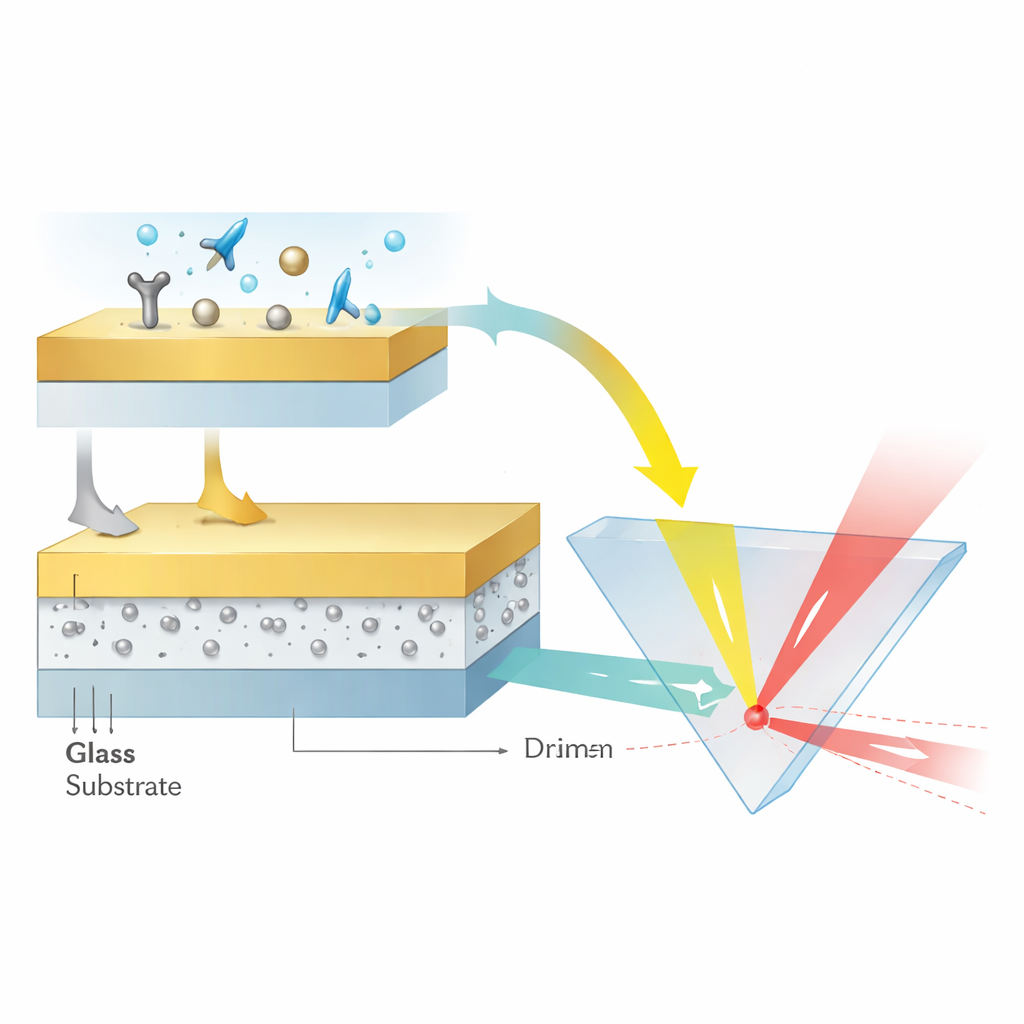
Das Licht seitlich verschieben lassen
Anstatt Winkel oder Farben zu messen, lesen die Autoren ihren Sensor aus, indem sie verfolgen, wie weit der reflektierte Lichtstrahl seitlich entlang der Oberfläche verschoben wird — ein Phänomen, das als Goos–Hänchen-Verschiebung bezeichnet wird. Wenn ein Laserstrahl unter den richtigen Bedingungen reflektiert wird, kann sein Energiepeak leicht versetzt auftreten gegenüber der einfachen geometrischen Erwartung. In der Nähe einer Phasensingularität wächst diese Verschiebung dramatisch. Durch Einstellung der Silbernanopartikelkonzentration auf etwa 16 Prozent brachten die Forscher die Reflexion nahe null und schärften den Phasensprung so weit, dass winzige Änderungen des Brechungsindexes, verursacht durch Moleküle, die an der Goldoberfläche binden, laterale Strahlverschiebungen von Hunderten von Mikrometern erzeugten. In Kalibrierungstests mit verdünnten Glycerinlösungen erreichte das Gerät eine Empfindlichkeit entsprechend 3,27 × 10^8 Nanometern Strahlverschiebung pro Einheitsänderung des Brechungsindex und löste Änderungen von etwa vier Teilen in zehn Millionen auf.
Kleine Moleküle bei verschwindend geringen Konzentrationen nachweisen
Um die praktische Biosensorik zu demonstrieren, richteten die Forschenden zunächst ihr Ziel auf Biotin, ein vitaminähnliches Molekül mit sehr geringer Molekülmasse. Standardoberflächenplasmonensensoren können Biotin selbst in Mikromolar-Konzentrationen nicht zuverlässig erkennen. Hier verfolgte die neue Plattform durch das Funktionalisieren der Goldoberfläche mit Streptavidin, das Biotin stark bindet, die Echtzeitbindung eindeutig bei Konzentrationen bis hinunter zu 1 Femtomolar — etwa ein Molekül unter 10^15 Lösungsmolekülen. Das Signal nahm bei jeder zehnfachen Konzentrationssteigerung stetig zu, was bestätigt, dass die Strahlverschiebung vorhersehbar mit der Bedeckung durch solche winzigen Analyten skaliert.
Auf der Suche nach Krebsmarkern im Attowelt-Bereich
Das Team wandte sich dann einem klinisch relevanten Ziel zu: Tumornekrosefaktor-alpha (TNF-α), einem Zytokin, das mit Entzündung und Krebs assoziiert ist und in Patientenserum bei etwa 10^−13 molar vorkommt. Sie funktionalisierten die Goldoberfläche mit kurzen DNA-Strängen (Aptameren), die TNF-α spezifisch erfassen, und blockierten verbleibende Flächen, um unspezifische Bindung zu unterdrücken. Unter diesen Bedingungen registrierte der Sensor klare, stabile Signale für TNF-α bei Konzentrationen bis hinunter zu 0,1 Attomolar (10^−19 molar) und erzeugte bei 10^−13 molar eine Verschiebung von nahezu 47 Mikrometern — deutlich im medizinisch relevanten Bereich. Kontrolltests mit einem anderen Zytokin, Interleukin-6, zeigten nahezu kein anhaltendes Signal, was bestätigt, dass die Reaktion sowohl hochsensitiv als auch selektiv war.
Was das für künftige medizinische Tests bedeutet
Kurz gesagt zeigt diese Arbeit, dass sorgfältig angeordnete Silbernanopartikel, verborgen unter einer dünnen Goldschicht, eine fast unmerkliche Veränderung an der Oberfläche in eine große seitliche Lichtbewegung verwandeln können, die leicht zu messen ist. Durch das Arbeiten an Phasensingularitäten umgeht die Plattform die Notwendigkeit fluoreszenter Labels und verschiebt die Empfindlichkeit in den ZEPTO- bis ATTOmolaren Bereich für reale biologische Ziele. Wenn sich das Prinzip in robuste, benutzerfreundliche Geräte übersetzen lässt, könnten solche Sensoren Bluttests ermöglichen, die Krankheitsmarker lange vor den heutigen Methoden erkennen — und damit neue Möglichkeiten für Früherkennung und Echtzeitüberwachung der Gesundheit eröffnen.
Zitation: Du, F., Gireau, M., Youssef, J. et al. Extreme sensitivity label-free biosensing platform based on topologically disruptive phase nano-optics. Microsyst Nanoeng 12, 106 (2026). https://doi.org/10.1038/s41378-026-01222-3
Schlüsselwörter: labelfreie Biosensorik, plasmonischer Sensor, Nanopartikel, früherkrankungserkennung, Krebs-Biomarker