Clear Sky Science · de
PEGylierten, mit Kupfer dotierten WS2‑Hybrid‑Nanosheets für zielgerichtete multimodale Krebstherapie
Warum klügere Krebsbehandlungen wichtig sind
Viele Menschen mit Brustkrebs stehen weiterhin harten Behandlungen gegenüber, die gesundes Gewebe schädigen können, ohne den Tumor vollständig zu stoppen. Diese Studie beschreibt eine neue Art winziger, gezielt entwickelter Schichten, zu klein, um sie mit bloßem Auge zu sehen, die so konstruiert sind, dass sie sich im Körper verteilen, Brusttumoren ansteuern und diese auf mehreren koordinierten Wegen gleichzeitig angreifen. Indem Hitze, chemische Reaktionen und ein klassisches Krebsmedikament in einem einzigen zielgerichteten Paket kombiniert werden, wollen die Forscher die Therapie sowohl wirkungsvoller als auch schonender für den übrigen Körper machen. 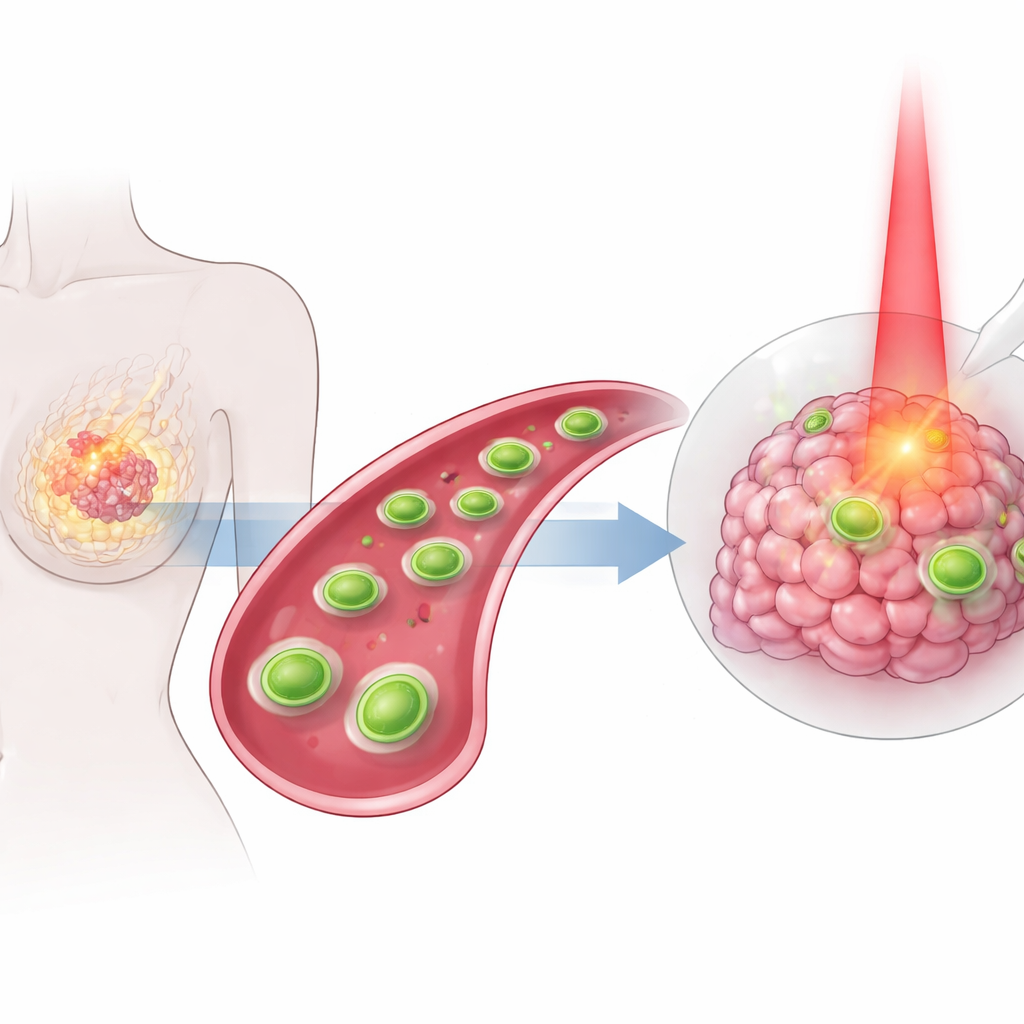
Winzige Schichten, gebaut zum Tragen und Freisetzen von Therapie
Das Herzstück des Ansatzes ist ein ultradünnes Material aus Wolfram und Schwefel, geformt als nanoskalige Blättchen. Diese Schichten absorbieren natürlicherweise nahes Infrarotlicht und wandeln es in Wärme um. Das Team stellte zunächst diese Schichten her und rauhte dann gezielt ihre Oberfläche auf, damit sie andere nützliche Bestandteile aufnehmen können. Kupferatome wurden in hochdisperser Form auf den Schichten verankert, und eine weiche, flexible Beschichtung ähnlich einem molekularen „Regenmantel“ wurde hinzugefügt, um die Partikel besser in Körperflüssigkeiten zu dispergieren und ein Verklumpen zu verhindern. Schließlich wurde Folsäure — ein Vitamin, das viele Tumorzellen verstärkt aufnehmen — als Zielmolekül angebracht und das gängige Chemotherapeutikum Doxorubicin auf der Oberfläche geladen. Das Endergebnis ist eine winzige, geschichtete Plattform, die im Blut zirkulieren, Tumorzellen erkennen und eine beträchtliche Ladung an Wirkstoffen transportieren kann.
Wie Licht, Chemie und Wirkstoff zusammenwirken
Sobald diese Partikel einen Tumor erreichen, laufen mehrere Prozesse gleichzeitig ab. Wenn der Tumorbereich mit einem sanften Rotlaser bestrahlt wird, erwärmen sich die Wolfram‑Schwefel‑Schichten effizient und erhöhen die lokale Temperatur so weit, dass Krebszellen gestresst und geschädigt werden, ohne den Rest des Körpers zu überhitzen. Gleichzeitig reagieren die Kupferatome auf den Schichten mit natürlich vorkommenden Peroxidemolekülen, die in Tumoren oft erhöht sind. Diese Reaktion wandelt das Peroxid in sehr reaktive, kurzlebige Oxidantien um, die Zellbestandteile von innen zerstören. Tumoren sind außerdem meist etwas saurer als gesundes Gewebe; in diesem sauren Milieu und unter Erwärmung durch den Laser schwächt sich die Bindung zwischen Schicht und Doxorubicin, wodurch mehr des Medikaments genau dort freigesetzt wird, wo es gebraucht wird. Diese drei Effekte — Hitze, chemischer Angriff und fokussierte Chemotherapie — sind so ausgelegt, dass sie sich gegenseitig verstärken. 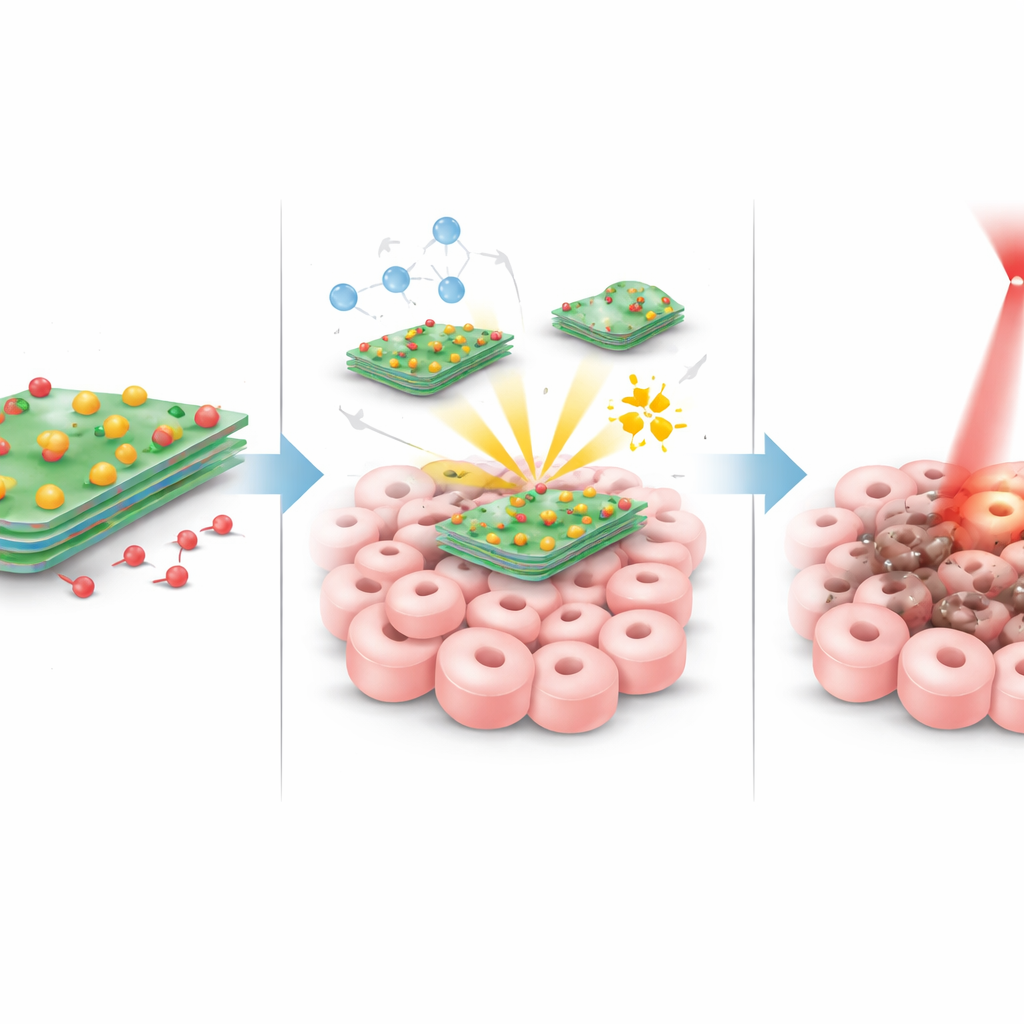
Belege aus Zellen und tumorbefallenen Mäusen
In Zellkulturen zeigten die beschichteten Schichten allein nur geringe Schädigung normaler Zellen, was auf eine gute grundlegende Verträglichkeit hindeutet. Wurden sie jedoch mit Doxorubicin beladen und in Gegenwart von Peroxid dem Laserlicht ausgesetzt, führten sie zu einem starken Absterben von Brustkrebszellen — deutlich stärker als jede Einzelbehandlung. Die Forschenden konnten zudem nachweisen, dass die Partikel eine Welle reaktiver Oxidantien innerhalb von Tumorzellen erzeugen, was bestätigt, dass die Kupferchemie aktiv ist. Bei Mäusen mit Brusttumoren akkumulierten Partikel mit Folsäurebeschichtung deutlich stärker und länger im Tumorgewebe als nicht zielgerichtete Partikel. Erhielten die Mäuse die vollständige Kombination — zielgerichtete Partikel plus Rotlichtbestrahlung — schrumpften ihre Tumoren dramatisch, die Überlebenszeit verlängerte sich, und Körpergewicht sowie Organbefund blieben weitgehend normal, was auf begrenzte Nebenwirkungen im Vergleich zur Standardmedikation hindeutet.
Was dies für die zukünftige Krebsversorgung bedeuten könnte
Insgesamt deuten die Ergebnisse darauf hin, dass diese konstruierten Schichten wie ein multifunktionales Werkzeug für die Krebstherapie wirken: Sie spüren Tumoren auf, erhitzen sie, vergiften sie von innen durch reaktive Chemie und liefern ein bewährtes Medikament präziser, während sie den Großteil des restlichen Körpers schonen. Die Arbeit befindet sich noch im Tierexperimentstadium, und wichtige Fragen zur Langzeitverträglichkeit, zum Abbau und zur praktikablen Herstellung solcher Partikel für den Menschen bleiben offen. Dennoch zeigt das Design, wie die Kombination mehrerer bescheidener Behandlungsformen in einem einzigen intelligenten Paket, das auf das Tumormilieu zugeschnitten ist, eine deutlich stärkere Gesamtwirkung erzielen kann. Bestätigen zukünftige Studien Sicherheit und Wirksamkeit, könnten derartige multifunktionale Nanoplattformen die Brustkrebsbehandlung zielgerichteter, effizienter und weniger belastend für Patientinnen und Patienten machen.
Zitation: Li, D., Wen, C., Wu, H. et al. PEGylated Cu-doped WS2 hybrid nanosheets for targeted multimodal cancer therapy. Microsyst Nanoeng 12, 121 (2026). https://doi.org/10.1038/s41378-026-01218-z
Schlüsselwörter: Brustkrebsbehandlung, Nanomedizin, photothermale Behandlung, zielgerichtete Wirkstofffreisetzung, chemodynamische Therapie