Clear Sky Science · de
Schnell herstellbares und kostengünstiges einlagiges Mikrofluidikgerät zur hochdurchsatzfähigen dreidimensionalen hydrodynamischen Fokussierung
Warum das Verengen winziger Ströme wichtig ist
Die moderne Medizin ist zunehmend darauf angewiesen, sehr viele einzelne Zellen nacheinander zu betrachten, zum Beispiel um Krebszellen im Urin oder Blut zu entdecken. Um dies schnell und kostengünstig zu tun, werden Zellen oft durch haarfeine Kanäle auf Mikrochips geleitet, wo Laser oder Kameras sie untersuchen. Damit bei extrem hohen Geschwindigkeiten scharfe, zuverlässige Bilder entstehen, muss jede Zelle nahezu exakt dieselbe winzige Stelle passieren. Diese Arbeit stellt eine neue Methode vor, solche Chips so zu bauen, dass sie Zellen selbst bei sehr hohen Geschwindigkeiten dicht in einem schmalen dreidimensionalen Strom bündeln — mit einem Gerät, das schneller und günstiger herzustellen ist als heutige Standardsysteme.
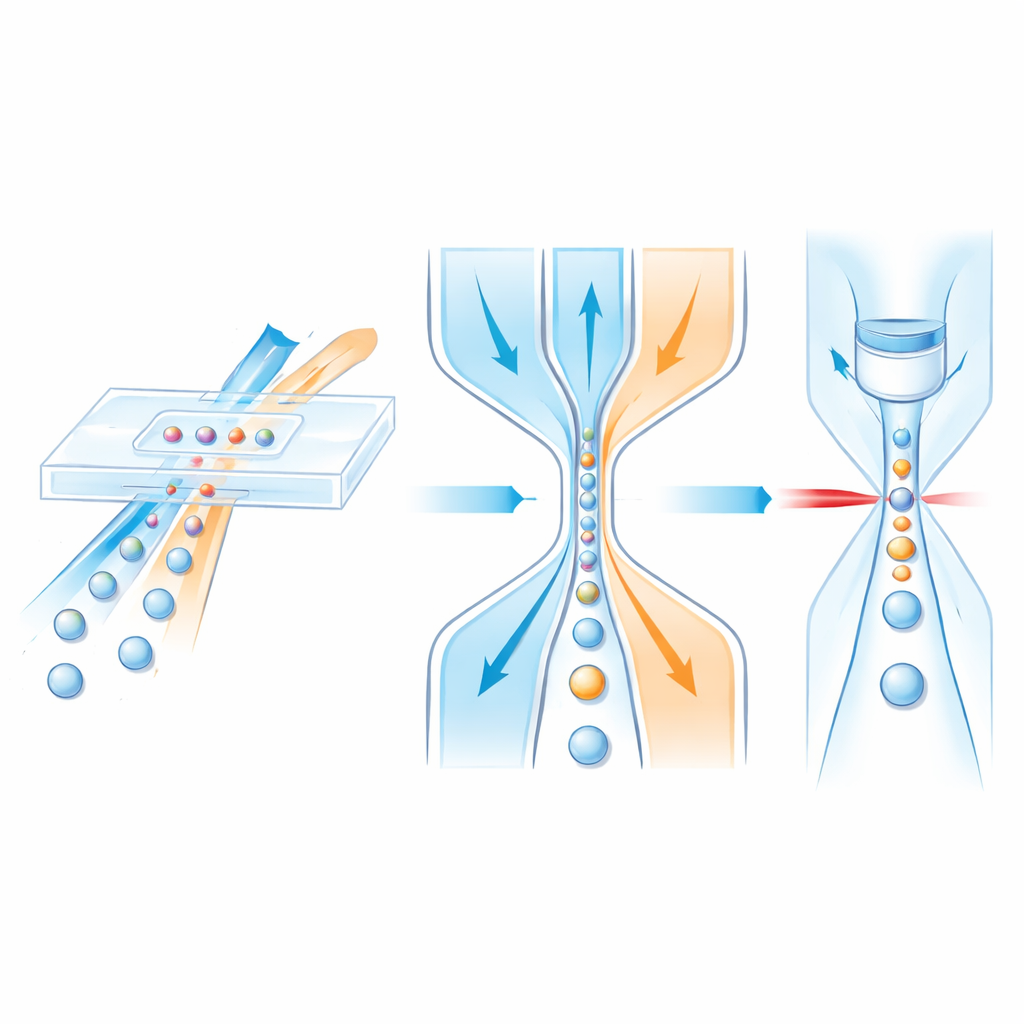
Zellen mit fließenden „Fahrspuren“ führen
Innerhalb eines Mikrofluidikchips bewegen sich Zellen in einem zentralen Probenstrom, während umgebende „Hüll“-Flüssigkeiten wie unsichtbare Leitplanken wirken und die Probe sanft zur Mitte drücken. Frühere Designs konnten Zellen meist nur seitlich fokussieren, nicht in der Höhe, oder sie beruhten auf komplexen mehrlagigen Strukturen, die langsam und kostenintensiv in der Herstellung sind. Die Autoren entwerfen stattdessen einen einlagigen Kanal, der dennoch vollständige dreidimensionale Kontrolle erreicht. Zunächst trifft die Probe an einer schrägen T-förmigen Verzweigung auf einen vertikalen Hüllstrom, der sich längs verengt. Durch die Kanalform und die Trägheit der Flüssigkeiten bei höheren Geschwindigkeiten wird der Probenstrom in die obere Kanalfalte gedrückt. Weiter stromabwärts drücken zwei seitliche Hüllströme von links und rechts und quetschen die bereits angehobene Probe zu einem engen zentralen Filament, das durch ein Detektionsfenster läuft.
Bessere Chips in Minuten statt Stunden bauen
Die meisten mikrofluidischen Forschungschips bestehen heute aus weichem Silikon (PDMS) und werden mittels Softlithographie hergestellt — ein Verfahren mit mehrfachen Heiz- und Aushärteschritten, das pro Gerät eine Stunde oder länger dauern kann. PDMS lässt sich zwar leicht formen, verformt sich aber unter hohem Druck, sodass sich die Kanäle aufwölben und der fokussierte Strom auseinanderläuft. Das neue Gerät nutzt einen harten Kunststoff namens Polyurethanacrylat (PUA), der in einem „Doppeltransfer“-Verfahren strukturiert wird. Zuerst wird aus einem Siliziummaster eine wiederverwendbare PDMS-Form mit erhabenen Kanalmerkmalen gegossen. Flüssiges PUA wird dann in diese Form gegossen, unter UV-Licht gehärtet und abgezogen, um die Kanalschicht zu bilden. Eine separate, flach mit PUA beschichtete Glasscheibe dient als Basis. Die beiden PUA-Oberflächen werden ausgerichtet, aufeinander gepresst und mit einer weiteren kurzen UV-Belichtung verbunden. Da jeder Aushärteschritt nur Sekunden dauert und kein langes Backen erforderlich ist, kann ein kompletter Chip in etwa fünf Minuten hergestellt werden — ungefähr zehnmal schneller als traditionelle Methoden.
Den Durchfluss testen und Verformung zähmen
Um zu verstehen, wie gut das Design funktioniert, kombiniert das Team Computersimulationen mit Experimenten. Zuerst simulieren sie, wie Änderungen der Flussraten von Probe und Hüllströmen die Form des fokussierten Kerns beeinflussen. Die Ergebnisse zeigen, dass sowohl erhöhte vertikale als auch seitliche Hüllflüsse dazu beitragen, die Probe in Höhe und Breite zu verengen, und dass höhere Gesamtraten (höhere Reynolds-Zahl) die Fokussierung weiter verbessern. Anschließend simulieren sie, wie sich die Kanalwände bei weichem PDMS gegenüber steifem PUA verformen. Unter realistischen Hochgeschwindigkeitsbedingungen wölben sich PDMS-Wände um über hundert Mikrometer, genug, um den Fluss so stark zu verzerren, dass die Probe splittert und zu den Ecken abdriftet. Im Gegensatz dazu verformt sich PUA um weniger als hundert Nanometer — in diesem Maßstab effektiv starr —, sodass der fokussierte Strom auch bei hohem Druck zentriert und eng bleibt.
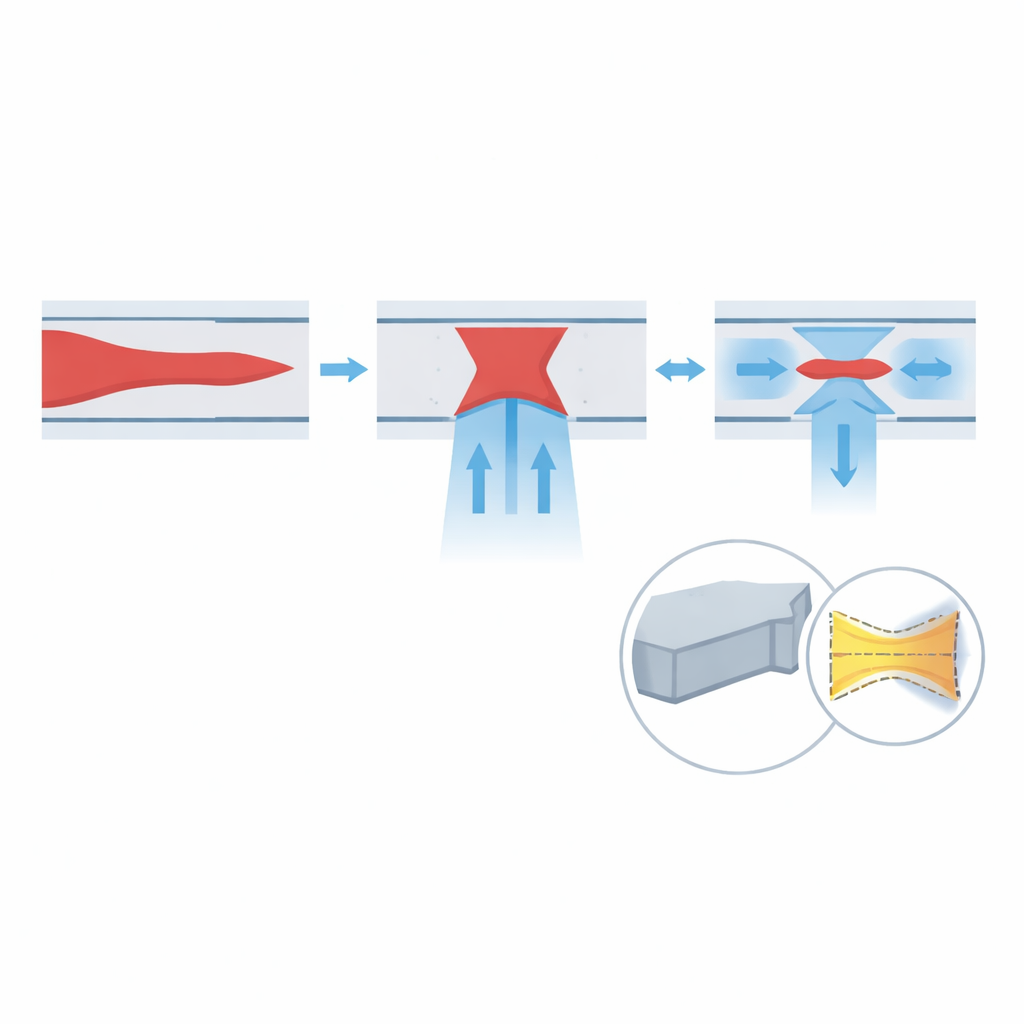
Reale Zellen bei extremen Geschwindigkeiten beobachten
Über Farbstofftests hinaus bewerten die Autoren das Gerät mit optischer Time-Stretch-(OTS-)Mikroskopie, einer Technik, die ultraschnelle Laserpulse in schnelle Zeilenscans umwandelt und Millionen von Zeilenbildern pro Sekunde ermöglicht. Sie leiten behandeltes Urinmaterial von Blasenkrebspatienten mit steigenden Flussraten durch den Chip, während OTS zweidimensionale Bilder jeder vorbeiziehenden Zelle aufzeichnet. Da das optische System eine sehr dünne Fokalregion hat, erscheint jede Zelle, die nach oben oder unten ausweicht, unscharf — ein direkter Maßstab für die vertikale Fokussierung. Über Geschwindigkeiten von 3,3 bis 16,7 Metern pro Sekunde steigt der Anteil scharf fokussierter Bilder an und erreicht bei der höchsten getesteten Geschwindigkeit 98,4 %. Die laterale Fokussierung wird gemessen, indem ermittelt wird, wie weit Zellzentren vom Kanalmittelpunkt abweichen; dieser Versatz nimmt mit der Geschwindigkeit ab, entsprechend etwa 95,0 % lateraler Fokussierungseffizienz bei 16,7 Metern pro Sekunde.
Was das für die zukünftige Zellanalyse bedeutet
Einfach ausgedrückt zeigen die Forscher, dass ein geradliniger, einlagiger Kunststoffchip Zellen zuverlässig in einem engen, gut kontrollierten Strom in alle Richtungen führen kann, selbst unter den anspruchsvollen Bedingungen, die für ultraschnelle Bildgebung nötig sind. Durch die Kombination eines verformungsresistenten Materials mit einer durchdachten Anordnung von Hüllströmen umgehen sie die mechanischen Grenzen weicher Silikongeräte und verkürzen gleichzeitig die Fertigungszeit drastisch. Das erleichtert die Produktion vieler identischer Chips für klinische und industrielle Anwendungen und ermöglicht groß angelegte Hochdurchsatztests an echten Patientenproben. Damit bietet die Technologie einen praktischen Weg zu schnelleren, präziseren Screening-Werkzeugen für Zellen, die Diagnostik, Krebsmonitoring und andere Anwendungen unterstützen könnten, die auf die genaue Untersuchung großer Zellmengen angewiesen sind.
Zitation: Yan, R., Wei, S., Weng, Y. et al. Rapid-manufacturing and cost-effective single-layer microfluidic device for high-throughput three-dimensional hydrodynamic focusing. Microsyst Nanoeng 12, 87 (2026). https://doi.org/10.1038/s41378-026-01212-5
Schlüsselwörter: Mikrofluidische Durchflusszytometrie, 3D-hydrodynamische Fokussierung, hochdurchsatzfähige Einzelzellanalyse, Polyurethanacrylat-Mikrofluidikchips, optische Time-Stretch-Mikroskopie