Clear Sky Science · de
Robotisches Zelltransportsystem basierend auf Modellierung des Widerstands in Mikropipetten
Kleine Zellen bewegen — ganz ohne Mikroskop
Die moderne Biologie hängt oft von einer überraschend einfachen Aufgabe ab: eine einzelne Zelle mit einem Glasröhrchen aufzunehmen und an einen anderen Ort zu platzieren. Das ist essenziell für Fruchtbarkeitsbehandlungen, Embryoneneinfrieren, zellbasierte Therapien und Grundlagenforschung. Heute erfordert das fast immer ein sperriges Mikroskop und eine hochqualifizierte Person, die jede Bewegung visuell überwacht. Dieser Artikel beschreibt ein neues Robotersystem, das einzelne Zellen zwischen Flüssigkeitströpfchen bewegen kann, ganz ohne mikroskopische Sicht — und damit den Weg zu vollständig geschlossenen, automatisierten ‚Zellfabriken‘ öffnet, die schneller, günstiger und schonender für empfindliche Zellen arbeiten können.
Warum das Zellverhalten ein Update braucht
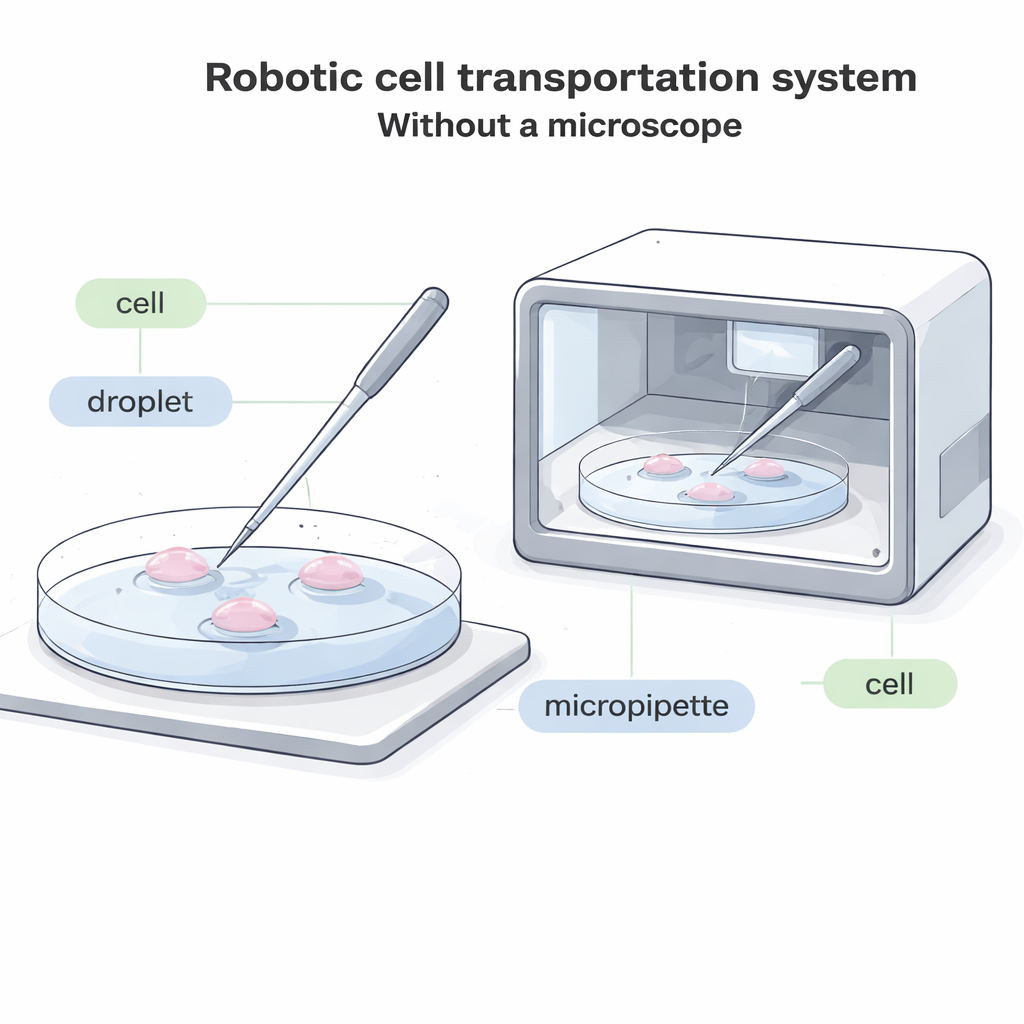
In heutigen Laboren beobachtet eine Bedienperson durch ein Mikroskop und benutzt eine dünne Glasröhre, die Mikropipette, um den Boden einer Schale zu erreichen, eine Zelle sanft einzusaugen, sie in einen neuen Flüssigkeitstropfen zu verschieben und dort wieder auszustoßen. Dieser Prozess ist langsam, visuell anspruchsvoll und schwer zu automatisieren. In vielen zukünftigen Systemen — etwa kompakten, verschlossenen Geräten, die Embryonen oder andere Zellen in einem Behälter kultivieren — ist schlicht kein Platz für ein herkömmliches Mikroskop. In anderen Fällen werden Zellen mit fluoreszierenden Farbstoffen markiert, die verblassen oder lichtempfindlich sein können; deshalb ist es wichtig, intensive mikroskopische Beobachtung zu minimieren. Bestehende ‚blinde‘ Systeme, die ohne Bildgebung arbeiten, funktionieren nur für ungewöhnlich große Zellen, sodass die meisten gängigen Zelltypen keine praktikable automatisierte Lösung haben.
Ein Spezialstroh mit eingebauter Stoppeinrichtung
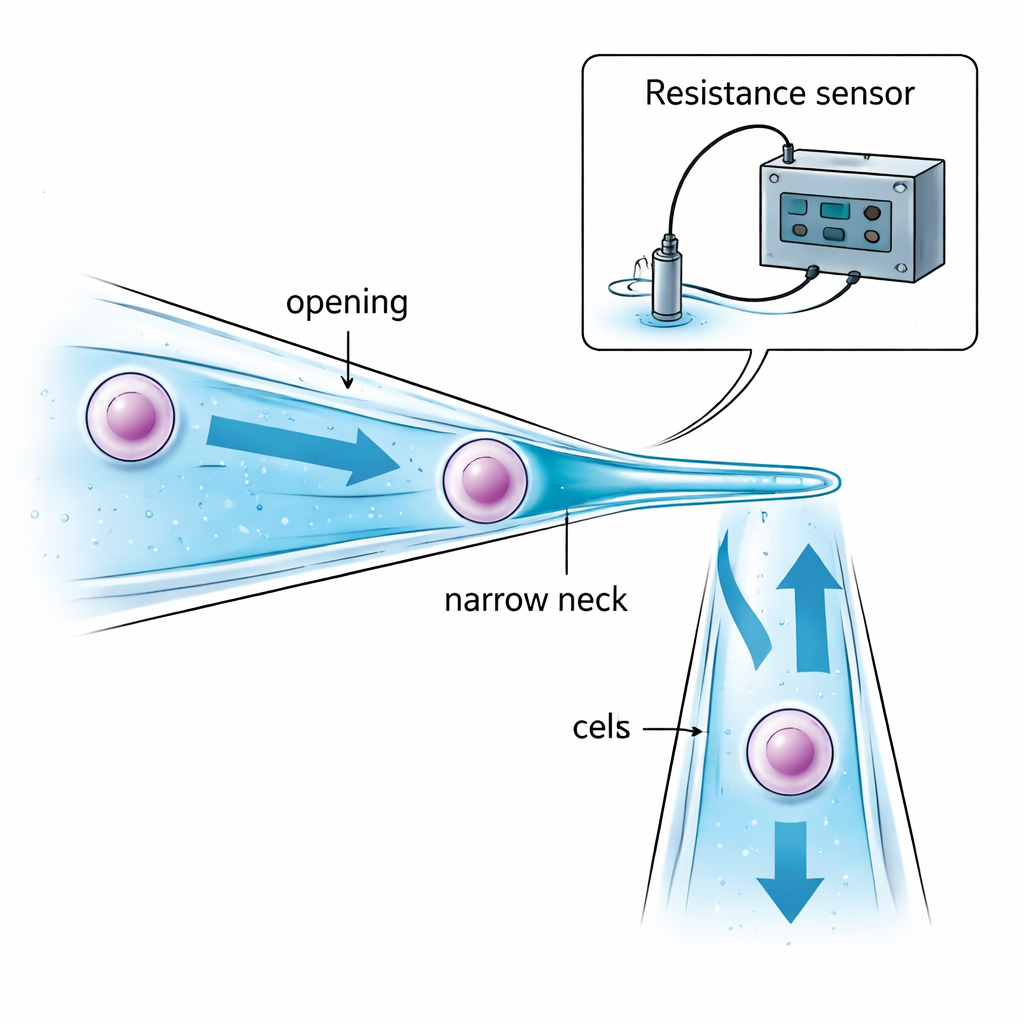
Die Autoren gehen das Problem an, indem sie die Mikropipette selbst neu gestalten. Anstelle eines durchgehend gleich großen Glasrohres fertigen sie eine Mikropipette mit engem Hals. Die Öffnung ist etwas größer als die Zielzelle, sodass die Zelle hineingezogen werden kann. Weiter innen verjüngt sich das Rohr zu einem ‚Hals‘, der kleiner ist als die Zelle. Wenn die Saugkraft die Zelle in Richtung dieser Verengung zieht, wird die Zelle dort gestoppt und im Rohr gehalten — statt am Spitzenende zu hängen und zwischen Tröpfchen Öl oder Luft ausgesetzt zu sein. Die sorgfältige Wahl von Öffnungsdurchmesser, Halsdurchmesser und Abstand dazwischen stellt sicher, dass die Zelle sicher erfasst wird, ohne zu stark gequetscht zu werden, und dass nur eine geringe Flüssigkeitsmenge von einem Tropfen zum anderen mittransportiert wird, was Kontamination reduziert.
Anstatt zu sehen: auf elektrische Signale hören
Ohne Mikroskop muss der Roboter trotzdem drei Dinge wissen: wann die Glasspitze nahe genug am Schalenboden ist, wann die Zelle am Hals erfolgreich erfasst wurde und wann sie vollständig im neuen Tropfen freigegeben ist. Das Team löst dies, indem es winzige Änderungen des elektrischen Widerstands in der Flüssigkeit innerhalb und um die Mikropipette überwacht. Wenn sich die schräg gestellte Pipette dem Schalenboden nähert, wird die Flüssigkeitslücke kleiner und der elektrische Widerstand steigt auf vorhersehbare Weise an, was kurz vor dem Kontakt eine sichere Landung signalisiert. Wenn eine Zelle den engen Hals blockiert, verengt sich der elektrische Leitungsweg durch die Flüssigkeit und der Widerstand springt plötzlich an; wird die Zelle herausgedrückt, fällt der Widerstand ebenso scharf ab. Mathematische Modelle dieser ‚Spalt‘-, ‚Aspiration‘- und ‚Injektions‘-Widerstände erlauben es einem Computer, diese Signale in Echtzeit zu interpretieren und zu entscheiden, wann die Saug- oder Drucksteuerung gestoppt werden soll — ganz ohne visuelles Feedback.
Prüfung des Roboters
Um zu testen, ob dieser Ansatz in der Praxis funktioniert, bauten die Forschenden ein komplettes Robotersystem, das Bewegungssteuerung, Druckregelung, Widerstandsmessung und einen Host-Computer kombiniert. Sie prüften es an kleinen Krebszellen (HeLa-Zellen, etwa 10 Mikrometer Durchmesser) und deutlich größeren Schweineeizellen (rund 150 Mikrometer). Das System konnte Landung, Erfassung und Freigabe zuverlässig allein aus Widerstandssignalen über einen weiten Bereich von Pipettengrößen erkennen. In direkten Vergleichen bewegte der Roboter HeLa-Zellen mit einer Erfolgsrate von 90 Prozent — besser als eine frühere bildbasierte Automatik — und transportierte Schweineeier mit einer Erfolgsrate von 95 Prozent, höher als eine standardmäßige mikroskopgestützte Methode. Die Einsatzzeiten pro Zelle waren ähnlich oder kürzer als bei menschlicher Steuerung, vor allem weil der enge Hals die Notwendigkeit wiederholter Feineinstellung der Saugkraft zur Positionierung der Zelle reduziert.
Zellen schonend behandeln und hochskalieren
Jeder robotische Helfer im Biolabor muss vermeiden, die bearbeiteten Zellen zu schädigen. Nach dem Transport mit dem neuen System wurden sowohl HeLa- als auch Schweineeizellen einen Tag lang kultiviert und mit einem Farbstoff angefärbt, der nur in lebenden Zellen aufleuchtet. Die Überlebensraten der neuen Methode entsprachen denen traditioneller mikroskopgeführter Transfers oder kamen ihnen sehr nahe, was darauf hinweist, dass die sanfte mechanische Quetschung am engen Hals die Zellvitalität bei korrekt gesetzten Schwellenwerten nicht merklich reduziert. Die Autoren schlagen vor, dass dieselbe widstandsbasierten Sensorik und Druckregelung in kompakte mikrofluidische Chips integriert werden kann. Das würde viele Kanäle erlauben, die parallel arbeiten, und so hochdurchsatzfähige, vollständig geschlossene Zellhandhabungssysteme ermöglichen — geeignet für automatisierte Reproduktionsmedizin, Zelltherapien und Langzeitkultivierungsgeräte, in die Mikroskope nur schwer passen.
Was das für die zukünftige Zellarbeit bedeutet
Für Nicht-Spezialisten ist die Kernbotschaft: Das Bewegen einzelner Zellen muss nicht länger davon abhängen, dass eine Person durch ein Mikroskop zusieht. Durch die gezielte Formung eines Glasrohres und das ‚Zuhören‘, wie Elektrizität durch die umgebende Flüssigkeit fließt, kann ein Roboter spüren, wann er gelandet ist, eine Zelle gepackt hat und sie wieder freigibt — alles im Dunkeln und an engen Orten. Das macht die Gestaltung geschlossener, selbstlaufender Zellkultursysteme praktikabler, schützt empfindliche Proben, vereinfacht klinische Abläufe und bringt laborqualitative Zellmanipulation näher an automatisierte, fabrikähnliche Abläufe.
Zitation: Zhao, Q., Liu, M., Zhu, R. et al. Robotic cell transportation system based on micropipette resistance modeling. Microsyst Nanoeng 12, 65 (2026). https://doi.org/10.1038/s41378-026-01193-5
Schlüsselwörter: Zellmanipulation, Mikropipette, Robotik, Mikrofluidik, Automatisierung