Clear Sky Science · de
Strategien zur Kontrolle der zellulären räumlichen Organisation in mikrophysiologischen Systemen
Winzige Gewebe im Labor aufbauen
Unsere Organe funktionieren so gut, weil ihre Zellen nicht zufällig verteilt sind – sie sind räumlich sorgfältig angeordnet. Dieser Artikel untersucht, wie Forschende lernen, diese komplexe Ordnung innerhalb von „Organen auf Chips“ und anderen miniaturisierten, im Labor gezüchteten Geweben nachzubilden. Indem sie steuern, wo verschiedene Zellen sitzen und wie sie interagieren, können Wissenschaftler realistischere Modelle von Herz, Gehirn, Darm, Blutgefäßen und sogar von Mensch‑Mikroben‑Ökosystemen erzeugen. Diese fortgeschrittenen Systeme versprechen sicherere Medikamententests, weniger Tierversuche und bessere Werkzeuge zur Erforschung von Krankheiten und zur Entwicklung personalisierter Therapien.
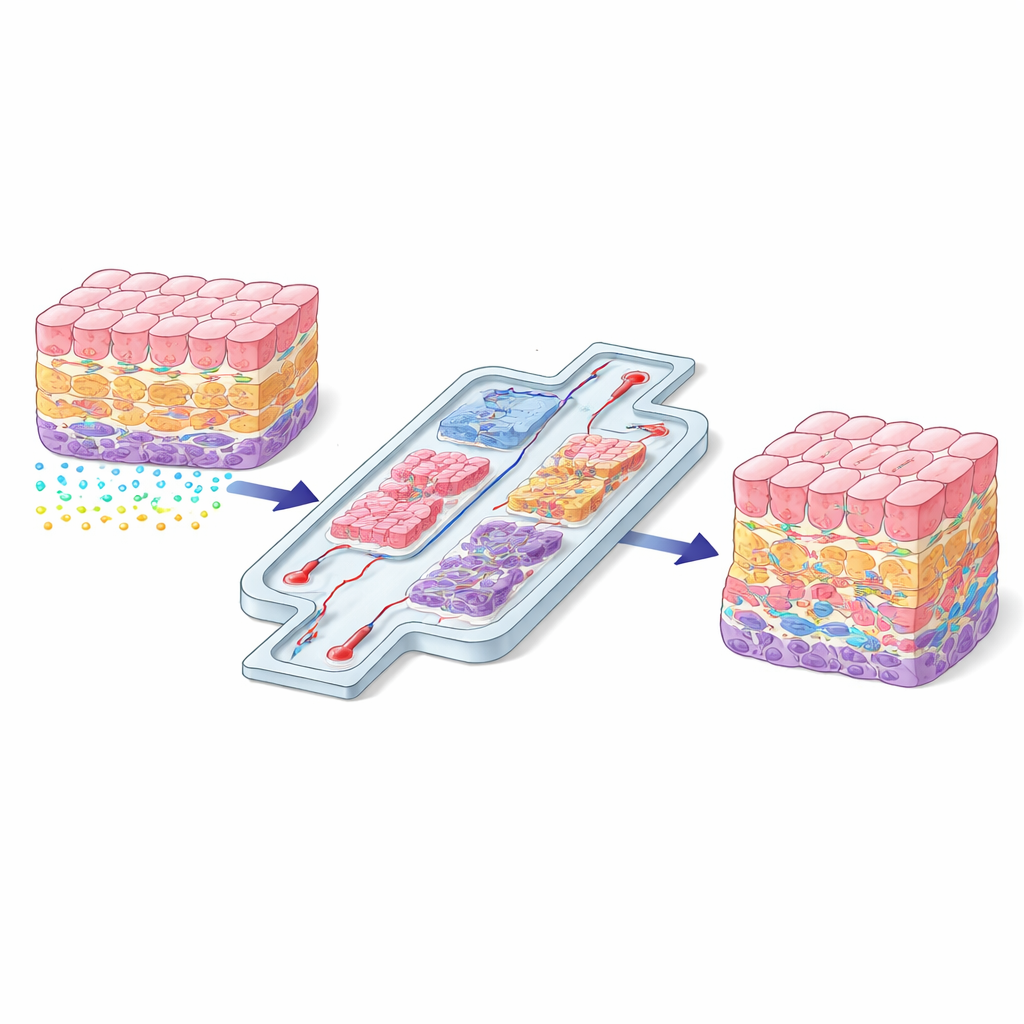
Warum die Zellposition wichtig ist
Im Körper lebt jede Zelle in einer bestimmten Nachbarschaft mit einer eigenen Mischung aus Stützstrukturen, chemischen Signalen und physikalischen Kräften. Eine Leberzelle in der Nähe eines Blutgefäßes erhält andere Hinweise als eine Zelle tief im Organinneren. Diese Unterschiede in der Lage bestimmen, wie Zellen wachsen, wozu sie sich entwickeln und wie sie auf Verletzung oder Medikamente reagieren. Wenn Forschende Zellen auf flachen Plastikschalen kultivieren, geht dieses räumliche „Gespräch“ größtenteils verloren, und Zellen verhalten sich oft unnatürlich. Der Artikel argumentiert, dass die Nachbildung realistischer räumlicher Organisation kein optionales Upgrade ist, sondern eine Grundvoraussetzung, damit im Labor gezüchtete Gewebe echte Organe nachahmen können.
Zwei Hauptwege, Zellen anzuordnen
Die Autoren fassen aktuelle Strategien in zwei große Familien: direkte und indirekte Kontrolle. Direkte Methoden platzieren Zellen oder Kompartimente physisch genau dort, wo sie gebraucht werden. Beispiele sind 3D‑Bioprinting, das Schichten aus Zellen und weichen Gelen wie ein biologischer 3D‑Drucker ablegt; mikrofluidische Chips, die Gewebe in verbundene Kammern und Kanäle formen; und physikalische Fangmethoden, die Zellen mittels Licht, Schall, Magneten oder elektrischen Feldern in Position bringen. Diese Ansätze sind besonders vorteilhaft, wenn präzise Geometrie entscheidend ist – etwa beim Nachbilden einer Blut‑Hirn‑Schranke, einer geschichteten Gefäßwand oder des Flusswegs vom Darm zur Leber.
Zellen ihre Umgebung lesen lassen
Indirekte Methoden gestalten stattdessen die Umgebung um und überlassen den Rest den Zellen. Hier stimmen Forschende die „Landschaft“ ab, die Zellen wahrnehmen: die Zusammensetzung des umgebenden Gels, die Steifigkeit und Textur von Oberflächen sowie Gradienten gelöster Stoffe wie Wachstumsfaktoren oder Medikamente. Sorgsam platzierte Stützmoleküle können bestimmte Zelltypen dazu bringen, sich in definierten Regionen anzusiedeln. Intelligente Hydrogele, die sich beim Umbau durch Zellen erweichen oder Signale freisetzen, fördern selbstorganisierte Strukturen wie Gefäßnetzwerke oder darmähnliche Krypten und Zotten. Mikrofluidische Vorrichtungen können stabile chemische Gradienten erzeugen, die Stammzellen entlang eines Kanals unterschiedliche Identitäten annehmen lassen oder Krebs‑ und Immunzellen in getrennte Zonen wandern lassen, wodurch sichtbar wird, wie sich Krankheiten ausbreiten.
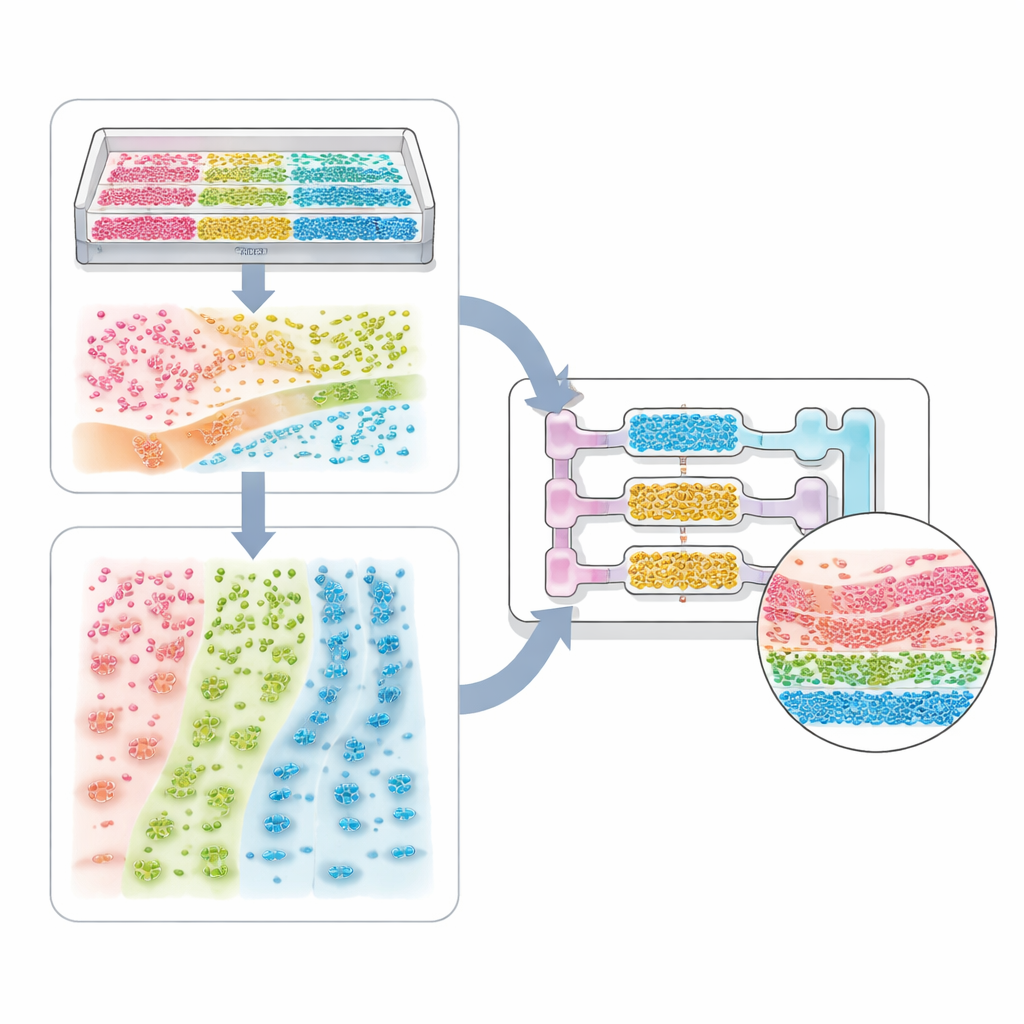
Von Einzellersystemen bis zu Ganzkörpermodellen
Die Übersichtsarbeit führt durch ein Spektrum von Anwendungen. Am einfachsten sind Systeme mit nur einem Zelltyp, bei denen gemusterte Rillen oder Steifigkeitsgradienten Herzmuskelzellen synchron schlagen oder Nervenzellen ausgerichtete Fasern ausbilden lassen. Komplexere Gewebemodelle mischen mehrere Zelltypen – etwa Tumorzellen, Stütz‑/Stroma‑Zellen und Gefäßzellen – zu Sphären und Organoiden mit inneren Kernen und Schalen. Mikrokanal‑Chips und Bioprinting fügen dann Begrenzungen und Fluss hinzu, wodurch Lungenbläschen, Nierenfilter, Leberzonen und Mehrorgan‑Schaltkreise nachgebildet werden können, die verfolgen, wie ein Medikament aufgenommen, umgewandelt und eliminiert wird. Dieselben Konzepte gelten für Wirts‑Mikroben‑Systeme, bei denen die räumliche Anordnung von Bakterien entlang der Darmwand oder über eine Schleimschicht bestimmt, ob sie schützen oder Krankheit verursachen.
Überprüfen, ob Muster echt sind
Da diese Systeme immer komplexer werden, brauchen Forschende verlässliche Methoden, um zu bestätigen, dass Zellen dort landen, wo sie sollen, und sich wie beabsichtigt verhalten. Der Artikel hebt Bildgebungsverfahren hervor, die lebende Zellen über die Zeit beobachten können, sowie fortgeschrittene Färbe‑ und Sequenzierungstechniken, die kartieren, welche Gene, Proteine und Metabolite an jedem Ort vorkommen. In Chips eingebaute Sensoren können Sauerstoff, Nährstoffe, Säuren und mechanische Kräfte verfolgen und lokale Bedingungen mit Zellantworten verknüpfen. Zusammen helfen diese Werkzeuge Forschenden zu verifizieren, dass ein Design nicht nur optisch überzeugend, sondern auch funktional treu zum echten Gewebe ist.
Wohin diese Arbeit führt
Die Autoren kommen zu dem Schluss, dass die leistungsfähigsten Systeme direkte und indirekte Strategien kombinieren werden: Chips und Bioprinter, die das Gesamtlayout vorgeben, ergänzt durch einstellbare Gele, Oberflächenstrukturen und Gradienten, die es Geweben erlauben, im Laufe der Zeit zu reifen und sich umzubauen. Sie benennen auch praktische Hürden – etwa die Skalierung der Fertigung, die Reduzierung von Variabilität zwischen Labors und ethische Fragen im Umgang mit komplexen menschlichen Gewebemodellen. Dennoch ist die Botschaft klar: Die Beherrschung räumlicher Organisation ist entscheidend, um mikrophysiologische Systeme in vertrauenswürdige Stellvertreter für menschliche Organe zu verwandeln und neue Möglichkeiten zur Erforschung der Entwicklung, zur Testung von Therapien und zur individuellen Medizin zu eröffnen.
Zitation: Truong, H.D., Ge, Z., Chng, E. et al. Strategies to control cellular spatial organization in microphysiological systems. Microsyst Nanoeng 12, 85 (2026). https://doi.org/10.1038/s41378-025-01141-9
Schlüsselwörter: organ-on-a-chip, zellräumliche Organisation, 3D-Bioprinting, mikrofluidische Gewebemodelle, mikrophysiologische Systeme