Clear Sky Science · de
Ein-Einzelgefäß-CRISPR-Punkt‑of‑Care‑System für die schnelle, spezifische und empfindliche Nachweis von HPV16 ohne Vorverstärkung
Warum das Erkennen eines Virustyps wirklich wichtig ist
Gebärmutterhalskrebs steht häufig in Verbindung mit Infektionen durch Humane Papillomaviren (HPV), aber nicht alle HPV‑Typen tragen dasselbe Risiko. Ärztinnen und Ärzte benötigen daher Tests, die diese sehr ähnlichen Viren zuverlässig unterscheiden können, insbesondere den Hochrisikotyp HPV16. Die Herausforderung besteht darin, dass heutige Gentests nahe Verwandte gelegentlich verwechseln, was zu Fehlalarmen oder übersehenen Fällen führen kann. Diese Studie stellt eine neue Testmethode vor, die sowohl die Genauigkeit als auch die Praktikabilität deutlich verbessert und darauf abzielt, präzise HPV‑Subtypisierung in Kliniken und an Point‑of‑Care‑Stellen zu bringen.
Ein intelligentes molekulares Schloss und Schlüssel
Die Forschenden entwickelten einen Ein‑Gefäß‑Test, den sie CASTSA nennen, der zwei leistungsfähige Konzepte kombiniert: die Präzision von CRISPR, einem aus Bakterien adaptierten Genzielsystem, und die Signalverstärkung durch PCR, die Standardmethode zur Vervielfältigung von DNA. In CASTSA wird das CRISPR‑Protein Cas12a durch eine kurze RNA‑„Schlüssel“ zur HPV16‑Gensequenz geführt. Findet es die exakte Übereinstimmung plus ein benachbartes kurzes Erkennungsmuster, schneidet Cas12a die virale DNA an einer vorhersehbaren Stelle. Dieser Schnitt erzeugt ein charakteristisches offenes Ende an einem DNA‑Strang, das als eindeutiger Startpunkt für die Amplifikation dient. Andere HPV‑Typen, selbst mit sehr ähnlichen Sequenzen, werden entweder nicht geschnitten oder erzeugen nicht den richtigen Startpunkt und werden daher nicht amplifiziert.
Aus einem winzigen Schnitt ein starkes Signal machen
Um den CRISPR‑Schnitt in ein nachweisbares Signal zu verwandeln, entwarfen die Autoren ein spezielles DNA‑Primer, das terminal‑spezifische Primer genannt wird. Dieser Primer bindet nur korrekt an den durch Cas12a erzeugten Strang, klappt dann wie eine Haarnadel zurück und hilft, eine stabile Vorlage für die PCR aufzubauen. Zusätzliche „universelle“ Primersequenzen heften sich anschließend an und treiben eine konventionelle Echtzeit‑PCR‑Reaktion an. Entscheidend ist, dass eine Amplifikation nur stattfindet, wenn Cas12a zuvor seine Arbeit getan hat und der Primer korrekt faltet — wodurch zwei Kontrollschichten entstehen. Diese Architektur verringert deutlich die Wahrscheinlichkeit, dass partiell passende, nicht‑zielgerichtete DNA versehentlich amplifiziert wird, und behebt damit eine häufige Schwäche früherer CRISPR‑basierter Tests, die auf einer separaten Vorverstärkung beruhten.
Alles in einem Gefäß, mit weniger Fehlern
Ein wichtiger praktischer Fortschritt besteht darin, dass CRISPR‑Schnitt und PCR‑Amplifikation gemeinsam im gleichen versiegelten Röhrchen ablaufen, sodass das Öffnen der Röhrchen zwischen den Schritten entfällt — eine wesentliche Kontaminationsquelle in vielen Laborabläufen. Die Autorinnen und Autoren optimierten sorgfältig die Reaktionsbedingungen, insbesondere den Magnesiumgehalt, sodass sowohl Cas12a als auch das DNA‑kopierende Enzym gut funktionieren, ohne unerwünschte Reaktionen zu begünstigen. Sie zeigten, dass ihr Ein‑Gefäß‑Ansatz HPV16 zuverlässig von mehreren anderen Hochrisiko‑Typen, darunter HPV18, 33, 45 und 52, unterscheiden kann, obwohl diese Viren hochkonservierte genetische Regionen teilen. Im Vergleich zu Standard‑Echtzeit‑PCR allein oder zu CRISPR‑Tests, die zuerst DNA amplifizieren und dann CRISPR‑Detektion durchführen, erzeugte CASTSA deutlich weniger irreführende Signale von Off‑Target‑HPV‑Typen.
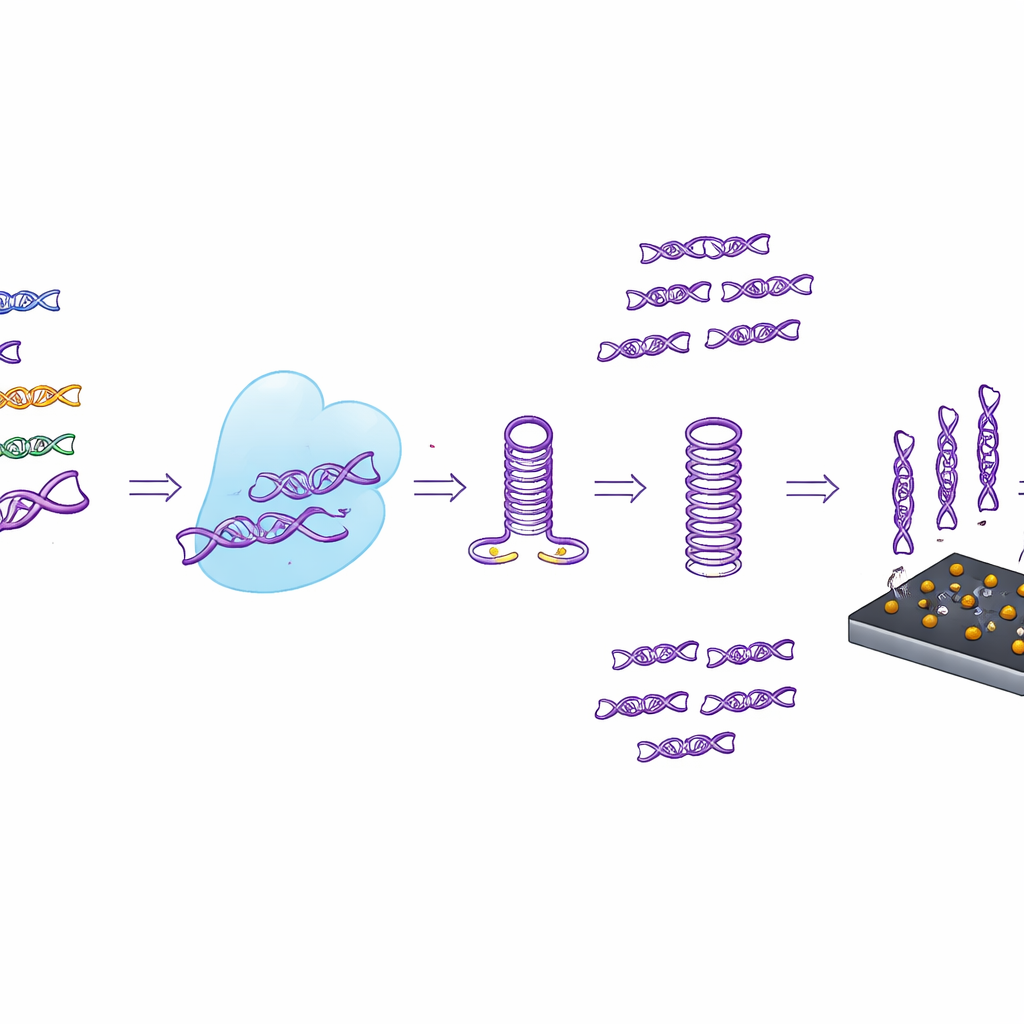
Vom Reagenzglas zum tragbaren Sensor
Statt sich nur auf fluoreszenzbasierte Auslesungen zu stützen, koppelte das Team CASTSA auch an einen kompakten elektrochemischen Sensor aus laserinduzierter Graphen. Diese poröse, hochleitfähige Kohlenstoffoberfläche ist mit Goldnanopartikeln versehen, die Fangstränge tragen, die nur die CASTSA‑Amplifikationsprodukte von HPV16 binden sollen. Wenn diese Produkte haften, verschiebt sich der elektrische Strom durch den Sensor messbar. Mit einem Vier‑Elektroden‑Array — drei Messstellen und einer eingebauten Hintergrundkontrolle — kann das Gerät Rauschen durch unspezifisches Haften herausrechnen. In Tests erkannte das integrierte System bereits 18 Kopien des HPV16‑Ziels pro Reaktion, übertraf damit die Sensitivität der reinen Fluoreszenz und zeigte eine sehr gute Wiederholbarkeit.
Wie das die HPV‑Testung verändern könnte
Um die Methode in der Praxis zu prüfen, testete das Team 20 klinische Proben, von denen bekannt war, dass sie HPV16 enthalten, sowie 10 Proben von gesunden Spendern. CASTSA — sowohl in der Fluoreszenzversion als auch in Verbindung mit dem Graphen‑basierten Sensor — stimmte vollständig mit den standardmäßigen Krankenhaus‑PCR‑Tests überein. Gleichzeitig zeigte es eine überlegene Fähigkeit, andere Hochrisiko‑HPV‑Typen zu ignorieren, die häufig zu Verwirrung führen. Für Patientinnen und Patienten könnte das weniger unklare Ergebnisse und sicherere Entscheidungen über Nachverfolgung und Behandlung bedeuten. Generell bietet die CASTSA‑Strategie — zuerst CRISPR‑Erkennung, dann Amplifikation, alles in einem versiegelten Röhrchen — einen Bauplan für hochspezifische, kontaminationsarme Gentests, die auf viele Erreger und Mutationen anpassbar sind, besonders in Umgebungen, die schnelle und zuverlässige Antworten erfordern.
Zitation: Chen, Y., Chen, Y., Zhang, C. et al. One-pot CRISPR-based point of care platform for rapid, specific and sensitive detection of HPV 16 without pre-amplification. Microsyst Nanoeng 12, 81 (2026). https://doi.org/10.1038/s41378-025-01130-y
Schlüsselwörter: HPV16-Nachweis, CRISPR-Diagnostik, PCR-basierte Tests, elektrochemischer Biosensor, Punkt‑of‑Care‑Assay