Clear Sky Science · de
Interferometrische Image-Scanning-Mikroskopie für kennzeichnungsfreies Imaging mit 120-nm-lateralem Auflösungsvermögen in lebenden Zellen
Leben in Zellen ohne zusätzliche Farbstoffe sehen
Die moderne Biologie stützt sich häufig auf leuchtende fluoreszierende Marker, um die verborgene Architektur innerhalb von Zellen sichtbar zu machen. Diese Marker können Zellen jedoch belasten, ihr Verhalten verändern und sind manchmal in empfindlichen oder schwer zu manipulierenden Proben gar nicht einsetzbar. Dieser Artikel stellt eine neue Methode vor, mit der man das Geschehen in lebenden Zellen hochauflösend beobachten kann — ohne Farbstoffe oder genetische Marker — und so schonendere, längere und naturgetreuere Beobachtungen ermöglicht, wie Zellen tatsächlich funktionieren.
Zellen betrachten anhand ihrer Lichtstreuung
Die Methode baut auf einer Familie von Techniken auf, die nicht auf Fluoreszenz beruhen, sondern darauf, wie winzige Strukturen Licht streuen. Eine dieser Methoden, die interferometrische Streumikroskopie (iSCAT), mischt das von einem nanoskaligen Objekt gestreute Licht mit einer Referenzreflexion von einer Glasfläche. Das resultierende Interferenzmuster ist extrem empfindlich gegenüber sehr kleinen Partikeln wie Proteinen, Viren oder Vesikeln. iSCAT funktionierte bisher am besten bei einfachen, sauberen Proben wie isolierten Partikeln auf Glas. Die Anwendung tief im Inneren lebender Zellen war jedoch schwierig, weil Zellen dicht gepackt und unübersichtlich sind: zahlreiche überlagerte Streuereignisse erzeugen einen körnigen Hintergrund, der feine Details verschleiert.
Zwei Ideen kombinieren für schärferes, schonenderes Imaging
Um diese Begrenzungen zu überwinden, kombinierten die Autorinnen und Autoren iSCAT mit einer leistungsfähigen Bildgebungsstrategie namens Image Scanning Microscopy (ISM). Bei ISM wird die Probe Punkt für Punkt mit einem fokussierten Strahl abgescannt, und statt eines einzelnen Detektors zeichnet ein Detektorarray viele leicht verschobene Blickwinkel auf jeden Punkt auf. Durch geschicktes Neuausrichten und Kombinieren dieser Ansichten lässt sich das endgültige Bild schärfen, ohne wertvolle Photonen zu verschwenden. Die neue Technik — interferometrische Image-Scanning-Mikroskopie, kurz iISM — passt dieses Prinzip an die komplexeren, phasensensitiven Signale der interferometrischen Streuung an. Das Mikroskop verwendet einen blauen Laser, spezielle Optiken zur symmetrischen Polarisation des Lichts und eine empfindliche Kamera, die für jede Scanposition das gestreute und reflektierte Licht aufzeichnet. Ein maßgeschneiderter Rechenworkflow weist dann die Pixelinformationen in einer Weise neu zu, die der Wellencharakter des Signals respektiert, und liefert Bilder mit etwa 120 Nanometer lateraler Auflösung — ungefähr doppelt so fein wie herkömmliche, beugungsbegrenzte Optiken.
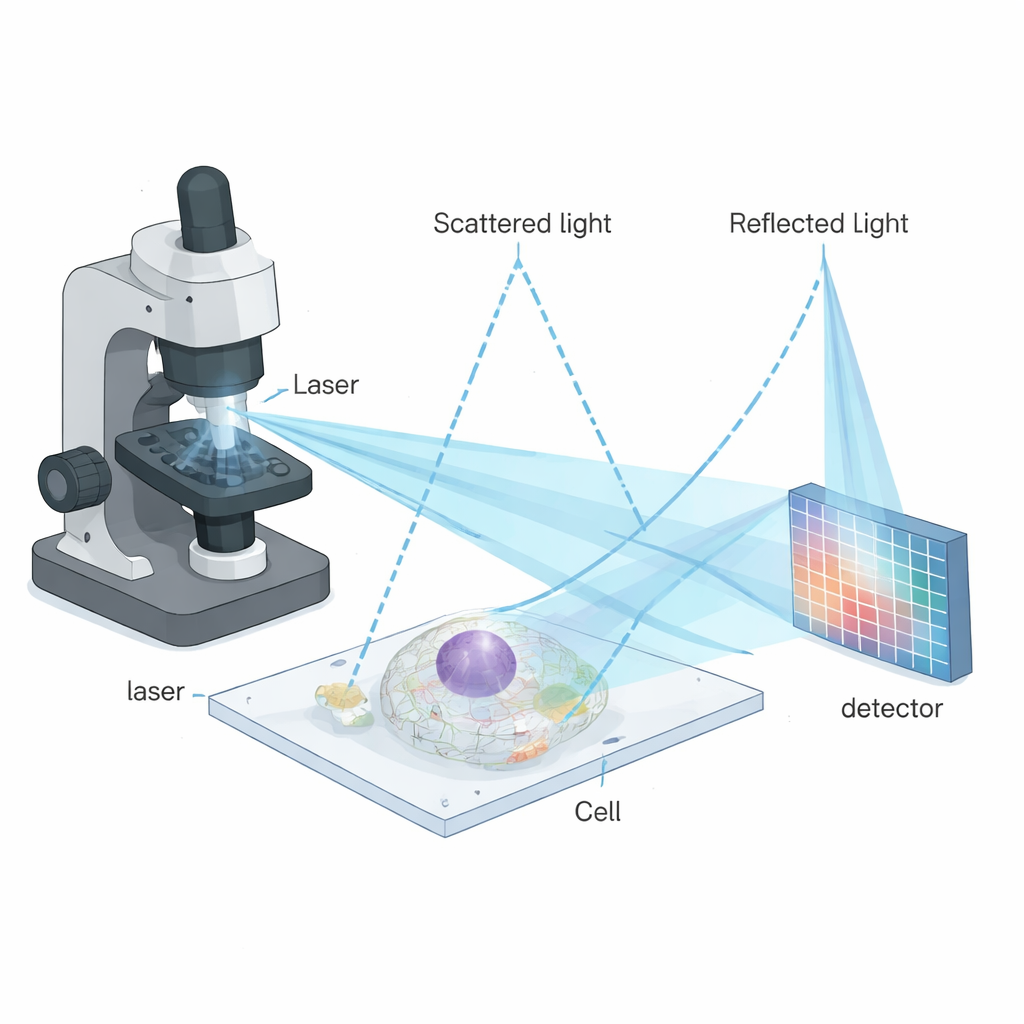
Intelligente Algorithmen verwandeln rauschartige Muster in klare Bilder
Weil interferometrische Signale sowohl Helligkeits- als auch Phaseninformation tragen, reichen die üblichen Verarbeitungsansätze aus der Fluoreszenzbildgebung nicht aus. Die Autoren entwickelten ein adaptives Pixel-Reassignment-(APR-)Verfahren, das auf kohärentes Licht zugeschnitten ist. Zunächst wandeln sie jedes kleine interferometrische Muster in eine „radiale Varianz“-Karte um, die Symmetriezentren hervorhebt, ohne zwischen positivem oder negativem Signal zu unterscheiden. Dieser Schritt konvertiert komplizierte Interferenzfransen effektiv in Bilder, die sich stärker wie konventionelle Intensitätsabbildungen verhalten. Anschließend bestimmen sie mit quelloffener Software, wie stark das Bild jedes Detektorpixels relativ zum Zentrum verschoben ist, und rücken diese entsprechend wieder ein, bevor sie sie aufsummieren. Diese verfeinerte Ausrichtung konzentriert das nützliche Signal und mittelt das Rauschen herunter, wodurch das Kontrast-zu-Rausch-Verhältnis im Vergleich zu einem eng abgeblendeten konfokalen iSCAT-Bild bei gleicher Lichtstärke etwa um den Faktor vier verbessert wird.
Organelle und Zytoskelette in Aktion beobachten
Mit diesen technischen Verbesserungen testete das Team iISM an lebenden COS-7-Zellen, um die praktische Leistungsfähigkeit zu prüfen. Bei sehr geringer Beleuchtungsstärke — etwa zehnmal schwächer pro Fokuspunkt als bei konventionellen konfokalen Mikroskopen üblich — konnten sie wichtige Organellen klar unterscheiden: das endoplasmatische Retikulum, Mitochondrien, Vesikel, das Aktin-Zytoskelett, die Plasmamembran und dünne Vorwärtsstrukturen, sogenannte Lamellipodien. Da der interferometrische Kontrast empfindlich von der vertikalen Position abhängt, konnten ähnliche Organellen mit positiver oder negativer Kontrastgebung erscheinen und subtile Höhenunterschiede von nur wenigen hundert Nanometern sichtbar machen. Durch Zeitrafferaufnahmen verfolgten sie Vesikelbewegungen und die Umgestaltung von Retikulum-Tubuli über viele Minuten hinweg, ohne offensichtliche Photodamage und ohne Hinweise darauf, dass die Bildgebung das Verhalten der Zellen störte.
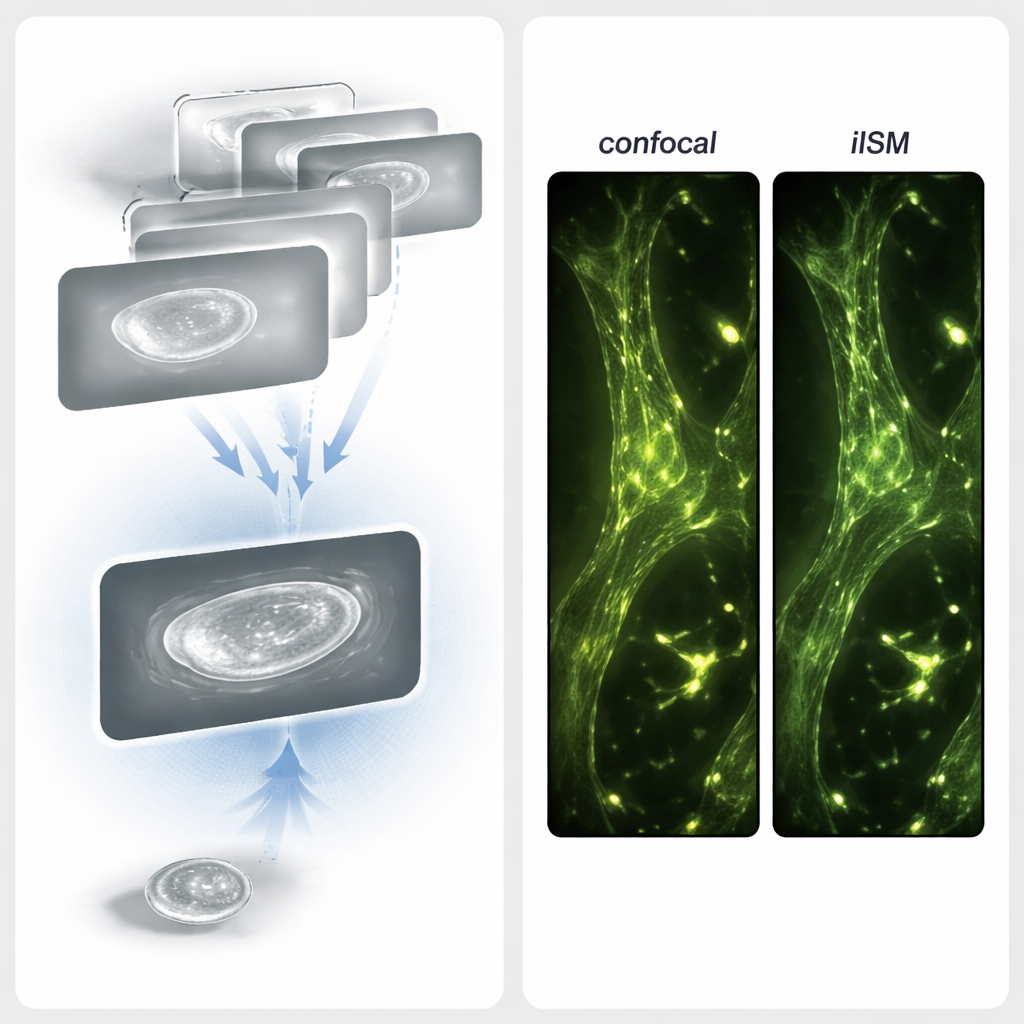
Kennzeichnungsfreie Ansichten mit fluoreszenten Karten abgleichen
Um zu prüfen, ob die kennzeichnungsfreien Bilder tatsächlich reale zelluläre Strukturen wiedergeben, führten die Forschenden außerdem kombinierte iISM- und Fluoreszenz-ISM-Messungen an fixierten Zellen durch. Sie färbten das Aktin-Zytoskelett mit einem roten Fluoreszenzfarbstoff und nahmen superaufgelöste Fluoreszenzbilder parallel zu den kennzeichnungsfreien iISM-Bildern derselben Region auf. Beim Überlagern stimmten helle Aktinfilamente im Fluoreszenzkanal eng mit filamentösen Strukturen in den iISM-Bildern überein. In einigen Bereichen zeigte iISM sogar zusätzliche Streudetails — etwa Längenvariationen entlang von Filamenten oder benachbarte ungekennzeichnete Strukturen wie Fokaladhäsionen —, die im Fluoreszenzkanal unsichtbar blieben. Zusammen zeigen diese Ergebnisse, dass iISM bekannte Strukturen bestätigen und zusätzliche Informationen über ungekennzeichnete Umgebungen liefern kann.
Ein neues Fenster in Zellen, mit weniger Störung
Für Nichtfachleute ist die zentrale Botschaft, dass iISM eine Möglichkeit bietet, feine Details in lebenden Zellen zu sehen, ohne sie künstlich zum Leuchten zu bringen. Es vereint die Empfindlichkeit der interferometrischen Streuung mit der Schärfung durch Image Scanning und erreicht ungefähr 120 Nanometer Auflösung bei deutlich geringerer Lichtbelastung als viele bestehende Mikroskope. Da die Methode aus Komponenten aufgebaut ist, die bereits in fortgeschrittenen konfokalen Systemen verbreitet sind, könnte sie prinzipiell an kommerzielle Instrumente angebaut werden. Künftig könnte iISM mit traditioneller Fluoreszenz, schnellen Detektoren oder sogar maschinellen Lernverfahren für „virtuelle Färbungen“ kombiniert werden, um Infektionen, Frachttransport oder Umorganisationen des Zytoskeletts unter Bedingungen zu verfolgen, die näher am natürlichen, ungestörten Zustand der Zellen liegen.
Zitation: Küppers, M., Moerner, W.E. Interferometric Image Scanning Microscopy for label-free imaging at 120 nm lateral resolution inside live cells. Light Sci Appl 15, 129 (2026). https://doi.org/10.1038/s41377-026-02210-y
Schlüsselwörter: kennzeichnungsfreies Imaging, Lebendzellmikroskopie, interferometrische Streuung, Superauflösung, zelluläre Organellen