Clear Sky Science · de
Synthetische Letalität von MCL‑1‑Hemmung und CAR‑T‑Therapie bei aggressivem B‑Zell‑Lymphom
Warum das für die Krebsbehandlung wichtig ist
Aggressive B‑Zell‑Lymphome sind schnell wachsende Bluttumoren, die nach einer Behandlung häufig wieder auftreten. Selbst mächtige neue Verfahren wie die CAR‑T‑Zelltherapie, die die körpereigenen Immunzellen eines Patienten so umprogrammiert, dass sie Krebs angreifen, versagen im Laufe der Zeit bei etwa der Hälfte der Patienten. Diese Studie untersucht einen Weg, diese Schwäche in eine Stärke zu verwandeln: ein Medikament zu verwenden, das ein zentrales Überlebensprotein in Lymphomzellen anvisiert, um sowohl Tumoren zu töten als auch die verbleibenden Zellen für CAR‑T‑Zellen leichter angreifbar zu machen.
Das Problem hartnäckiger Lymphomzellen
Aggressive B‑Zell‑Lymphome werden häufig durch übermäßige Aktivität des Gens MYC angetrieben, das die Zellteilung stark beschleunigt und den Zellen zugleich hilft, sich dem Immunsystem zu entziehen. Standardtherapien und selbst CAR‑T‑Behandlungen können kleine Nester von Lymphomzellen zurücklassen, die Medikamente tolerieren und später Rezidive verursachen. Diese „Persister“ und resistenten Zellen leben in einer Tumorumgebung, die von unterdrückenden Immunzellen bevölkert ist und cytotoxische T‑Zellen in Schach hält. Die Autoren fragten, ob die Blockade von MCL‑1, einem Protein, auf das Lymphomzellen angewiesen sind, um nicht in den programmierten Zelltod zu gehen, eine verborgene Schwäche in diesem System offenlegen könnte.
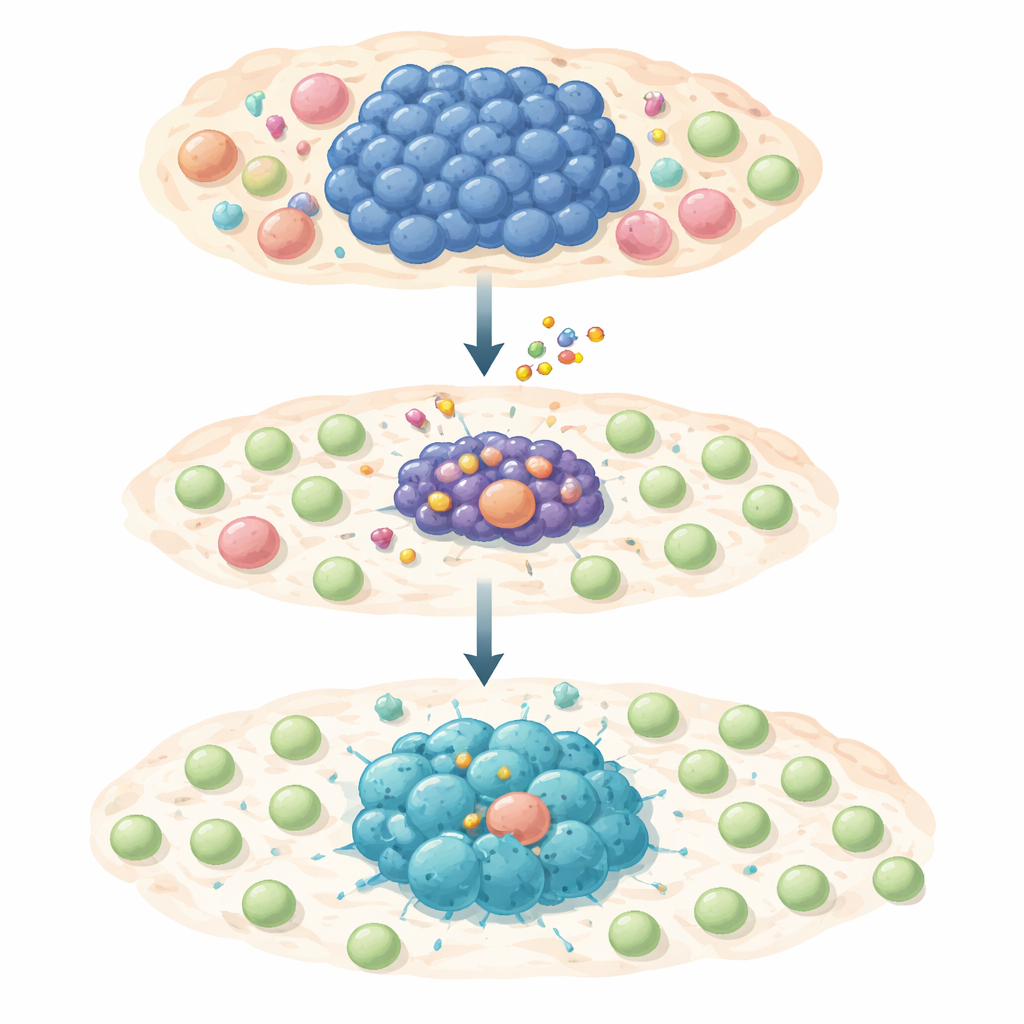
Ein zweistufiger Angriff auf Tumorüberleben und Verstecken
Das Team testete den selektiven MCL‑1‑Blocker S63845 an einem großen Panel humaner Lymphomzelllinien, die von MYC abhängig sind. Die meisten dieser Krebszellen waren hochsensitiv gegenüber dem Wirkstoff und durchliefen programmierten Zelltod, wenn MCL‑1 blockiert wurde. Eine kleine Fraktion überlebte jedoch kurz‑ oder langfristige Exposition und wurde medikamententolerant oder vollständig resistent. Bei näherer Untersuchung dieser Überlebenden fanden die Forschenden reduzierte MYC‑Aktivität, während ein anderes Molekül, STAT1, und der dazugehörige Interferon‑Alarmweg aktiviert waren. Diese Verschiebung schaltete Gene für inflammatorische Signale und Chemokine an—molekulare „Fackeln“, die T‑Zellen in das Tumorareal locken können.
Das immunologische Umfeld reaktivieren
Um zu sehen, wie sich das in einem lebenden Organismus auswirkt, behandelten die Autoren Mäuse mit MYC‑getriebenen Lymphomen mit einer niedrigen Dosis des MCL‑1‑Inhibitors. Das Medikament verringerte die Tumorlast und schonte dabei normale B‑Zellen, doch seine Wirkung ging über eine bloße Volumenreduktion hinaus. Behandelte Tumoren zeigten mehr CD4‑ und CD8‑T‑Zellen, weniger erschöpfte T‑Zellen, weniger regulatorische T‑Zellen und weniger suppressive myeloische Zellen — alles Anzeichen eines immunfreundlicheren Umfelds. Einzelzell‑RNA‑Sequenzierung der Tumor‑ und Umgebungszellen bestätigte, dass die verbliebenen Lymphomzellen geringeres MYC, erhöhtes STAT1 sowie stärkere Interferon‑ und Entzündungssignale aufwiesen, während das umliegende Gewebe mit aktiven T‑ und Natural‑Killer‑Zellen und nicht mit suppressiven Zellen repopuliert wurde.
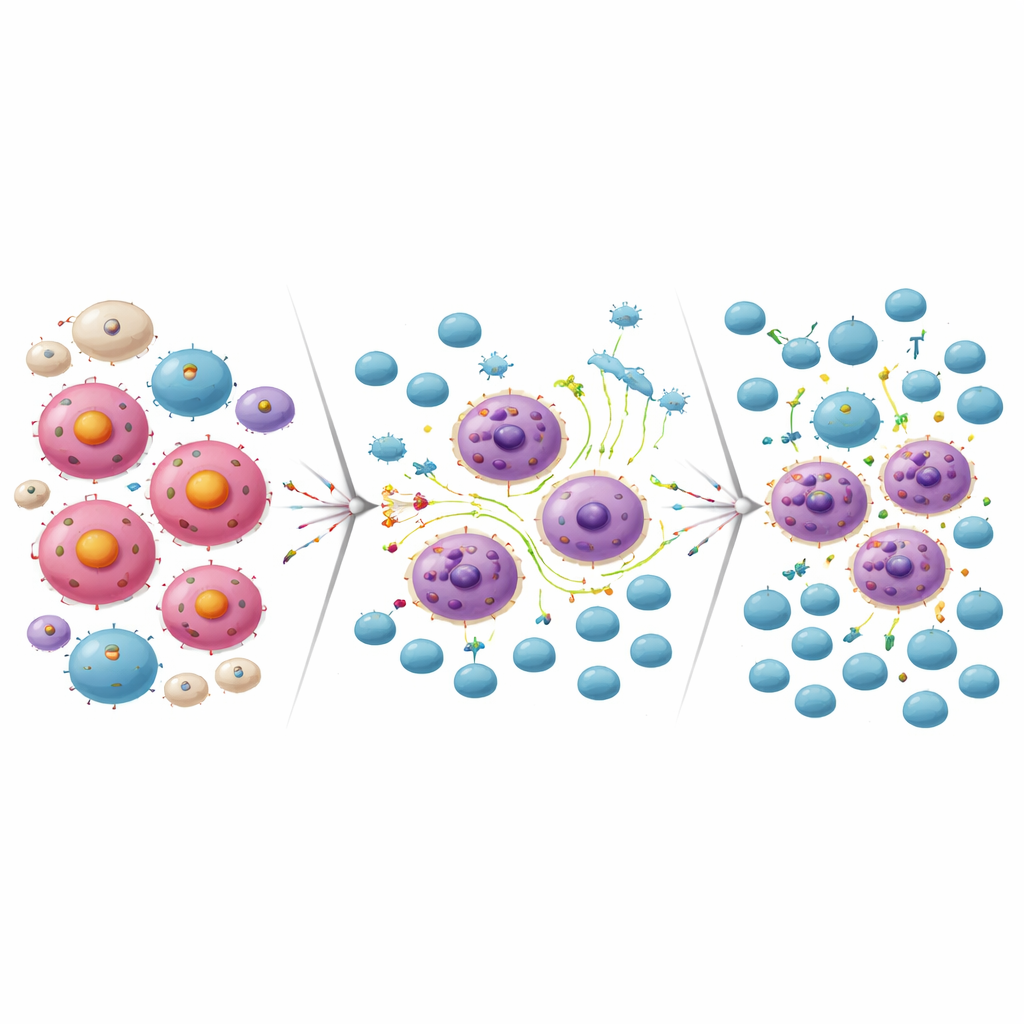
Resistance in eine Chance für CAR‑T‑Zellen verwandeln
Dasselbe inflammatorische Umprogrammieren, das einigen Lymphomzellen half, der MCL‑1‑Blockade zu entgehen, machte sie gleichzeitig anfälliger für immunologische Angriffe. Im Labor töteten CD19‑gerichtete CAR‑T‑Zellen effizient Lymphomzellen, die gegenüber dem MCL‑1‑Wirkstoff resistent geworden waren. Umgekehrt waren Lymphomzellen, die gegen CD19‑CAR‑T‑Therapie resistent geworden waren, hochsensitiv gegenüber dem MCL‑1‑Inhibitor. Kombinierte man in Zellkulturen eine subletale Dosis des MCL‑1‑Wirkstoffs mit CAR‑T‑Zellen, beseitigten die beiden Behandlungen zusammen weit mehr Lymphomzellen als jede für sich. In Mausmodellen führte die Gabe des MCL‑1‑Inhibitors gefolgt von CD19‑CAR‑T‑Zellen zu nahezu vollständiger Tumorbeseitigung und deutlich verlängerter Überlebenszeit im Vergleich zu Einzeltreatments.
Ein Schlag mit kurativer Aussicht
Kurz gesagt, die Studie schlägt eine „One‑Two‑Punch“-Strategie vor. Zuerst reduziert ein MCL‑1‑blockierendes Medikament den Großteil des Lymphoms und zwingt überlebende Krebszellen in einen entzündlichen, hoch sichtbaren Zustand, der T‑Zellen anzieht und Schutzmechanismen abträgt. Anschließend nutzen CD19‑CAR‑T‑Zellen diese neu freigelegte Verwundbarkeit, um die verbleibende Krankheit zu eradizieren. Indem sowohl die interne Überlebensverdrahtung des Tumors als auch dessen schützendes Umfeld angegriffen werden, könnte dieser kombinierte Ansatz Rezidive verringern und aggressive B‑Zell‑Lymphome näher an eine langanhaltende Remission bringen.
Zitation: Gao, J., Zhao, X., Yin, Q. et al. Synthetic lethality of MCL-1 inhibition and CAR-T therapy in aggressive B-cell lymphoma. Leukemia 40, 638–648 (2026). https://doi.org/10.1038/s41375-026-02884-8
Schlüsselwörter: B‑Zell‑Lymphom, CAR‑T‑Therapie, MCL‑1‑Hemmung, Tumormikroumgebung, Arzneimittelresistenz