Clear Sky Science · de
Alnuctamab, ein bivalenter T‑Zell‑Engager, der das B‑Zell‑Reifungsantigen anvisiert, für Patientinnen und Patienten mit rezidiviertem oder refraktärem multiplen Myelom: Ergebnisse einer Phase‑1‑Erst‑in‑Mensch‑Studie
Warum dieses neue Krebsmedikament wichtig ist
Für Menschen mit multiplem Myelom, einer Blutkrebserkrankung, die nach einer Behandlung fast immer wiederkehrt, kann jede neue Option mehr Lebenszeit und bessere Lebensqualität bedeuten. Diese Studie prüft eine nächste Generation der Immuntherapie namens Alnuctamab, entwickelt, um körpereigene Abwehrzellen dabei zu unterstützen, Myelomzellen zu finden und zu zerstören. Die Forschung beantwortet eine praktische Frage, die für Patientinnen, Patienten und Ärztinnen und Ärzte gleichermaßen zählt: Lässt sich diese potente Therapie als einfache Unter‑der‑Haut‑Injektion verabreichen, mit starker anti‑tumoraler Wirkung, aber weniger gefährlichen Nebenwirkungen?
Ein kluger Weg, das Immunsystem umzulenken
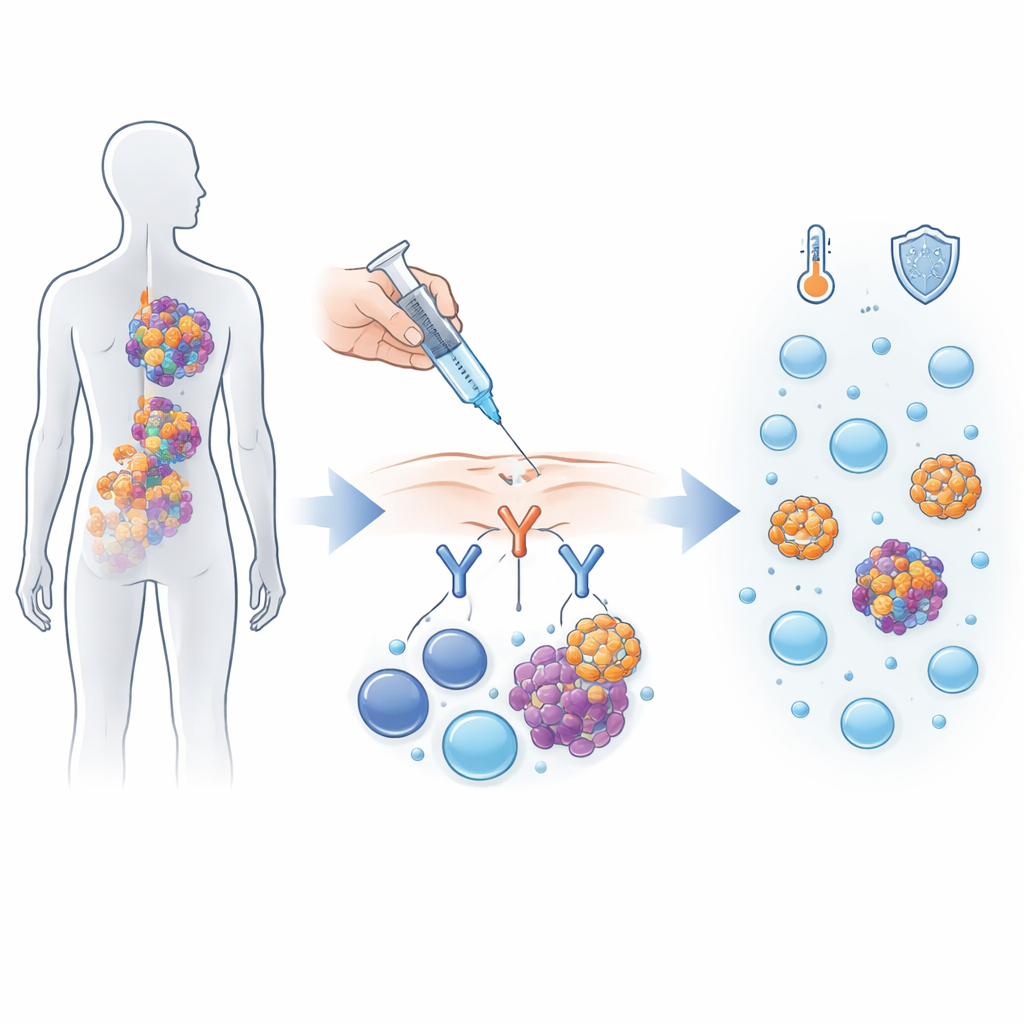
Alnuctamab gehört zu einer neuen Wirkstoffklasse, die wie molekulare Kuppler zwischen Krebszellen und Immunzellen wirkt. Myelomzellen tragen an ihrer Oberfläche einen Marker namens BCMA, während körpereigene T‑Zellen einen anderen Marker, CD3, tragen. Alnuctamab ist so konstruiert, dass es zwei „Arme“ hat, die an BCMA binden, und einen Arm, der an CD3 bindet, wodurch T‑Zellen in engen Kontakt mit Myelomzellen gebracht werden, damit sie diese angreifen können. In dieser Erst‑in‑Mensch‑Studie erhielten 165 Personen mit einem nach mindestens drei verschiedenen Behandlungsarten rückfällig gewordenen Myelom Alnuctamab, entweder intravenös über einen Tropf oder subkutan unter die Haut.
Von der Infusion zur Injektion
Anfangs wurde das Medikament über die Vene verabreicht, doch dieser Ansatz löste stärkere Immunreaktionen aus, darunter eine lebensbedrohliche Episode eines Komplikationsbildes namens Zytokinfreisetzungssyndrom, bei dem das Immunsystem plötzlich große Mengen entzündlicher Signale ausschüttet. Wegen dieser Sicherheitsbedenken und des nur mäßigen Nutzens stellte die Studie auf die subkutane Verabreichung um, die das Medikament gleichmäßiger freisetzt. Fünfundneunzig Patientinnen und Patienten wurden so mit einem „Step‑up“‑Schema behandelt: kleine Einstiegsdosen gefolgt von höheren Zieldosen, wobei die Häufigkeit der Injektionen im Laufe der Zeit von wöchentlich auf alle vier Wochen reduziert wurde, sofern die Behandlung fortgesetzt wurde.
Wie gut es den Patienten ging und was sie in Kauf nahmen
Unter allen Patienten, die die subkutanen Injektionen erhielten, verkleinerte sich das Tumorvolumen bei etwa 59 % der Fälle um mindestens die Hälfte, und fast die Hälfte wurde „minimal residual disease negativ“—das heißt, hochsensitive Tests konnten keine Myelomzellen mehr im Knochenmark nachweisen. Bei der empfohlenen Dosis von 30 Milligramm waren die Ansprechraten sogar noch besser: etwa 71 % sprachen an und mehr als die Hälfte erreichte MRD‑Negativität. Viele Patientinnen und Patienten konnten ihre Erkrankung fast ein Jahr oder länger kontrollieren, selbst während die Dosisintervalle weniger intensiv wurden. Nebenwirkungen waren häufig, aber größtenteils beherrschbar. Fieberähnliche Immunreaktionen traten bei etwa drei von fünf Patientinnen und Patienten auf, waren jedoch allesamt leicht bis mäßig. Niedrige weiße Blutkörperchenzahlen und Infektionen traten ebenfalls auf, was sowohl die Wirkstärke des Medikaments als auch die bereits geschwächte Immunlage der Patienten widerspiegelt; schwere Infektionen waren jedoch seltener als bei mehreren ähnlichen Präparaten berichtet.
Warum die Injektionsroute sicherer war
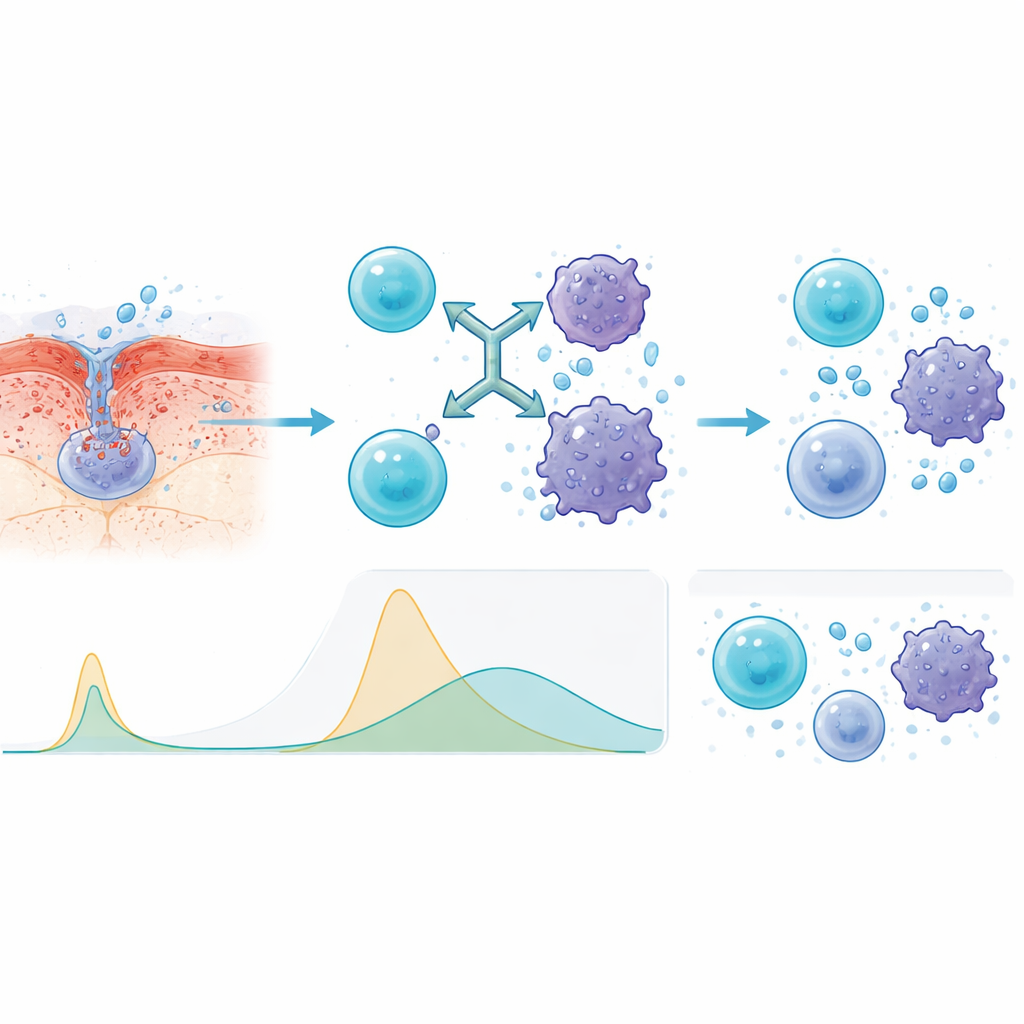
Um zu verstehen, warum die subkutane Methode besser abschnitt, maßen die Forschenden immunaktive Signalmoleküle im Blut. Im Vergleich zur intravenösen Infusion erzeugten Injektionen langsamere und niedrigere Spitzen bei wichtigen entzündlichen Botenstoffen wie Interleukinen und Tumornekrosefaktor. Dieses abgeflachte Profil bedeutet, dass das Immunsystem weiterhin gegen den Krebs aktiviert wird, jedoch ohne die gleiche plötzliche Ausschüttung, die Patientinnen und Patienten gefährlich krank machen kann. Das Team stellte außerdem fest, dass Personen mit niedrigeren Startwerten von ‚shed BCMA‘ im Blut—ein Zeichen für weniger aggressive oder weniger fortgeschrittene Erkrankung—tendenziell besser ansprachen und länger in Remission blieben.
Was das für die zukünftige Myelombehandlung bedeutet
Obwohl das Unternehmen sich später aus strategischen Gründen gegen eine weitere Entwicklung von Alnuctamab entschieden hat, sind die Lehren aus dieser Studie bedeutsam. Die Untersuchung zeigt, dass ein sorgfältig gestalteter Immun‑Engager als einfache Injektion verabreicht werden kann, auf einem Zeitplan, der mit der Zeit weniger belastend wird, und dennoch bei vielen Menschen mit schwer behandelbarem Myelom tiefe und dauerhafte Ansprechraten erzielt. Sie legt außerdem nahe, dass ein schrittweises Hochdosieren und das Vermeiden scharfer Spitzen in der Immunaktivierung schwere Reaktionen begrenzen kann, ohne die antitumorale Wirkung zu beeinträchtigen. Diese Erkenntnisse werden voraussichtlich die Entwicklung künftiger immunbasierter Therapien leiten und bieten die Hoffnung, dass mehr Patientinnen und Patienten mit rezidiviertem Myelom wirksame Therapien erhalten, die nicht nur stark, sondern auch sicherer und lebensverträglicher sind.
Zitation: Bar, N., Martin, T., Hofmeister, C.C. et al. Alnuctamab, a bivalent B-cell maturation antigen-targeting T cell engager for patients with relapsed or refractory multiple myeloma: results from a phase 1, first-in-human study. Leukemia 40, 481–490 (2026). https://doi.org/10.1038/s41375-025-02841-x
Schlüsselwörter: multiples Myelom, Immuntherapie, bispezifischer Antikörper, BCMA, T‑Zell‑Engager