Clear Sky Science · de
Löslicher Notch-Agonist ermöglicht die Reifung menschlicher Ameloblasten und die Bildung von schmelzähnlichem Gewebe zur Zahnregeneration
Warum es so schwer ist, Zahnschmelz zu reparieren
Schmelz, die glasig weiße Schicht, die unsere Zähne überzieht, ist das härteste Material im menschlichen Körper – aber ist er erst einmal verloren, ist er verloren. Mehr als 90 Prozent der Erwachsenen haben irgendeinen Schmelzverlust oder -schäden, doch unsere Zähne besitzen keine natürliche Fähigkeit, diese Schutzschicht wieder aufzubauen. Diese Studie beschreibt eine Methode, menschliche schmelzbildende Zellen im Labor zu züchten, sie bis zu einem voll ausgereiften Zustand zu bringen und sie sogar dazu zu veranlassen, in Tieren schmelzähnliches Mineral zu bilden. Die Arbeit öffnet einen Weg zu möglichen zukünftigen Therapien, die Zähne mit lebendem Gewebe statt mit Füllungen und Kronen reparieren könnten.
Zahnschmelz aus Stammzellen aufbauen
Schmelz wird von spezialisierten Zellen, den Ameloblasten, gebildet, die nach dem Durchbruch eines Zahns durch das Zahnfleisch absterben. Ohne sie können erwachsene Zähne keinen neuen Schmelz bilden. Die Forscher nutzen humane induzierte pluripotente Stammzellen – ausgereifte Zellen, die in einen flexiblen, embryonal-ähnlichen Zustand zurückprogrammiert wurden – um „induzierte Ameloblasten“ zu erzeugen. In früheren Arbeiten konnten diese im Labor gezüchteten Zellen beginnen, natürlichen schmelzbildenden Zellen ähnlich zu werden, blieben aber vor der vollständigen Reifung stehen und funktionierten nur dann richtig, wenn sie in engem Kontakt mit Odontoblasten wuchsen, den Zellen, die das darunterliegende Dentin bilden. Daraus ergab sich eine zentrale Frage: Was genau liefern Odontoblasten, das Ameloblasten benötigen, um ihre Entwicklung abzuschließen?
Die fehlende Kommunikation zwischen Zahnzellen
Um diesen zellulären Dialog zu entschlüsseln, analysierte das Team Einzelzell-Genexpressionskarten sich entwickelnder menschlicher und Mauszähne. Sie suchten nach Signalwegen, die offensichtlich speziell von Odontoblasten zu Ameloblasten während des entscheidenden Zeitfensters laufen, in dem Schmelz entsteht. Ein Weg hob sich hervor: Notch, ein direkter Zell-zu-Zell-Kommunikationsmechanismus, der vielfach in der Embryonalentwicklung verwendet wird. In diesen Zahnkarten fanden sich Delta-ähnliche Liganden (insbesondere DLL1 und DLL4) vorwiegend auf Odontoblasten, während Notch-Rezeptoren auf sich reifenden Ameloblasten konzentriert waren. Als die Forscher die Notch-Aktivität mit einem Medikament in ihrem Ko-Kultursystem blockierten, reduzierten die Ameloblasten die Produktion von Enamelin, einem wichtigen Schmelzprotein, stark – ein starker Hinweis darauf, dass Notch-Signalgebung für die Reifung schmelzbildender Zellen essenziell ist. 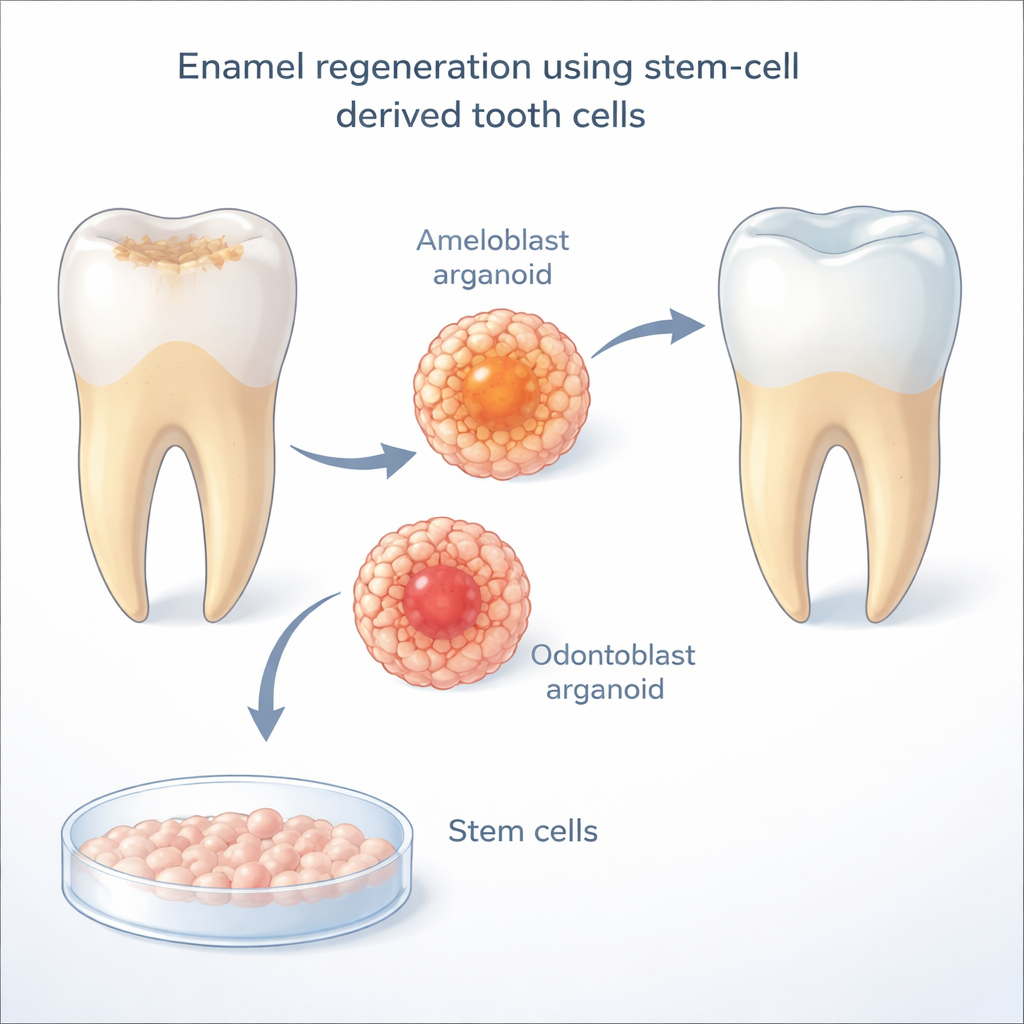
Ein KI-entworfenes Proteinschalter für Schmelzzellen
Um einen Schritt weiterzugehen, wollten die Forschenden Notch auf präzise und kontrollierbare Weise einschalten, ohne auf echte Odontoblasten angewiesen zu sein. Sie verwendeten ein künstliches Protein namens C3-DLL4, das mit Rechentools entworfen wurde. Dieses lösliche Molekül ordnet drei Kopien der DLL4-Signaldomäne in einem starren, dreiarmsigen Gerüst an, wodurch es Notch-Rezeptoren auf benachbarten Zellen ähnlich wie eine natürliche Nachbarzelle zusammenziehen und aktivieren kann. In Reporterzelllinien schaltete C3-DLL4 stark Notch-abhängige Gene ein. Als es frühen Ameloblast-Organoiden – winzigen 3D-Zellverbänden aus Stammzellen – zugesetzt wurde, bewirkte es einen umfassenden Wechsel im Genexpressionsprofil. Die Organoide verschoben sich von einem unreifen Profil hin zu einem, das sekretorischen und voll ausgereiften Ameloblasten entsprach, und schalteten charakteristische Gene wie AMELX, ENAM, MMP20, ODAM, KLK4, TUFT1 und WDR72 ein. Die Entfernung der Notch-Aktivität hatte den gegenteiligen Effekt, stoppte die Reifung und störte die Produktion von Schmelzproteinen.
Von Organoiden zu schmelzähnlichem Gewebe
Bemerkenswerterweise begannen diese durch Notch aktivierten Ameloblast-Organoide, nachdem sie unter die Nierenkapsel immundefizienter Mäuse transplantiert worden waren – eine sichere, gut versorgte Nische, die häufig zum Testen menschlicher Gewebe verwendet wird – dichte, mineralisierte Substanz abzusetzen. Hochauflösende Mikro-CT-Scans und klassische Anfärbemethoden für Knochen bestätigten das Vorhandensein verkalkter Nodule an Stellen, an denen normalerweise kein solches Gewebe existiert. Die Mikroskopie zeigte organisierte, polarisierte Schichten menschlicher Zellen, die wichtige Schmelzproteine und WDR72 exprimierten, einen Faktor, der mit korrekter Schmelzmineralisierung in Verbindung steht. Auch wenn dieses Material besser als „schmelzähnlich“ denn als vollständig natürlicher Schmelz beschrieben wird, zeigt es, dass gentechnisch erzeugte menschliche Ameloblasten prinzipiell hartes Mineral in einem lebenden Organismus ablagern können. 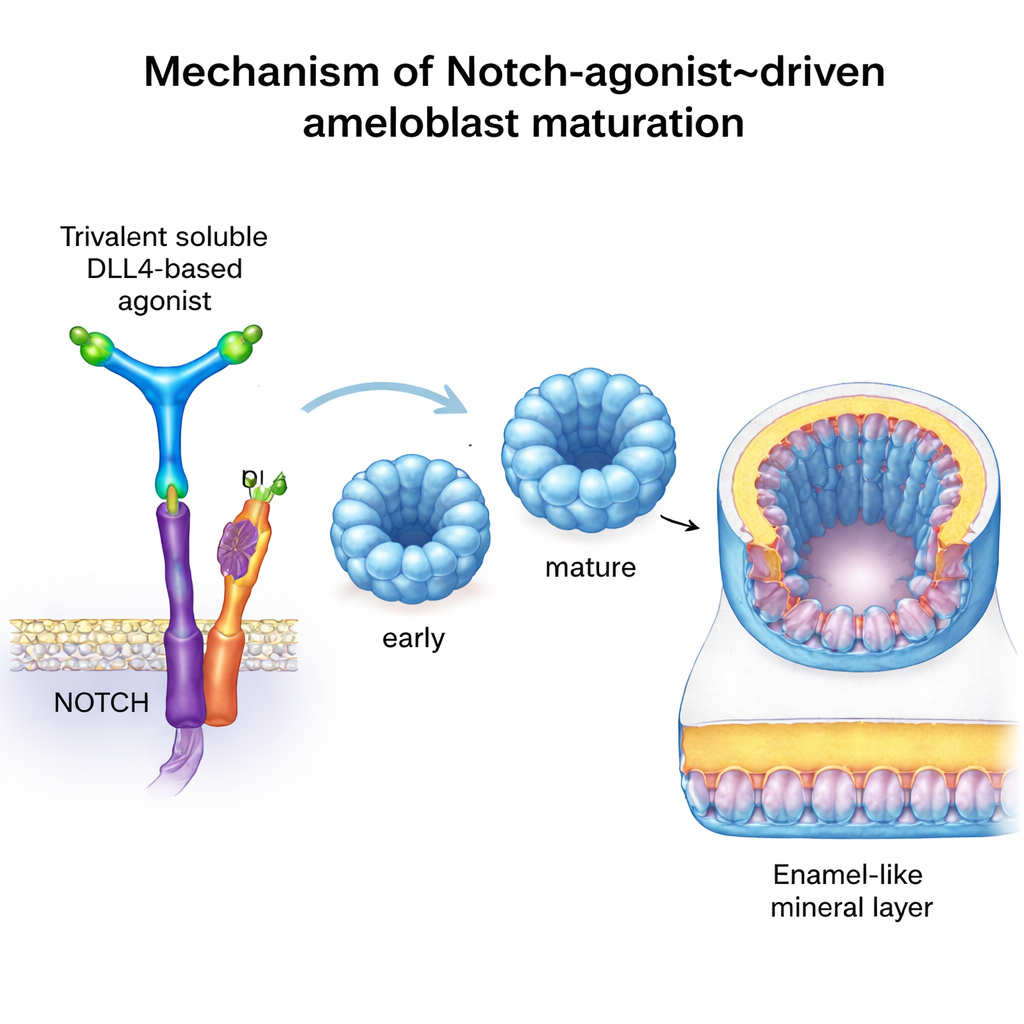
Ein genetisches Rätsel um schwachen Schmelz lösen
Die Studie geht außerdem ein langjähriges Rätsel um ein Gen namens DLX3 an, dessen Mutationen bestimmte vererbte Schmelzdefekte verursachen und das Kariesrisiko erhöhen. DLX3 ist sowohl in Ameloblasten als auch in Odontoblasten aktiv, wodurch schwer zu sagen ist, welche Zellart am stärksten betroffen ist, wenn etwas schiefgeht. Mithilfe ihres odontoblastfreien Organoid-Systems und CRISPR-Geneditierung entfernten die Forscher DLX3 gezielt in der Ameloblastenlinie. Frühere Schritte der Ameloblastenbildung traten noch auf, doch die letzte Reifungsphase brach zusammen: Schlüssel-Schmelzproteine wie Enamelin, AMELX, MMP20, KLK4, TUFT1 und WDR72 waren sowohl auf RNA- als auch auf Proteinebene drastisch reduziert. Das zeigt, dass DLX3 direkt innerhalb menschlicher Ameloblasten erforderlich ist, um das Schmelzbildungsprogramm abzuschließen, und hilft zu erklären, warum Varianten in der Nähe dieses Gens mit bruchanfälligen, kariesanfälligen Zähnen verknüpft sind.
Was das für die zukünftige Zahnmedizin bedeuten könnte
Gemeinsam zeichnen diese Befunde eine Schritt-für-Schritt-Roadmap von Stammzellen über schmelzproduzierende Organoide bis hin zu schmelzähnlichem Gewebe in vivo, gesteuert durch einen einstellbaren Notch-„Ein“-Schalter und das DLX3-Gen. Obwohl die klinische Zahnregeneration noch in weiter Ferne liegt, bietet diese Arbeit eine leistungsfähige Testplattform, um genetische Zahnkrankheiten zu verstehen, neue Behandlungen zu screenen und Strategien zu verfeinern, verlorenen Schmelz mit lebenden Zellen statt mit inertem Material wieder aufzubauen. Für Patientinnen und Patienten besteht die langfristige Hoffnung, dass ein Zahnarztbesuch eines Tages darin bestehen könnte, abgenutzte oder kariöse Zähne mit bioingeniertem Schmelz zu reparieren, der sich viel natürlicher verhält.
Zitation: Patni, A.P., Mout, R., Alghadeer, A. et al. Soluble Notch agonist enables human ameloblast maturation and enamel-like tissue formation for tooth regeneration. Int J Oral Sci 18, 25 (2026). https://doi.org/10.1038/s41368-026-00429-4
Schlüsselwörter: Schmelzregeneration, Ameloblast-Organoide, Notch-Signalgebung, DLX3, Zahnstammzellen