Clear Sky Science · de
Gli2 und Gli3 vermitteln synergetisch die HH–TGF-β‑Wechselwirkung in mesenchymalen Vorläuferzellen zur Orchestrierung der Zahnwurzelmorphogenese
Warum Zahnwurzeln wichtiger sind, als Sie denken
Die meisten von uns denken nur an ihre Zähne, wenn sie wehtun oder man sie im Spiegel sieht. Doch das, was jeden Zahn im Kiefer verankert — die Wurzel — ist ebenso bedeutsam wie die sichtbare Krone. Gesunde Wurzeln halten Zähne beim Kauen und Sprechen ein Leben lang stabil. Diese Studie untersucht, wie winzige Signale im Kiefergewebe unreifen Zellen mitteilen, wie sie starke Zahnwurzeln aufbauen sollen — ein Mechanismus, der eines Tages helfen könnte, Wurzeldefekte zu verhindern oder zu reparieren, die zu locker sitzenden Zähnen und Zahnverlust führen.
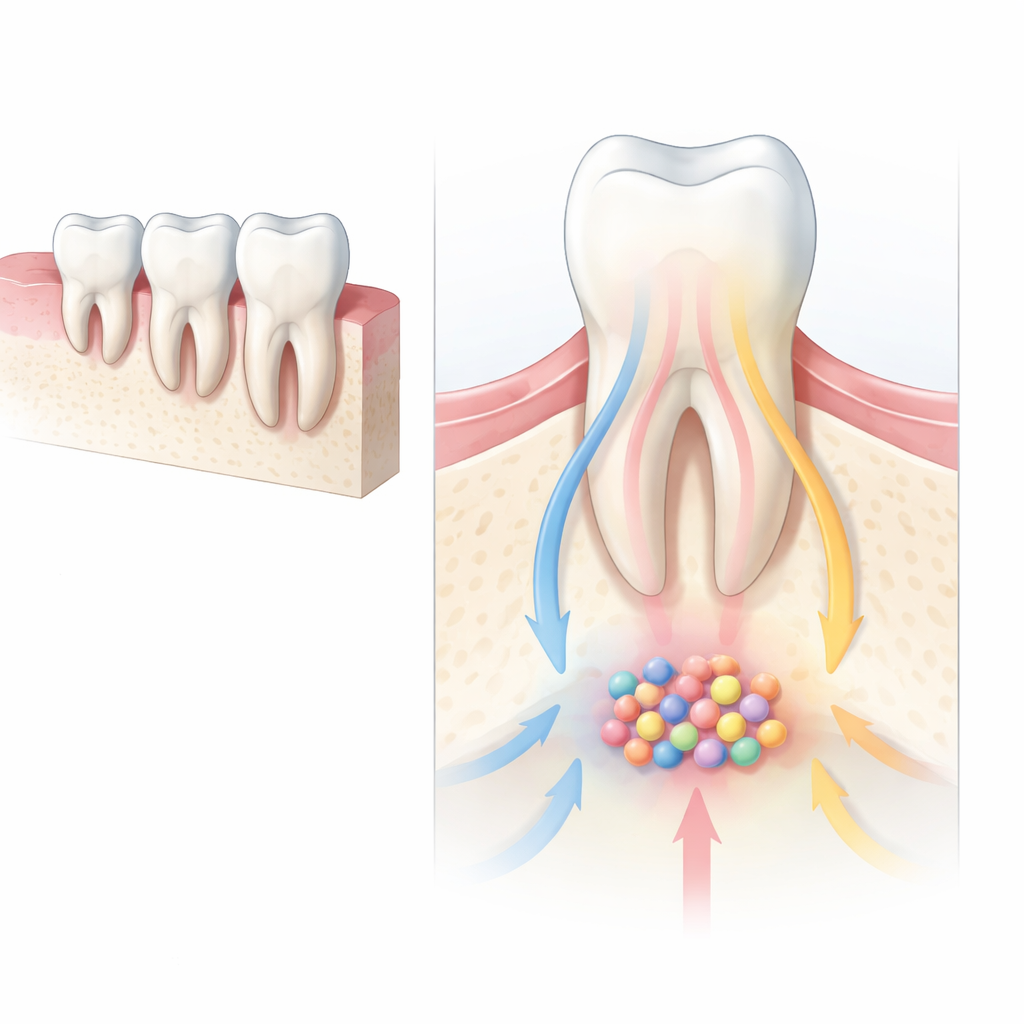
Die wandernden Zellen, die unser Gesicht formen
Früh in der Entwicklung wandert eine besondere Zellpopulation, die so genannten kranialen Neuralleistenzellen, in das sich formende Gesicht und die Kiefer ein und differenziert dort zu Knochen, Knorpel und den zahnstützenden Geweben. Wenn diese Umwandlung fehlerhaft verläuft, können Babys mit schweren Gesichts‑ und Zahnfehlbildungen geboren werden. Ein Schlüssel‑Signal, das diese Zellen leitet, ist der Hedgehog‑Weg, der wie ein molekulares GPS wirkt und den Zellen hilft zu entscheiden, wohin sie gehen und was sie werden sollen. Die Autoren konzentrierten sich auf zwei durch Hedgehog gesteuerte Helferproteine, Gli2 und Gli3, um zu untersuchen, wie sie gemeinsam die Zellen lenken, die schließlich die Wurzeln der Backenzähne bei Mäusen aufbauen.
Zwei genetische Schalter, die im Team arbeiten
Mithilfe fein konstruierter Maussysteme schalteten die Forschenden Gli2, Gli3 oder beide selektiv in einer Gruppe wurzelbildender Vorläuferzellen aus, die sich in der Nähe der wachsenden Wurzelspitzen befinden. Die Entfernung von Gli2 allein veränderte die Wurzelbildung kaum, während das Entfernen von Gli3 deutlich kürzere Wurzeln, verzögertes Zahndurchbruch und weniger stützenden Kieferknochen um die Zähne verursachte. Wurden sowohl Gli2 als auch Gli3 gemeinsam entfernt, wurden die Probleme deutlich schwerer: Die Wurzeln waren etwa halb so lang wie normal, der Zahndurchbruch verzögerte sich und der Knochen, der die Wurzeln normalerweise umgibt, war stark reduziert. Diese Experimente zeigen, dass Gli2 und Gli3 nicht isoliert wirken, sondern kooperativ die Wurzel und ihre umgebenden Stützstrukturen formen.
Zellen in die richtigen Aufgaben lenken
Um zu verstehen, warum die Wurzeln fehlschlugen, untersuchte das Team genau, was aus den Wurzel‑Vorläuferzellen normalerweise wird. In gesunden Zähnen differenzieren diese Zellen zu odontoblasten, die Dentin produzieren, zu faserigen Bandzellen, die die Wurzel mit dem Knochen verbinden, und zu knochenbildenden Zellen in der Alveole. Wenn Gli3, und besonders sowohl Gli2 als auch Gli3, fehlten, waren diese Zelllinien gestört: Wichtige Marker für Dentin‑ und Band‑Identität waren stark vermindert, und weniger knochenbildende Zellen erschienen in der Nähe der Wurzeln. Die Verfolgung der Nachkommen der Vorläuferzellen zeigte, dass viele dieser Zellen statt die Wurzel und ihr Band zu besiedeln, weiter oben im Zahnbereich verblieben — ein Hinweis darauf, dass ihre normalen „Karriereentscheidungen“ fehlgeleitet wurden. Gleichzeitig sank die Zahl teilender Zellen in der Wurzelregion, sodass weniger Bausteine zur Verfügung standen, um die Wurzel zu konstruieren.
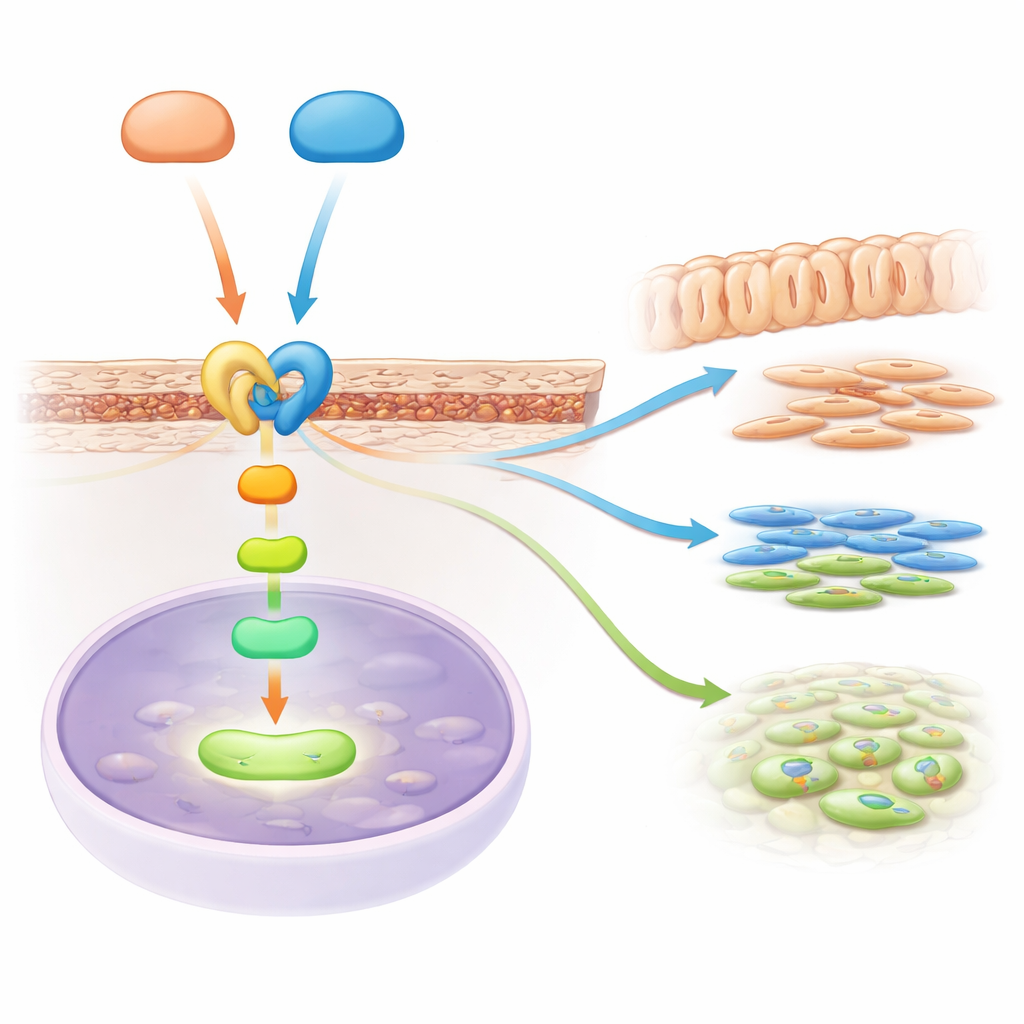
Eine Signalweiterleitung, die zwei große Wege verbindet
Die Geschichte endete nicht beim Hedgehog‑Signal. Durch das Ablesen, welche Gene an‑ oder abgeschaltet waren, entdeckten die Wissenschaftler, dass ein weiterer wichtiger Weg, die TGF‑beta‑Signalgebung, abgeschwächt war, wenn Gli2 und Gli3 verloren gingen. TGF‑beta ist bekannt dafür, die Bildung von Dentin und Knochen zu fördern. Das Team identifizierte ein zentrales Relay‑Molekül, einen Rezeptor namens Acvr2b, der an der Oberfläche der Wurzelvorläuferzellen sitzt und hilft, TGF‑beta‑Familien‑Signale in die Zelle weiterzuleiten. Sie zeigten, dass sowohl Gli2 als auch Gli3 physisch an die Kontrollregion des Acvr2b‑Gens binden und dessen Aktivität steigern. Ohne diese Helfer sanken die Acvr2b‑Spiegel in der Wurzelregion und die nachgeschalteten TGF‑beta‑Signalgeber in den Zellen waren weniger aktiv, wodurch die Instruktionen für Wachstum und Differenzierung der Wurzel abgeschwächt wurden.
Ein teilweise umgebautes, fehlerhaftes Wurzelbauprogramm
Um zu testen, ob die Wiederbelebung der TGF‑beta‑Signalgebung helfen könnte, behandelten die Forschenden Mäuse, denen sowohl Gli2 als auch Gli3 fehlten, mit einem Medikament, das diesen Weg stimuliert. Obwohl sich die normalen Wurzeln nicht vollständig wiederherstellen ließen, verlängerte die Behandlung die Wurzeln, vergrößerte die Menge des umgebenden Knochens und verbesserte die Bildung von Dentin und Bandgewebe im Vergleich zu unbehandelten Mutantenmäusen. Diese partielle Rettung legt nahe, dass die Kette Gli2/Gli3–Acvr2b–TGF‑beta ein wichtiger Pfad ist, über den Hedgehog‑Signale in das strukturelle Wachstum der Zahnwurzeln übersetzt werden.
Was das für die zukünftige Zahnmedizin bedeutet
Vereinfacht gesagt zeigt diese Arbeit, dass zwei genetische „Schalter“, Gli2 und Gli3, zusammenarbeiten, damit junge Kieferzellen Hedgehog‑Signale wahrnehmen und über eine Weiterleitung, die TGF‑beta einschließt, entscheiden, zu welchen spezialisierten Zellen sie werden, die Zahnwurzeln bauen und stützen. Bricht diese Kommunikation zusammen, sind die Wurzeln kurz, der Zahndurchbruch gestört und der stützende Knochen dünn. Das Verständnis dieses Signalinfrastrukturnetzes klärt nicht nur, wie normale Zahnwurzeln entstehen, sondern weist auch auf neue Strategien hin, wie man Stamm‑ oder Vorläuferzellen lenken könnte, um beschädigte Wurzeln zu reparieren oder sie künftig in regenerativen zahnmedizinischen Therapien vollständig neu zu erzeugen.
Zitation: Zhou, T., Huang, L., Xie, Y. et al. Gli2 and Gli3 synergistically mediate HH-TGF-β crosstalk in mesenchymal progenitor cells to orchestrate tooth root morphogenesis. Int J Oral Sci 18, 30 (2026). https://doi.org/10.1038/s41368-026-00427-6
Schlüsselwörter: Zahnwurzelentwicklung, kraniale Neuralleistenzellen, Hedgehog-Signalgebung, TGF‑beta‑Signalweg, dentale Stammzellen