Clear Sky Science · de
Ein Einzelzell‑Transkriptionsatlas zeigt unterschiedliche Mechanismen des Immun‑Chondrozyten‑Dialogs bei durch verschiedene Okklusionsstörungen induzierter Arthrose des Kiefergelenks
Warum Ihr Kiefergelenk wichtig ist
Die kleinen Gelenke vor Ihren Ohren, die sogenannten Temporomandibulargelenke (TMJ), ermöglichen Sprechen, Kauen, Gähnen und Lachen. Wenn sie Arthrose entwickeln, können alltägliche Bewegungen schmerzhaft und erschwert werden. Diese Studie verwendet fortschrittliche Einzelzell‑Genanalysen bei Mäusen, um diese Kiefergelenke Zelle für Zelle zu untersuchen. Sie zeigt, wie verschiedene Bissanomalien unterschiedliche Schadensmuster auslösen — und wie das präzisere Behandlungsansätze informieren könnte.
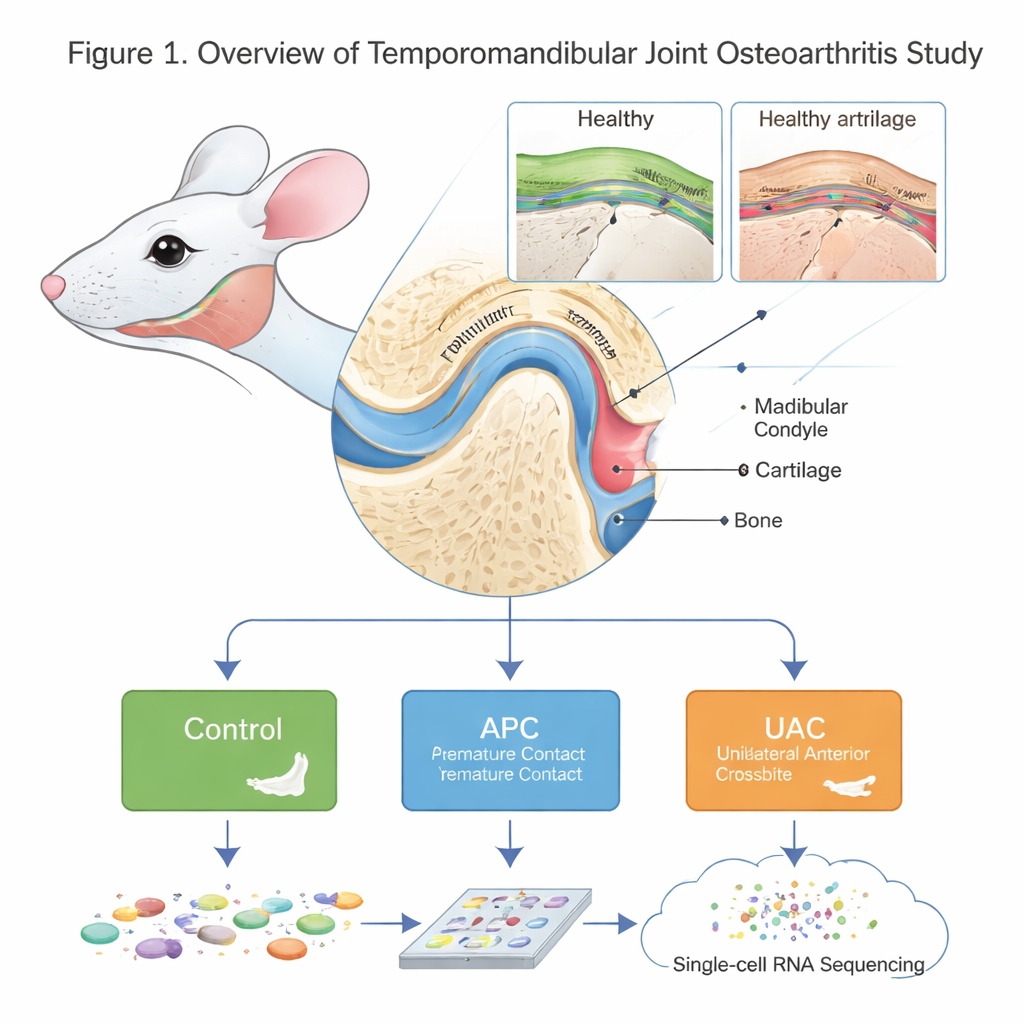
Ein genaues Bild eines kleinen, aber komplexen Gelenks
Das TMJ ist kein einfacher Scharniermechanismus. Sein abgerundetes Ende, der Unterkieferkondylus, ist von einer speziellen Knorpelschicht bedeckt und wird vom darunter liegenden Knochen gestützt. Arthrose in diesem Gelenk (TMJOA) verursacht Schmerzen, Steifheit und Funktionsverlust, doch die mikroskopischen und molekularen Ursachen waren schwer zu durchschauen. Die Autorinnen und Autoren erstellten einen detaillierten „Zellatlas“ des Maus‑Kondylus in Gesundheit und Krankheit mit Einzelzell‑RNA‑Sequenzierung, einer Methode, die abliest, welche Gene in tausenden einzelnen Zellen aktiv sind. Sie verglichen gesunde Mäuse mit zwei Modellen von Bissungleichgewicht — anteriorer vorzeitiger Kontakt (APC), bei dem die Frontzähne zu früh aufeinandertreffen, und unilateral anteriorer Kreuzbiss (UAC), bei dem eine Seite der Frontzähne falsch aufeinander beißt — die beide dafür bekannt sind, das Kiefergelenk zu überlasten.
Viele Arten von Knorpelzellen, nicht nur eine
Traditionell wurde der kondyläre Knorpel in groben Schichten beschrieben — proliferierende, ausgereifte und hypertrophe Zellen. Diese Studie zeigt, dass das tatsächliche Bild deutlich vielfältiger ist. Das Team identifizierte mehrere Subtypen von Chondrozyten (Knorpelzellen), jeder mit eigener Genaktivität und vermuteter Rolle. Es gab progenitorische Zellen nahe der Oberfläche, die wie ein Reparaturpool wirken, fibröse Chondrozyten, die an narbenähnlicher Matrix und Heilung beteiligt sind, entzündungsassoziierte Chondrozyten, die entzündliche Signale produzieren, mineralisierungsassoziierte und hypertrophe Chondrozyten, die am Übergang von Knorpel zu Knochen beteiligt sind, sowie reparative Zellen, die Stress und Entzündung dämpfen. In gesunden Gelenken sind diese Subtypen spatial geordnet und folgen einer glatten Entwicklungs‑„Trajectory“ vom Progenitor zu reiferen Zuständen.
Wenn Bissprobleme die zelluläre Ordnung des Gelenks durcheinanderbringen
Sowohl APC‑ als auch UAC‑Modelle führten zu dünnerem Knorpel, Oberflächenrauheit und typischen arthroseartigen Läsionen im Kondylus. Auf zellulärer Ebene sank der Anteil an Chondrozyten, während Immunzellen zunahmen. Im APC kam es zu einem Anstieg bestimmter mineralisierender und hypertropher Chondrozyten und zu einer Störung der normalen Progression vom Progenitor zur Ausreifung. Im UAC stieg außerdem der Anteil fibröser und reparativer Chondrozyten, was auf stärkere Reparatur‑ und Umbaumuster hindeutet. Die Mikroskopie bestätigte, dass Zellen ihre geordneten Schichten verloren und im erkrankten Knorpel verdichtet und desorganisiert waren — ein Befund, der zu den durch Genexpressionsdaten vermuteten gestörten Entwicklungspfaden passt.
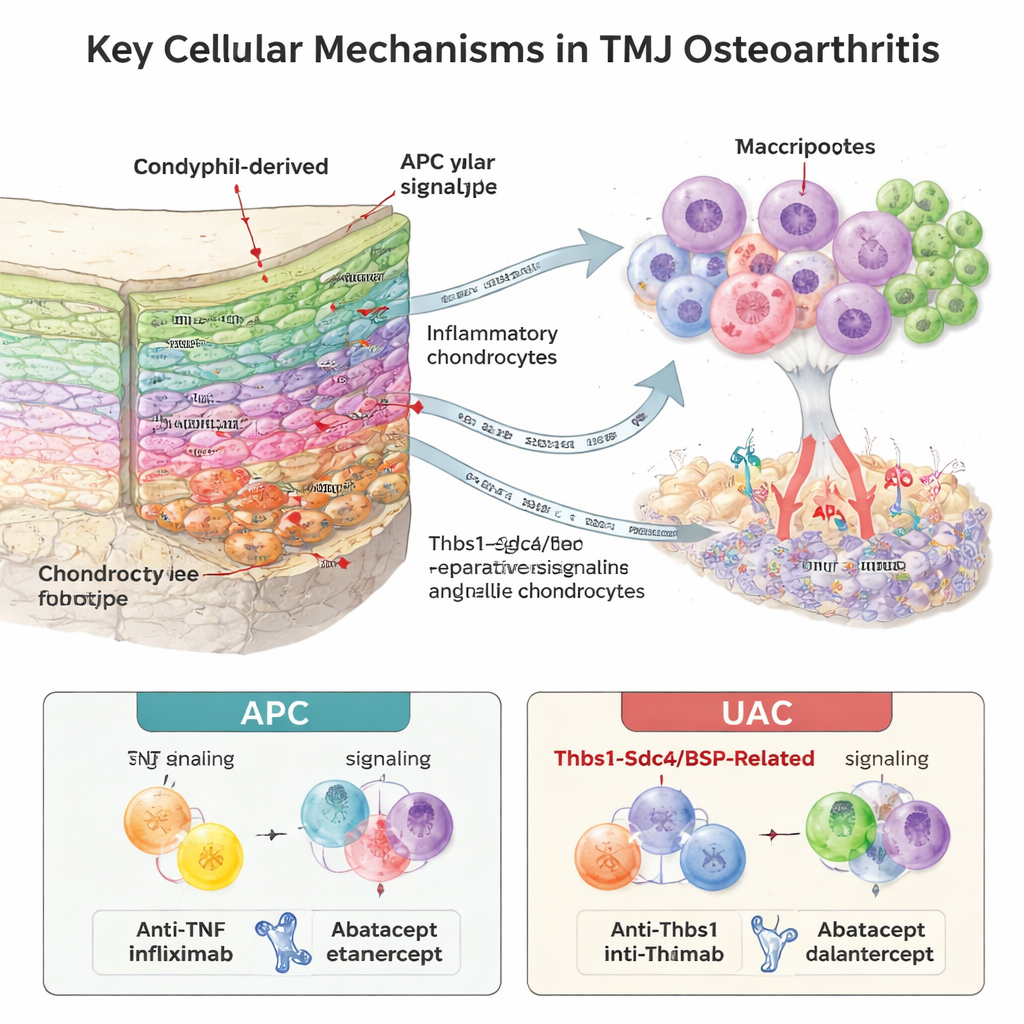
Immunzellen, Blutgefäße und Knorpel im Dialog
Der stützende Knochen und das Knochenmark des Kondylus beherbergten ein überraschend reiches immunologisches „Mikroumfeld“. Die Forschenden fanden neun Immunzelltypen, wobei Neutrophile (schnell reagierende weiße Blutkörperchen) in erkrankten Gelenken stark zunahmen, besonders in einem spezifischen Reifestadium. Durch die Analyse ko‑exprimierter Signalmoleküle und Rezeptoren schlossen sie auf intensive „Wechselwirkung“ zwischen Immunzellen und Chondrozyten. Im APC‑Modell wurden Neutrophile zur Hauptquelle von TNF‑alpha, einem starken entzündlichen Signal, das schädliche Botschaften an Knorpelzellen sendet. Im UAC‑Modell zeigte sich ein anderes Muster: knochen‑ und knorpelbezogene Signale, darunter Bone Sialoprotein (BSP) und der Thbs1–Sdc4‑Weg, waren prominenter und eng mit neuem Gefäßwachstum an der Grenze zwischen Knorpel und Knochen verknüpft. BSP‑reiche Bereiche überlappten mit Markern der Angiogenese, was darauf hindeutet, dass eindringende Gefäße und rekrutierte Immunzellen gemeinsam die Knorpelerosion antreiben.
Maßgeschneiderte Therapien für unterschiedliche Gelenkbelastungen
Um zu testen, ob diese unterschiedlichen Signale wirklich relevant sind, behandelte das Team Mäuse während der Krankheitsentwicklung mit Wirkstoffen, die spezifische Wege blockieren. Bei APC‑induzierter TMJOA schützte die Blockade von TNF‑alpha mit dem Medikament Etanercept klar den Knorpel, während ein Wirkstoff, der neutrophile Anziehungsrezeptoren hemmt (Navarixin), wenig Unterschied machte. Im Gegensatz dazu linderte bei UAC‑induzierter TMJOA Navarixin die Knorpelschäden deutlich, was zu einem stärker neutrophil‑getriebenen Gefäß‑Eindringen und Umbau passenden Krankheitsprozess passt, während Etanercept schwächere Effekte zeigte. Diese Befunde legen nahe, dass TMJ‑Arthrose keine einzelne Krankheit ist, sondern eine Gruppe verwandter Erkrankungen, die davon geprägt sind, wie das Gelenk mechanisch belastet wird, und dass wirksame Therapien an die spezifischen mechanischen und zellulären Muster jedes Patienten angepasst werden sollten.
Was das für Menschen mit Kieferschmerzen bedeutet
Für Personen mit Kieferknacken, Schmerzen oder eingeschränkter Mundöffnung betont diese Forschung zwei zentrale Punkte. Erstens wird das Kiefergelenk von einer vielfältigen Gemeinschaft aus Knorpel‑ und Immunzellen erhalten, die das Gewebe je nach Aktivierung schützen oder schädigen kann. Zweitens können verschiedene Bissprobleme diese Gemeinschaft in unterschiedliche schädliche Richtungen treiben — die eine stärker durch klassische Entzündung geprägt, die andere durch abnormales Gefäßwachstum und Knochen‑Knorpel‑Umbau. Langfristig könnte diese Art von Einzelzellkartierung Zahnärzten und Ärztinnen helfen, von Einheits‑Therapien zu individuell abgestimmten Ansätzen überzugehen, die Bisskorrektur mit gezielten Medikamenten kombinieren, die zum spezifischen Schadensmuster des Patienten passen.
Zitation: Wang, K., Li, Y., Xiang, S. et al. Single-cell transcriptional atlas reveals distinct immune-chondrocyte crosstalk mechanisms in temporomandibular joint osteoarthritis induced by different types of occlusal disorder. Int J Oral Sci 18, 22 (2026). https://doi.org/10.1038/s41368-025-00424-1
Schlüsselwörter: Arthrose des Kiefergelenks (TMJ), Einzelzell‑RNA‑Sequenzierung, Chondrozyten, Neutrophile, Okklusionsstörung