Clear Sky Science · de
Die Implantation weckt das periimplantäre osteogene Potenzial über die Snx5‑EGFR‑Achse vermittelte mechanische Transduktion
Warum es wichtig ist, den Kieferknochen nach Zahnverlust zu erhalten
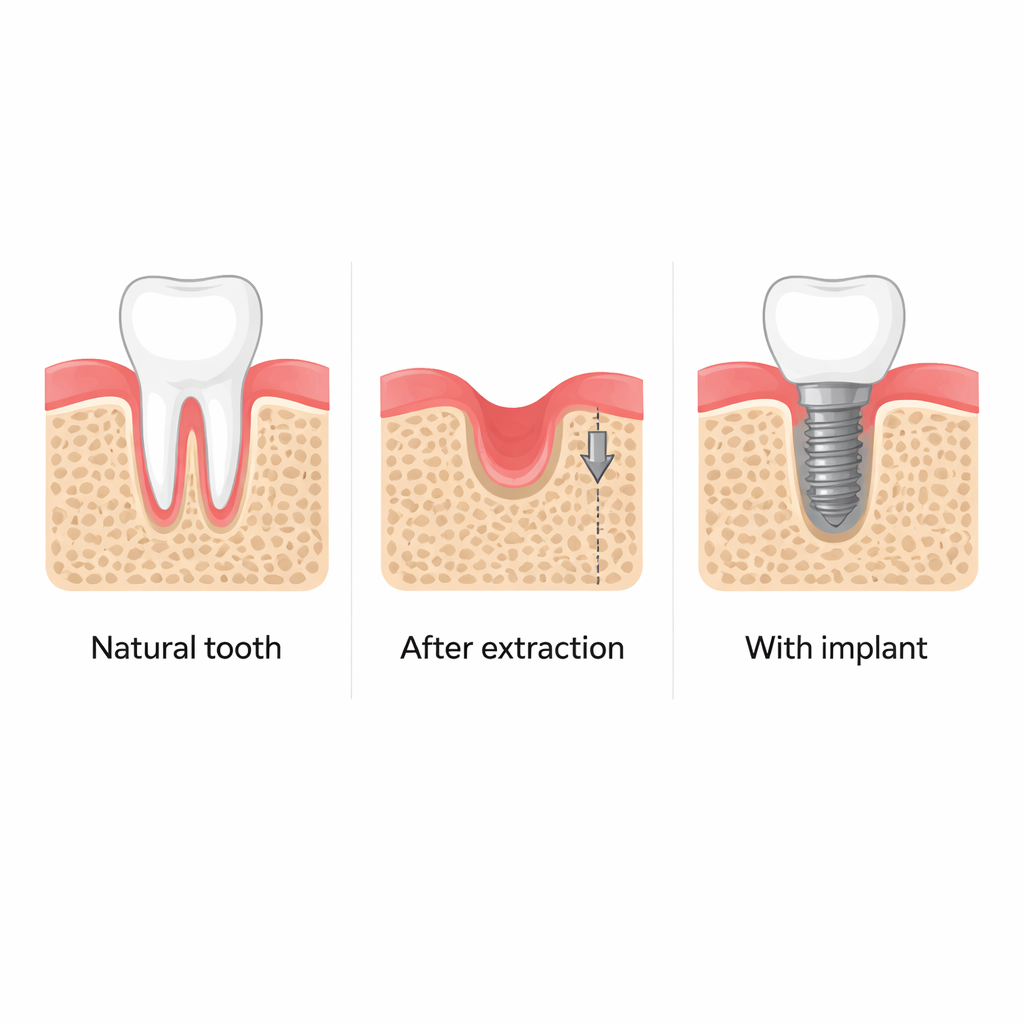
Nach einer Zahnextraktion schrumpft der umgebende Kieferknochen häufig, was die spätere Platzierung stabiler Zahnimplantate erschwert und das Gesichtsprofil beeinflusst. Zahnärzte haben längst beobachtet, dass das Einbringen eines Implantats in eine frische Alveole offenbar hilft, diesen Knochen zu erhalten, und zwar schon bevor das Implantat funktionell belastet wird. Diese Studie stellt eine einfache, aber wichtige Frage: Wie weckt der Akt des Implantierens selbst das Reparatursystem des Knochens, und kann man diesen Prozess gezielt nutzen, um die Regeneration des Kieferknochens zu verbessern?
Implantate als stille Knochenschützer
Klinische Aufnahmen von Patienten und detaillierte Experimente an Mäusen bestätigen, dass die sofortige Platzierung eines Zahnimplantats nach der Extraktion Höhe und Dicke des umgebenden Kieferknochens erhält. Im Gegensatz dazu verlieren frei verheilte Alveolen über mehrere Monate substantiell an Knochenmasse. In der Umgebung von Implantaten fanden die Forschenden mehr unreife knochenbildende Zellen (Osteoprogenitoren), was darauf hindeutet, dass das Gewebe neben der Metallstütze biologisch aktiver ist. Diese erhöhte Aktivität scheint nicht durch Kaubelastung getrieben zu werden, sondern durch die ungewöhnlichen mechanischen Spannungen, die entstehen, wenn ein straff sitzendes Implantat in leicht unterdimensionierten Knochen eingeschraubt wird.
Ein verborgener Schalter in den Knochenstammzellen
Das Team konzentrierte sich auf eine besondere Gruppe von Knochenmarkstammzellen, die durch das Protein LepR markiert sind und als wichtige Lieferanten neuen Knochens im Erwachsenenalter bekannt sind. Durch den Vergleich der Genaktivität dieser Zellen aus normalem Knochen, implantatnahem Knochen und in vitro mechanisch gestressten Zellen identifizierten sie ein Molekül, Sorting nexin 5 (Snx5), dessen Spiegel konsistent abnahmen, wenn mechanische Signale vorhanden waren. In Regionen um Implantate waren LepR‑Zellen mit niedrigem Snx5‑Gehalt eher mit Markern früher knochenbildender Zellen assoziiert, was darauf hindeutet, dass eine Herunterregulierung von Snx5 diese ruhenden Stammzellen in einen aktiven knochenbildenden Zustand treibt.
Wenn der Schalter ausfällt, kann der Knochen Kraft nicht richtig wahrnehmen
Um die Funktion von Snx5 zu prüfen, verwendeten die Forschenden Mäuse und Stammzellen ohne dieses Protein. Ohne Snx5 zeigten die Stammzellen eine ausgeprägte angeborene Neigung zur Knochenbildung, selbst ohne zusätzliche Stimulation. Wenn die Wissenschaftler jedoch mechanische Dehnung anlegten – eine Nachahmung der Belastungen in Implantatnähe – steigerten normale Zellen ihre knochenbildende Aktivität, während Snx5‑defiziente Zellen kaum reagierten. In lebenden Mäusen lösten Implantate in normalen Tieren deutliches neues Knochenwachstum um den Titanpfosten aus. Im Gegensatz dazu gewannen Mäuse ohne Snx5 nach der Implantation keinen zusätzlichen Knochen, was zeigt, dass Snx5 entscheidend dafür ist, mechanische Signale in zusätzliche Knochenreparatur umzusetzen, nicht jedoch für die Basal‑Knochenbildung an sich.
Wie ein Recycling‑Weg Knochen‑Signale steuert
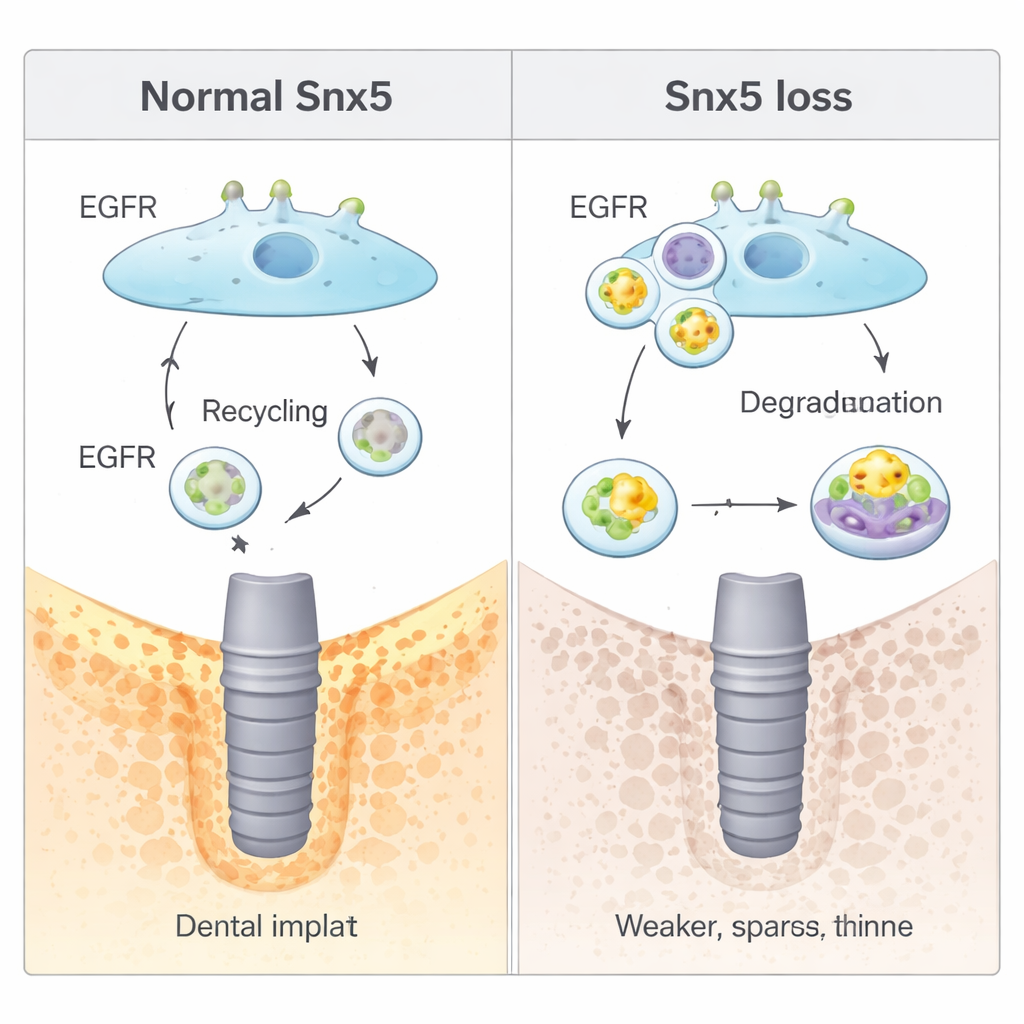
Die Studie deckte anschließend auf, wie Snx5 auf molekularer Ebene wirkt. Viele Wachstumssignale in Zellen laufen über Rezeptoren auf der Zelloberfläche, die ständig internalisiert und entweder recycelt oder abgebaut werden. Snx5 gehört zu einer Familie von „Sortier“‑Proteinen, die diesen Verkehr lenken. Hier zeigte sich, dass Snx5 den epidermalen Wachstumsfaktorrezeptor (EGFR) — einen Schlüsselregulator von Zellwachstum und Knochendifferenzierung — nach der Internalisation wieder zur Zellmembran zurückführt. Fehlt Snx5, wird mehr EGFR in zelluläre „Verdauungs“‑Kompartimente (Lysosomen) umgelenkt und dort abgebaut. Dies reduzierte die EGFR‑Signalgebung, was unerwartet die Basal‑Knochenbildung erhöhte, gleichzeitig aber die Fähigkeit der Zellen verringerte, ihr Verhalten bei veränderten mechanischen Kräften anzupassen. Wirkstoffe, die EGFR künstlich aktivierten, dämpften die vermehrte Knochenbildung ohne Snx5, während Hemmstoffe der lysosomalen Degradation die EGFR‑Signale wiederherstellten und die Knochenbildung erneut reduzierten.
Was das für künftige Implantatpatienten bedeutet
Für Laien legen diese Befunde nahe, dass der Kieferknochen ein eingebautes System besitzt, das das subtile Ziehen und Drücken, das bei der Implantation entsteht, wahrnehmen und in zusätzliches Knochenwachstum übersetzen kann. Snx5 wirkt wie ein Verkehrsregler, der einen wichtigen Wachstumsrezeptor, EGFR, auf einem genau passenden Niveau hält, damit Knochenstammzellen diese mechanischen Hinweise „hören“ und darauf reagieren können. Wenn dieser Regler verändert ist, kann Knochen zwar leichter in Ruhe gebildet werden, verliert jedoch seine fein abgestimmte Reaktion auf mechanische Reize. Das Verständnis dieser Snx5–EGFR‑Achse eröffnet Möglichkeiten für neue Therapien — Medikamente oder Implantatoberflächenbeschichtungen — die die mechanische Sensitivität des Knochens anpassen und so helfen könnten, den Kieferknochen zu erhalten und den Implantaterfolg in schwierigen klinischen Situationen zu verbessern.
Zitation: Jiang, X., Weng, Y., Feng, Y. et al. Implantation awakens peri-implant osteogenic potential via Snx5-EGFR axis-mediated mechanical transduction. Int J Oral Sci 18, 18 (2026). https://doi.org/10.1038/s41368-025-00423-2
Schlüsselwörter: Zahnimplantate, Kieferknochenregeneration, Mechanotransduktion, Knochenstammzellen, EGFR‑Signalgebung