Clear Sky Science · de
KDM6B/Pdk1-glykolysegetriebene ZEB2-Lactylierung fördert die Bildung von zellulärem Zementum
Warum der Schutz der Zahnwurzeln wichtig ist
Parodontalerkrankungen, also Parodontitis, sind eine der Hauptursachen für Zahnverlust bei Erwachsenen. Im Verlauf der Krankheit baut sie still und leise die Gewebe ab, die die Zähne am Kiefer verankern. Eines der wichtigsten dieser Gewebe ist das Zementum, eine dünne, knochenähnliche Schicht, die die Wurzeloberfläche bedeckt und es dem Zahn ermöglicht, über das umgebende Bindegewebe und den Knochen verankert zu bleiben. Geht das Zementum verloren, lockern sich die Zähne und können schließlich ausfallen. Die vorliegende Studie stellt eine einfache, aber wichtige Frage: Können wir im molekularen Detail verstehen, wie Zementum aufgebaut wird, damit man eines Tages dem Körper helfen kann, es wiederherzustellen und Zähne ein Leben lang zu erhalten?
Von zahnstützenden Zellen zu einem therapeutischen Ziel
Zementum wird von spezialisierten Zellen gebildet, den Zementoblasten, die auf der Wurzeloberfläche sitzen und neues Mineral ablagern. Diese Zellen verhalten sich ähnlich wie knochenbildende Zellen, doch die Signale, die ihnen sagen, wann und wie sie Zementum bilden sollen, waren bislang schlecht verstanden. Die Forscher konzentrierten sich auf ein Molekül namens KDM6B, ein Enzym, das chemische Markierungen an DNA-verpackenden Proteinen verändert und Gene aktivieren kann. An Hand von Mauszähnen verschiedenen Alters und im Labor gezüchteten Zementoblasten zeigten sie, dass die KDM6B-Spiegel während der aktiven Phase der Zementumbildung ansteigen und nachlassen, wenn das Wachstum abklingt. Wird KDM6B in Zellen oder in Mäusen blockiert, sinkt die Aktivität der Zementoblasten und der „zelluläre“ Anteil des Zementums – der dickere, lebende Bereich nahe der Wurzelspitze – wird dünner. Das deutet darauf hin, dass KDM6B ein zentraler Förderer gesunden Zementumwachstums ist.
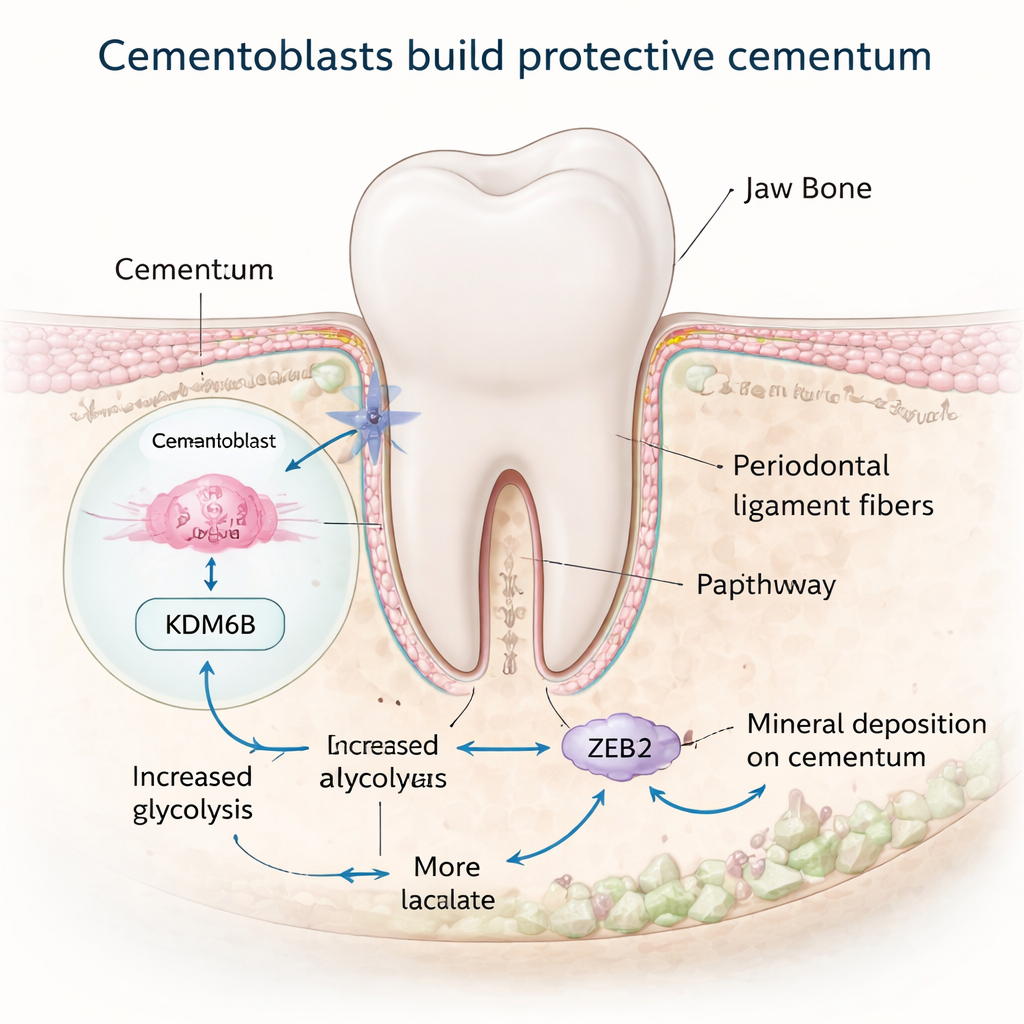
Den Zellstoffwechsel umbauen, um Mineral zu bilden
Der Aufbau mineralisierter Gewebe erfordert viel Energie, und viele Zellen schalten während dieser Arbeit ihren Stoffwechsel in einen besonders aktiven Modus. Das Team entdeckte, dass KDM6B Zementoblasten dabei hilft, ihre Zuckerstoffwechselwege umzuschalten. Normalerweise bevorzugen diese Zellen einen Weg namens Glykolyse, der Glukose schnell abbaut und Lactat produziert. Wenn KDM6B reduziert wurde, wurden Gene, die an der Glykolyse beteiligt sind, herunterreguliert, während Gene für langsamere, sauerstoffabhängige Energiegewinnung teils unverändert oder erhöht waren, und die Zellen produzierten insgesamt weniger Energie. Ein zentraler Akteur in dieser Verschiebung war das Enzym PDK1. Mit Genomkartierungswerkzeugen zeigten die Forscher, dass KDM6B physisch eine repressive Markierung aus dem DNA-Bereich entfernt, der das Pdk1-Gen kontrolliert, sodass PDK1-Spiegel ansteigen können. Die Wiederherstellung von PDK1 in KDM6B-defizienten Zellen brachte viele Marker der Mineralbildung zurück und offenbarte einen KDM6B–PDK1-Stoffwechselschalter, der Zementoblasten antreibt.
Lactat vom Abfallprodukt zum nützlichen Signal machen
Lactat gilt oft als Abfallprodukt mühevoll arbeitender Muskeln, aber neuere Arbeiten zeigen, dass es auch als Signal dienen kann, das Proteine modifiziert. Hier erhöhte die durch KDM6B und PDK1 gesteigerte Glykolyse die Lactatproduktion in Zementoblasten. Die Forscher verfolgten eine neue Art der Proteinmodifikation, die Lactylierung, bei der von Lactat abgeleitete Gruppen an bestimmte Proteinstellen angehängt werden. Sie fanden, dass die Lactylierungsniveaus in Zementoblasten während Phasen aktiver Zementumbildung stiegen und bei älteren Mäusen sowie in KDM6B-defizienten Zellen abnahmen. Die Zugabe von einfachem Natriumlactat steigerte die Lactylierung, reaktivierte mineralbezogene Gene und stellte die Bildung mineraler Knötchen sowohl in kultivierten Zellen als auch in einem Mausmodell wieder her, selbst wenn KDM6B blockiert war. Das legt nahe, dass Lactat selbst geschwächte zementumbildende Aktivitäten teilweise retten kann.
Ein molekularer Schub für einen Schlüsselregulator des Zementums
Das Team fragte dann, welche Proteine durch Lactylierung „dekoriert“ werden und dabei für das Zementum eine Rolle spielen. Sie konzentrierten sich auf ZEB2, ein Transkriptionsregulator, der bereits dafür bekannt ist, die Mineralisierung der Zementoblasten zu fördern. Mit Proteinkartierungstechniken identifizierten sie spezifische Stellen auf ZEB2, die Lactylierungsmarken tragen, und zeigten, dass die Veränderung einer kritischen Stelle die Fähigkeit der Zelle schwächte, Mineralbildungs‑Gene zu aktivieren. Weitere Experimente demonstrierten, dass der KDM6B–PDK1-Weg die ZEB2-Lactylierung fördert und dass zusätzliche Lactatzufuhr ZEB2-Aktivität wiederherstellen kann, wenn PDK1 niedrig ist. Im Kern sind Stoffwechsel und Genregulation verknüpft: Zuckerabbau treibt die Lactatproduktion an, und Lactat justiert ZEB2 so, dass Programme zur Zementum‑Bildung kräftig weiterlaufen.
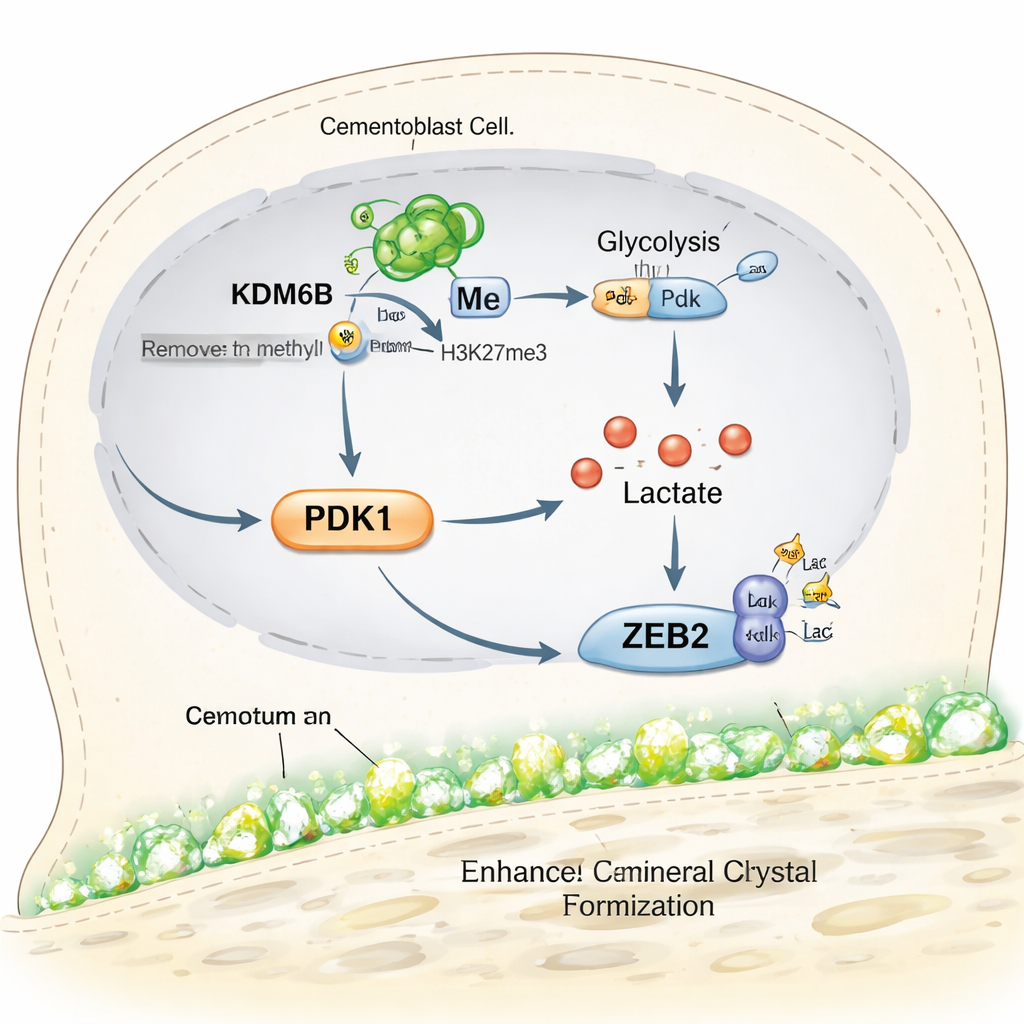
Was das für künftige zahnrettende Therapien bedeutet
Kurz gesagt offenbart die Studie eine Ereigniskette in zementum‑bildenden Zellen: Das Enzym KDM6B öffnet das Pdk1-Gen, PDK1 treibt die Zellen zu schneller Zuckerverwertung, dieser Stoffwechsel erzeugt Lactat, und Lactat stimmt das Protein ZEB2 chemisch so ab, dass Mineralablagerung gefördert wird. Wenn ein Schritt in dieser Kette blockiert ist, schwächelt das Zementumwachstum, doch durch gezielte Zugabe von Lactat lässt sich dies teilweise kompensieren. Für Patienten bedeutet das noch keine sofortige klinische Therapie, aber die Arbeit hebt neue, präzise Ziele für Medikamente oder Biomaterialien hervor, die darauf abzielen, Zementum zu regenerieren und Zähne bei fortgeschrittener Parodontitis zu stabilisieren. Zudem deutet sie darauf hin, dass ähnliche metabolische „Schalter“ genutzt werden könnten, um Knochenheilung an anderen Stellen des Körpers zu fördern.
Zitation: Yang, Z., Wang, H., Xiao, J. et al. KDM6B/Pdk1 glycolytic pathway-driven ZEB2 lactylation promotes cellular cementum formation. Int J Oral Sci 18, 21 (2026). https://doi.org/10.1038/s41368-025-00420-5
Schlüsselwörter: Zementumregeneration, Parodontitis, Zementoblaststoffwechsel, Histondemethylase KDM6B, Proteinlactylierung