Clear Sky Science · de
Strukturelle Einblicke in krankheitsassoziierte Mutationen der microRNA‑Verarbeitungsmaschinerie
Wie winzige RNA‑Scheren Gesundheit und Krankheit formen
In jeder Zelle gibt es ein verborgenes Bearbeitungssystem, das genetische Botschaften zuschneidet, bevor sie gelesen werden. Dieses System beruht auf winzigen RNA‑Stückchen, den microRNAs, die wie Feinabstimmregler für Tausende von Genen gleichzeitig wirken. Arbeiten die molekularen „Maschinen“, die microRNAs herstellen, korrekt, wachsen, teilen und differenzieren sich Zellen kontrolliert. Werden diese Maschinen durch Mutationen beschädigt, kann das Gleichgewicht der Genaktivität in Richtung Krebs, Blutkrankheiten oder Störungen der Hirnentwicklung kippen. Dieser Artikel erklärt, wie das Verständnis der 3‑D‑Formen dieser Maschinen Wissenschaftlern hilft, zu erkennen, was schiefläuft und wie man es möglicherweise beheben kann.
Das Gen‑Dämpfungswerkzeug der Zelle
MicroRNAs sind kurze RNA‑Abschnitte von etwa 22 Bausteinen Länge, die selbst keine Proteine kodieren. Stattdessen heften sie sich an längere Boten‑RNAs und markieren diese entweder zur Zerstörung oder blockieren ihre Translation, wodurch Gene heruntergeregelt, nicht komplett ausgeschaltet werden. Zur Herstellung dieser microRNAs passieren längere RNA‑Vorläufer eine sorgfältig gestufte Produktionslinie. Zuerst schneidet das Enzym DROSHA im Zellkern sperrige Primärtranskripte zu kürzeren, haarnadelartigen Stücken. Diese gelangen dann ins Zytoplasma, wo ein weiteres Enzym, DICER, sie mit einer Messung auf microRNA‑Größe zuschneidet. Schließlich wird ein Strang jedes Duplexes in ein Protein namens Argonaute 2 (AGO2) geladen, das die microRNA als Führungsripple verwendet, um passende Botschaften zu finden und zu stillen. 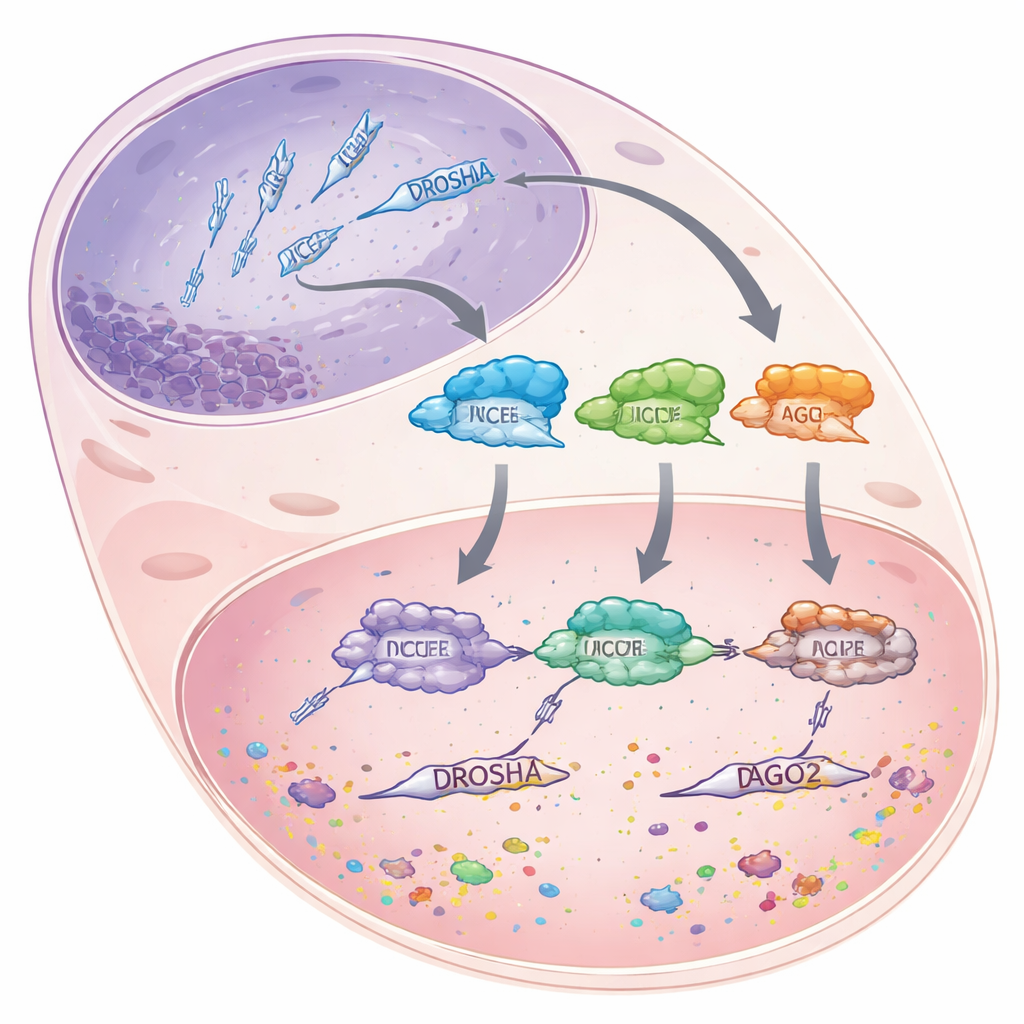
Zarte Formen mit präzisen Aufgaben
DROSHA, DICER und AGO2 sind keine einfachen Scheren; jedes ist aus mehreren miteinander interagierenden Teilen aufgebaut, die sich choreografiert bewegen müssen. DROSHA arbeitet mit einem Partnerprotein, DGCR8, zusammen, um die Enden eines primären microRNA‑Haarnadelmotivs zu greifen und genau zu bestimmen, wo geschnitten wird. DICER verwendet eine Art eingebauten Zollstock, gebildet durch seine Domänen, um einen festen Abstand zwischen der Stelle, an der es das Haarnadelelement hält, und dem katalytischen Zentrum festzulegen. AGO2 umschließt einen einzelnen microRNA‑Strang so, dass dessen „Seed“-Region perfekt exponiert ist, um Zielbotschaften zu erkennen, während Metallionen und Schlüsselaminosäuren im Kern ausgerichtet sind, um diese Ziele zu zerschneiden, wenn die Paarung stark genug ist. Bei allen drei Proteinen leiten positiv geladene Rinnen und flexible Verknüpfungen die RNA‑Stränge an ihren Platz, während metallbindende Taschen und katalytische Reste die chemischen Schnitte ausführen.
Wenn die Scheren verbogen oder abgestumpft sind
Genetische Untersuchungen bei Patienten mit Krebs, Blutkrankheiten und neuroentwicklungsbedingten Syndromen haben Mutationshäufungen in diesen microRNA‑Maschinen aufgedeckt. Viele der schädlichsten Veränderungen liegen direkt in katalytischen Zentren oder an engen RNA‑Greifflächen. Bei DROSHA beispielsweise sitzen Substitutionen wie E1147K und D1219G im Zentrum der Schnittstelle und stören die Fähigkeit, essentielle Metallionen zu halten, sodass das Enzym Primär‑microRNAs nicht mehr verarbeiten kann. Andere DROSHA‑Mutationen, wie Trunkierungen, die die Schnittregion entfernen, oder Veränderungen, die stützende Helices destabilisieren, schwächen den gesamten Komplex und führen zu globalen Abnahmen der microRNA‑Spiegel bei Wilms‑Tumor, Erkrankungen des Knochenmarks und Nervenkrankheiten. Bei DICER häufen sich wiederkehrende Mutationen in einer seiner beiden Schnittdomänen und verzerren die Produktion so, dass ein Arm des microRNA‑Duplexes verloren geht, wodurch sich das Gleichgewicht zwischen wachstumsfördernden und wachstumssuppressiven Signalen verschiebt. 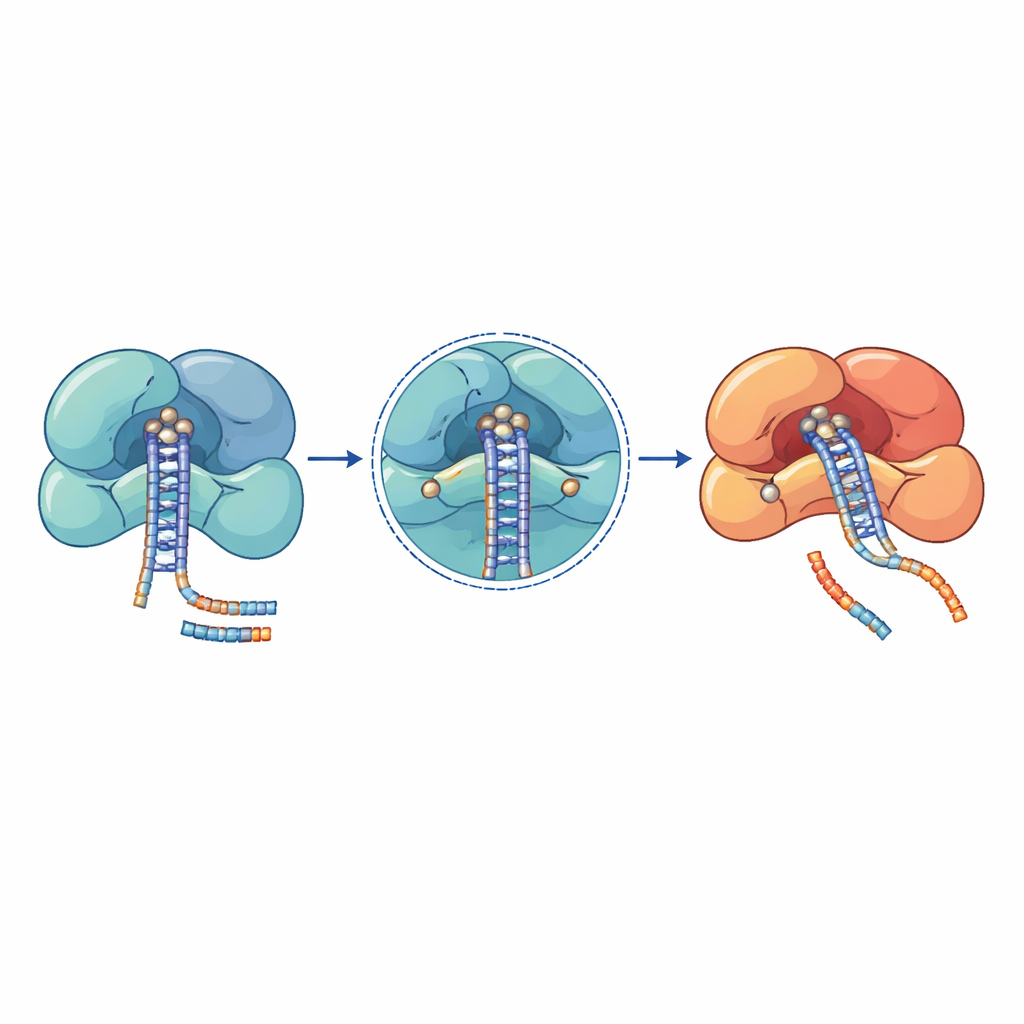
Fehlausgerichtete Führungen im Gehirn und darüber hinaus
AGO2‑Mutationen erzählen eine andere, aber verwandte Geschichte. Direkte Treffer am katalytischen Kern sind selten, vermutlich weil sie in der frühen Entwicklung tödlich wären. Stattdessen treten krankheitsassoziierte Varianten häufiger in flexiblen Verbindungsregionen und an Domain‑Schnittstellen auf, die die Form von AGO2 zusammenhalten. Beim Lessel–Kreienkamp‑Syndrom, einer neuroentwicklungsbedingten Erkrankung, verdrehen Mutationen in diesen Linkern und den umgebenden Oberflächen subtil, wie die PAZ‑, MID‑ und PIWI‑Teile von AGO2 sich packen und bewegen. Das kann die Ausrichtung der guide‑microRNA stören oder deren Bindung an Ziel‑RNAs schwächen und so die Präzision der Genstilllegung während der Gehirnentwicklung verwischen. Ähnliche strukturelle Änderungen an irgendeiner Stelle des microRNA‑Wegs – sei es in DROSHA, DICER oder AGO2 – können sich nach außen fortpflanzen und ganze Genetzwerke beeinflussen, die an Zellwachstum, Blutbildung oder neuronaler Verkabelung beteiligt sind.
Strukturelle Hinweise in zukünftige Therapien übersetzen
Indem Forscher krankheitsbedingte Mutationen auf hochauflösende 3‑D‑Karten dieser Proteine projizieren, können sie genau kategorisieren, wie jede Änderung Schaden anrichtet – sei es durch Abstumpfen der Schneide, Lockerung kritischer Kontakte mit Partnerproteinen oder Durchbiegen wichtiger Helices aus der Ausrichtung. Diese strukturellen Erkenntnisse eröffnen Wege zu gezielten Interventionen: kleine Moleküle, die geschwächte Schnittstellen stabilisieren, designte RNAs, die teilweise funktionelle Enzyme wieder auf die richtigen Substrate lenken, oder allosterische Verbindungen, die mutierte Proteine in aktivere Konformationen schubsen. Für den nichtfachlichen Leser ist die Kernaussage: winzige strukturelle Änderungen an den RNA‑Scheren der Zelle können überproportionale Auswirkungen auf die Gesundheit haben, bieten aber auch präzise Ansatzpunkte für die Entwicklung einer neuen Generation mutation‑bewusster Therapien.
Zitation: Lee, H., Lee, J. & Roh, SH. Structural insights into disease-associated mutations in the microRNA processing machinery. Exp Mol Med 58, 639–649 (2026). https://doi.org/10.1038/s12276-026-01669-4
Schlüsselwörter: microRNA, RNA‑Interferenz, DROSHA DICER AGO2, Krebsgenetik, neuroentwicklungsstörungen