Clear Sky Science · de
Regulatorische Mechanismen der Stabilität des Snail-Proteins: Ubiquitin‑Proteasom‑System und chaperonvermittelte Autophagie
Warum die Ausbreitung von Krebs von einem zerbrechlichen Protein abhängt
Krebs wird wirklich lebensbedrohlich, wenn Zellen sich vom ursprünglichen Tumor lösen und in entfernte Organe gelangen. Diese Ausbreitung, die Metastasierung, hängt teilweise von einem mächtigen „Master‑Schalter“ namens Snail ab, der Zellen dabei hilft, ihre Verbindungen zu lockern und mobiler zu werden. Dieser Artikel erklärt, wie unsere Zellen Snail normalerweise kurz halten, indem sie es rasch über zwei große Entsorgungssysteme abbauen. Das Verständnis dieses Gleichgewichts eröffnet neue Ansätze, um Metastasen zu verlangsamen oder zu verhindern.
Von dicht gepackten Zellen zu umherziehenden Eindringlingen
In gesunden Geweben bilden Epithelzellen geordnete, ziegelartige Schichten, die an Ort und Stelle bleiben und eng an ihren Nachbarn haften. Damit eine Tumorzelle entkommt, durchläuft sie häufig eine Umstellung, die als Epithel‑Mesenchym‑Transition (EMT) bezeichnet wird, bei der sie ihre engen Kontakte verliert und die Fähigkeit zur Bewegung und Invasion gewinnt. Snail ist ein wichtiger Treiber dieser Umstellung: Im Zellkern schaltet es Gene aus, die die Zell‑Zell‑Adhäsion erhalten, und schaltet Gene an, die Bewegung und Invasion begünstigen. Hohe Snail‑Spiegel sind mit aggressiven Krebsformen und schlechten Patientenverläufen verbunden, daher haben Zellen Mechanismen entwickelt, Snail unter normalen Bedingungen knapp und kurzlebig zu halten.
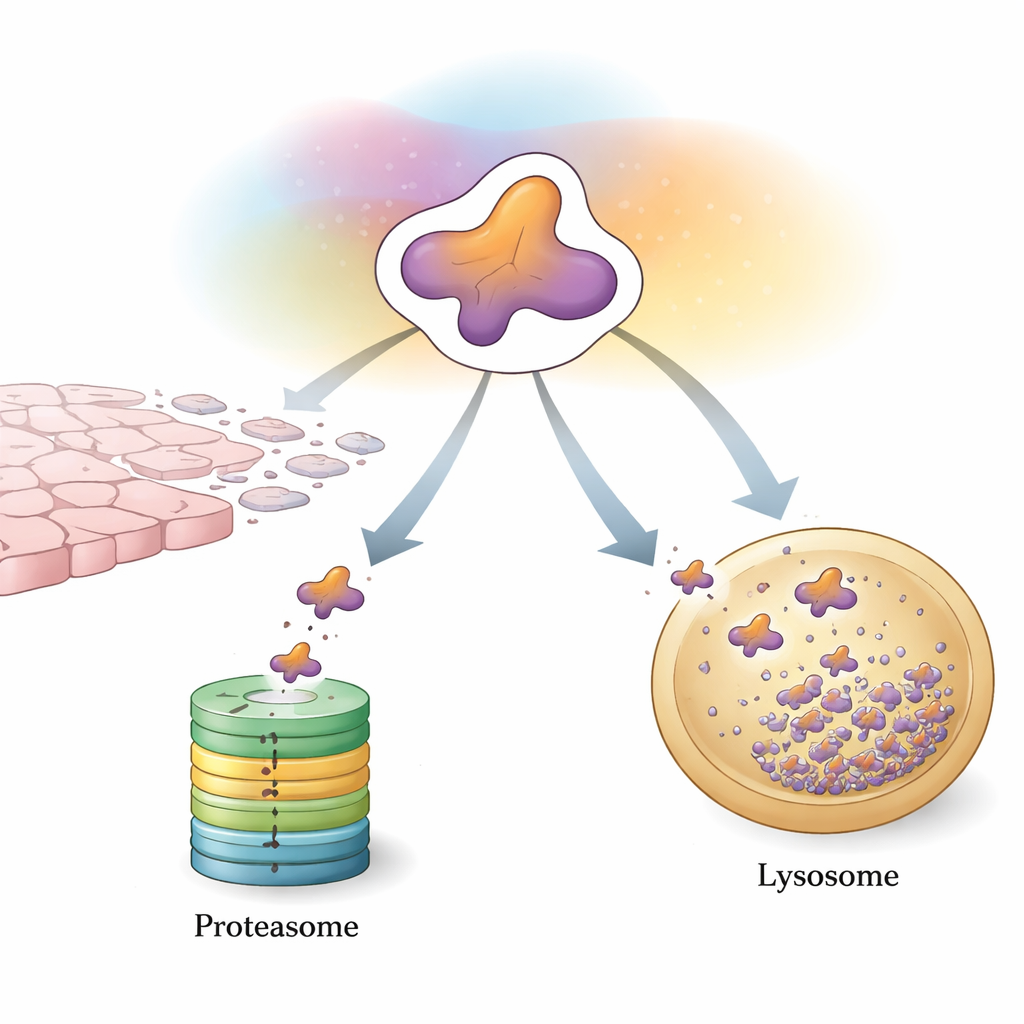
Die erste Kontrolllinie der Zelle: Markieren und zerkleinern
Eine Hauptmethode, mit der Zellen Snail kontrollieren, ist das Ubiquitin‑Proteasom‑System, eine Markier‑und‑Zerkleiner‑Maschine für unerwünschte Proteine. Spezialisierte Enzyme befestigen kleine „Flaggen“ aus dem Protein Ubiquitin an Snail. Wenn sich genügend dieser Flaggen in einem bestimmten Muster ansammeln, wird Snail in das Proteasom gesteuert, einen tonnenförmigen Komplex, der es in Stücke zerlegt. Eine große Anzahl von Hilfsproteinen verfeinert diesen Prozess. Einige Enzyme hängen abbaubegünstigende Ketten an, die Snail schnell zum Schredder schicken und so das Tumorwachstum und die Ausbreitung in Schach halten. Andere fügen Ketten hinzu, die Snail stattdessen stabilisieren oder indirekt seine Genproduktion verstärken und damit das Gleichgewicht zugunsten von EMT und Metastasierung verschieben. Chemische Modifikationen wie Phosphorylierung und Acetylierung wirken wie zusätzliche Schalter, die steuern, welche Helfer an Snail binden können und ob es zerstört oder verschont wird.
Die Bremsen lösen: Enzyme, die Snail retten
Die Geschichte endet nicht mit der Markierung von Snail zur Zerstörung. Eine andere Gruppe von Enzymen, die Deubiquitinylasen, kann die Ubiquitin‑Flaggen entfernen und Snail so vor dem Proteasom retten. Viele dieser Enzyme sind in Krebsen aktiviert oder verstärkt, sodass Snail dem Abbau entkommt und im Zellkern verweilt. Ihre Wirkungen hängen stark vom zellulären Kontext ab: In manchen Situationen stabilisieren sie Snail direkt, in anderen beeinflussen sie dessen zellulären Aufenthaltsort oder wie es mit Partnerproteinen interagiert. Signale aus krebsassoziierten Wegen, etwa Wachstumsfaktoren und Stressreaktionen, fließen in dieses Netzwerk ein und entscheiden, ob Snail rasch entfernt oder zugelassen wird, das EMT‑Programm zu steuern.
Ein zweites Sicherheitsnetz: Selektive Zustellung an das Recyclingzentrum der Zelle
Jenseits des Proteasoms verlassen sich Zellen auf Autophagie, eine Sammlung von Wegen, die Proteine zu sauren Kompartimenten, den Lysosomen, zum Abbau transportieren. Diese Übersicht hebt eine hochselektive Form hervor, die chaperonvermittelte Autophagie (CMA), als zweite wichtige Route zur Kontrolle von Snail. CMA erkennt eine kurze Sequenz innerhalb von Snail und liefert mit Hilfe von Begleitproteinen zytoplasmatisches Snail in die Lysosomen zur Zerstörung. In weniger aggressiven Brustkrebszellen hält dieses System Snail weitgehend außerhalb des Kerns und anfällig für lysosomalen Abbau. In aggressiveren, triple‑negativen Brustkrebserkrankungen dagegen sammelt sich Snail eher im Kern und umgeht CMA, wodurch seine Fähigkeit, EMT und Metastasen auszulösen, gestärkt wird.
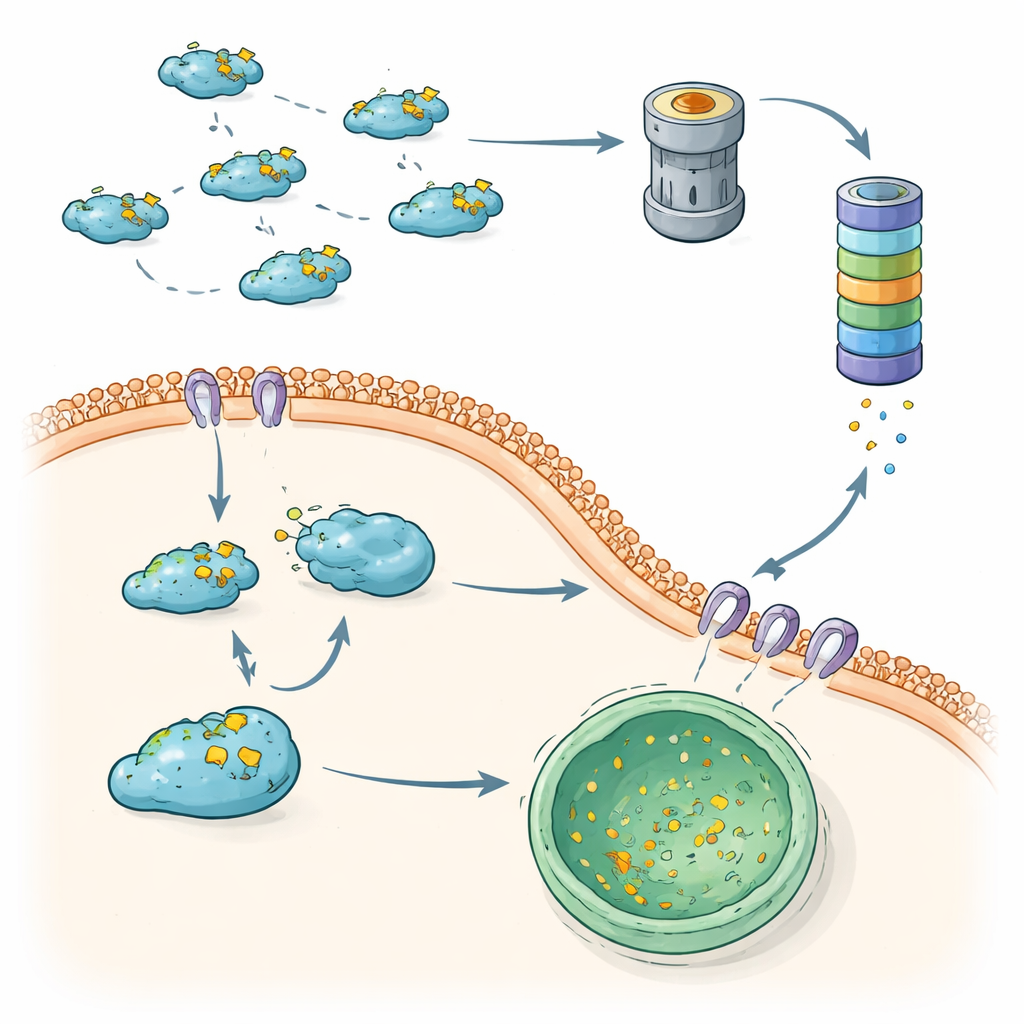
Wenn die Qualitätskontrolle versagt, gewinnt die Metastasierung Terrain
Zusammengefasst zeigen diese Befunde, dass Zellen zwei komplementäre „Qualitätskontroll“-Achsen nutzen, um Snail zu dämpfen: den Ubiquitin‑Proteasom‑Weg und die CMA‑basierte lysosomale Degradation. Wenn beide ordnungsgemäß funktionieren, wird Snail schnell abgebaut, wodurch EMT begrenzt und die Ausbreitung von Tumorzellen verhindert wird. Wenn eine der Achsen geschwächt ist — durch Veränderungen in Markierungsenzymen, Deubiquitinylasen oder CMA‑Komponenten — wird Snail stabiler, sammelt sich im Kern an und fördert stark invasives Verhalten. Durch die Kartierung dieser miteinander verknüpften Abbaurouten skizziert der Artikel neue therapeutische Möglichkeiten: Arzneistoffe, die den Abbau von Snail wiederherstellen oder verstärken oder Snail zurück zur CMA‑ oder proteasomalen Zerstörung lenken, könnten dazu beitragen, die Bremsen der Metastasierung wieder anzulegen, ohne diese essentiellen Protein‑Recycling‑Systeme vollständig abzuschalten.
Zitation: Kim, M., Hong, KS., Kim, T. et al. Regulatory mechanisms for Snail protein stability: ubiquitin–proteasome system and chaperone-mediated autophagy. Exp Mol Med 58, 408–415 (2026). https://doi.org/10.1038/s12276-026-01667-6
Schlüsselwörter: Krebs‑Metastasierung, Epithel‑Mesenchym‑Transition, Snail‑Protein, Proteinabbau, Autophagie