Clear Sky Science · de
Ein transienter Rezeptor potenziell vanilloider 1-abhängiger Hornhaut–Trigeminus-Neuroinflammationskreis fördert Hornhautneuropathie
Empfindliche Augen und anhaltende Schmerzen
Viele Menschen mit trockenen, gereizten Augen sind überrascht zu erfahren, dass ihre schlimmsten Symptome nicht von der Augenoberfläche selbst ausgehen, sondern von den Nerven, die Reizung und Schmerz wahrnehmen. Diese Studie an Mäusen deckt eine verborgene Rückkopplungsschleife zwischen dem Auge und dem sensorischen Zentrum des Gehirns auf, die erklärt, warum Augenschmerzen persistieren können und warum manchmal beide Augen betroffen sind, obwohl nur eines trocken erscheint. Indem sie einen spezifischen molekularen Türsteher in dieser Schleife beschreibt, weist die Arbeit auf neue Ansätze hin, schmerzende Augen zu beruhigen, ohne einfach nur mehr Tränen hinzuzufügen.

Wenn das Alarmsystem des Auges fehlgeht
Das klare vordere Fenster des Auges, die Hornhaut, ist dicht mit Nervenendigungen besetzt, die ständig Feuchtigkeit, Temperatur und die chemische Zusammensetzung der Tränen überwachen. Bei trockener Augenkrankheit sind die Tränen reduziert oder zu salzig, und Patientinnen und Patienten entwickeln häufig Brennen, Stechen oder sogar lähmende Schmerzen. Die Autorinnen und Autoren konzentrierten sich auf einen molekularen Sensor in schmerzleitenden Fasern der Hornhaut namens TRPV1, am besten bekannt als Rezeptor für die Chili‑Verbindung Capsaicin. Dieser Sensor reagiert auf Hitze und auf Signale, die bei Gewebestress freigesetzt werden. Das Team fragte, ob eine Überaktivierung von TRPV1 durch Trockenheit und Schäden nicht nur lokale Reizungen verursachen, sondern auch tiefere Veränderungen in den Nerven bewirken könnte, die das Auge mit dem Gehirn verbinden.
Ein Nerven–Immun-Kreis, der Auge und Gehirn verbindet
Mit Mausmodellen, bei denen die Tränenproduktion chirurgisch reduziert wurde, zeigten die Forschenden, dass trockene Augen TRPV1‑tragende Nervenfasern in der Hornhaut stark aktivieren. Dies verändert wiederum die Genaktivität und das Verhalten des Immunsystems im Trigeminusganglion, einem Nervenknoten, der die Zellkörper der körnigen Sinnesneurone der Hornhaut beherbergt. Bei normalen Mäusen führte Trockenheit dort zu einem Anstieg entzündungs‑ und immunbezogener Gene und veränderte den Zustand benachbarter Makrophagen, Immunzellen, die sensorische Neurone umhüllen. Gleichzeitig zeigten die trockenen Augen aktivierte Immunzellen an der Oberfläche, reduzierte Nervendichte und abnorme Sensitivität: Die Hornhaut reagierte weniger auf mechanische Berührung und auf einige chemische Reize, war jedoch stärker reaktiv gegenüber TRPV1‑Stimulation, was darauf hindeutet, dass dieser bestimmte Sensor sensibilisiert worden war.
Wie ein entzündetes Auge das andere beeinflussen kann
Um direkte Effekte der Trockenheit von entfernteren nervengesteuerten Signalen zu trennen, erzeugte das Team ein "einseitiges" Trockenauge, indem nur die Tränendrüse auf der rechten Seite entfernt wurde. Auffällig blieb das unbehandelte linke Auge normal feucht und behielt eine gesunde Oberflächenbarriere, doch im Laufe der Zeit entwickelte es eine subtile Entzündung und klare Zeichen von Nervendysfunktion — Ausdünnung tieferer Nervenfasern und veränderte Sensitivität — die das geschädigte Auge widerspiegelten, aber verzögert auftraten. Diese kontralateralen Veränderungen hingen von TRPV1 ab: Mäuse, denen dieser Sensor genetisch fehlte, waren sowohl im trockenen als auch im unbehandelten Auge geschützt. RNA‑Sequenzierung der Trigeminusganglien bestätigte, dass einseitige Trockenheit auch auf der gegenüberliegenden Seite ein immun‑ und entzündungsbezogenes Signaturmuster auslöste, was auf einen Hornhaut–Trigeminus–Hornhaut‑Kreislauf hinweist, der Probleme von einem Auge auf das andere übertragen kann.
Der Beweis, dass TRPV1 allein Schäden auslösen kann
Trockenheit ist komplex und aktiviert viele Pfade, daher fragten die Autorinnen und Autoren als Nächstes, ob TRPV1 allein diesen Kreis in Gang setzen könne. Sie applizierten Capsaicin lokal auf die Hornhaut eines Auges und stimulierten so TRPV1, ohne die Oberfläche auszutrocknen. Das behandelte Auge zeigte ausgeprägten Untergang von Hornhautnerven und verringerte Sensitivität, obwohl die epithelialle Barriere intakt blieb. Bemerkenswerterweise entwickelte das unbehandelte Auge erneut einen milderen, aber messbaren Verlust von Nervenendigungen und Veränderungen in der Sensitivität, was bestätigt, dass starke Aktivierung von TRPV1 in einer Hornhaut ausreicht, um Nervenschädigung und funktionelle Veränderungen im Partnerauge über das gemeinsame Trigeminusnetzwerk hervorzurufen. Mäuse ohne T‑ und B‑Lymphozyten zeigten Veränderungen nur im behandelten Auge, was darauf hindeutet, dass für eine vollständige bilaterale Ausbreitung neben der Nervenaktivierung auch eine adaptive Immunantwort erforderlich ist.
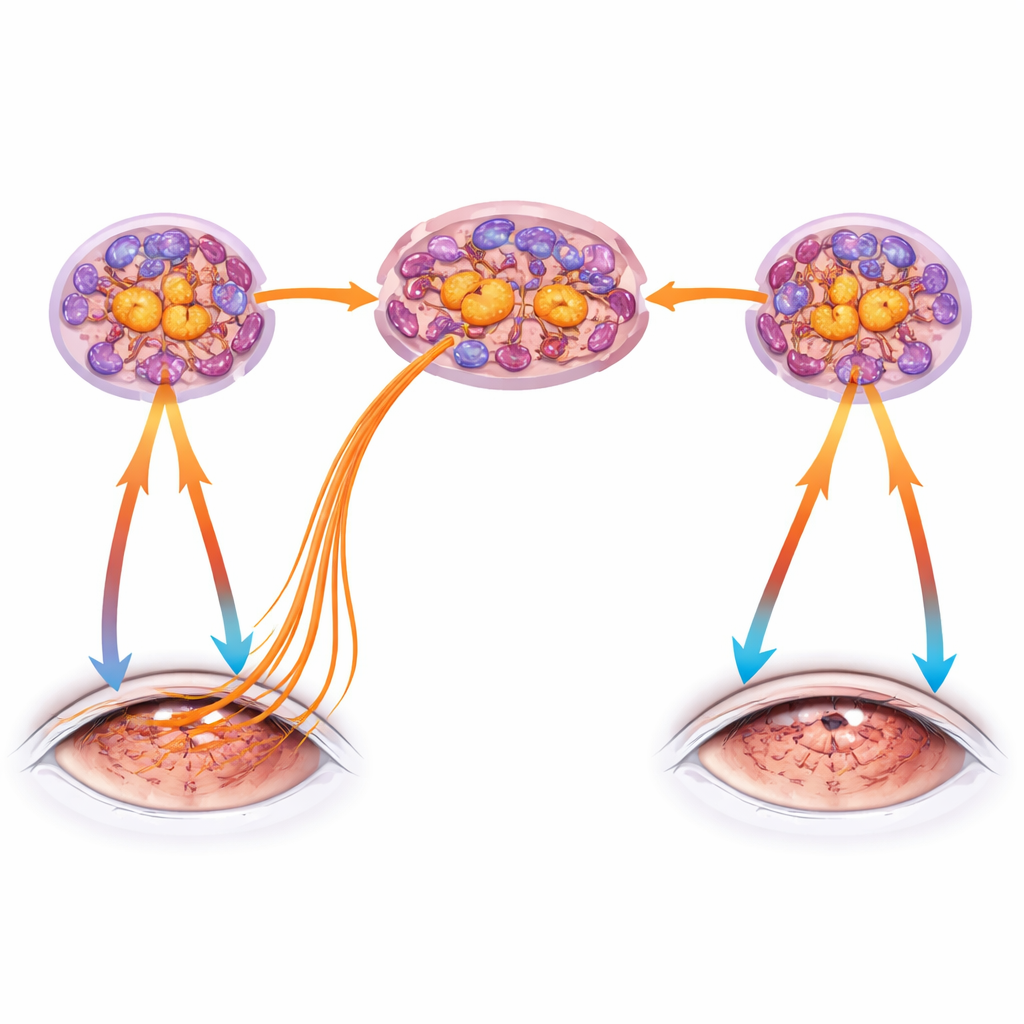
Ein schmerzfördernder Botenstoff und ein möglicher Behandlungsansatz
Die Studie untersuchte auch Substanz P, ein Neuropeptid, das aus aktivierten Schmerzfasern freigesetzt wird, Gewebe zusätzlich entzünden und TRPV1‑Aktivität verstärken kann. Die Blockade von Substanz‑P‑Rezeptoren mittels Augentropfen im nicht‑trockenen Auge einseitiger Trockenaugentiere schädigte die Hornhautoberfläche nicht, verringerte jedoch deutlich den Verlust der Berührungsempfindlichkeit und die gesteigerte Reaktion auf TRPV1‑Stimulation. Vollständig verhinderte sie jedoch nicht den strukturellen Verlust von Nervenendigungen, was unterstreicht, dass mehrere Faktoren zusammenwirken, um Hornhautnerven zu schädigen. Zusammen zeichnen die Ergebnisse einen Teufelskreis: Trockenheit und Verletzung aktivieren TRPV1 in Hornhautnerven, die Gefahrensignale ins Trigeminusganglion senden, Immunzellen dort rekrutieren und umlernen und dann proinflammatorische Nervensignale und die Freisetzung von Neuropeptiden an die Augenoberfläche zurücktreiben, wodurch die Nervendegeneration verschärft und Dysfunktionen zwischen den Augen verbreitet werden.
Was das für Menschen mit trockenen, schmerzenden Augen bedeutet
Für Nicht‑Spezialisten ist die Kernbotschaft, dass die trockene Augenkrankheit nicht nur ein lokales Problem fehlender Tränen ist. Sie umfasst eine sich selbst verstärkende Nerven‑Immun‑Schleife, die die Augenoberfläche mit sensorischen Zentren im Kopf verbindet und zurück. TRPV1 sitzt am Eingangspunkt dieser Schleife und wirkt wie ein überempfindlicher Alarm, der, einmal ausgelöst, Entzündungen und Nervenschädigung aufrechterhält, selbst wenn die ursprüngliche Trockenheit mäßig oder einseitig war. Therapien, die die TRPV1‑Aktivität an Hornhautnerven drosseln oder die nachgeschaltete Botenstoffe wie Substanz P unterbrechen, könnten daher mehr bewirken als nur die Oberfläche zu beruhigen — sie könnten einen tieferen Schmerzkreis durchbrechen und das komplexe Nervennetz schützen, das unsere Augen komfortabel und reaktionsfähig hält.
Zitation: Pizzano, M., Vereertbrugghen, A., Martinez Gomez, M.J. et al. A transient receptor potential vanilloid 1-dependent corneal–trigeminal neuroinflammatory circuit promotes corneal neuropathy. Exp Mol Med 58, 605–621 (2026). https://doi.org/10.1038/s12276-026-01653-y
Schlüsselwörter: Trockene-Augen-Erkrankung, Hornhautnerven, TRPV1, Neuroinflammation, Substanz P