Clear Sky Science · de
Metabolischer Querfunk zwischen tumorassoziierten Fibroblasten, Adipozyten und Immunzellen als Treiber eines immunsuppressiven Tumormikromilieus
Warum die Nachbarschaft des Tumors wichtig ist
Krebs wächst nicht isoliert. Er lebt in einer lebhaften Nachbarschaft aus Stütz‑, Fett‑ und Immunzellen, die fortwährend Nährstoffe und chemische Signale austauschen. Dieser Artikel erklärt, wie der "Stoffwechsel" dieser Nachbarschaft – also die Art, wie Zellen Energie nutzen und teilen – stillschweigend das Kräfteverhältnis zugunsten des Tumors und zuungunsten des Immunsystems verschiebt. Das Verständnis dieser verborgenen Ökonomie von Zuckern, Fetten und Aminosäuren eröffnet neue Wege, Immuntherapien wirksamer zu machen und das Unterstützungssystem des Tumors zu unterbinden.
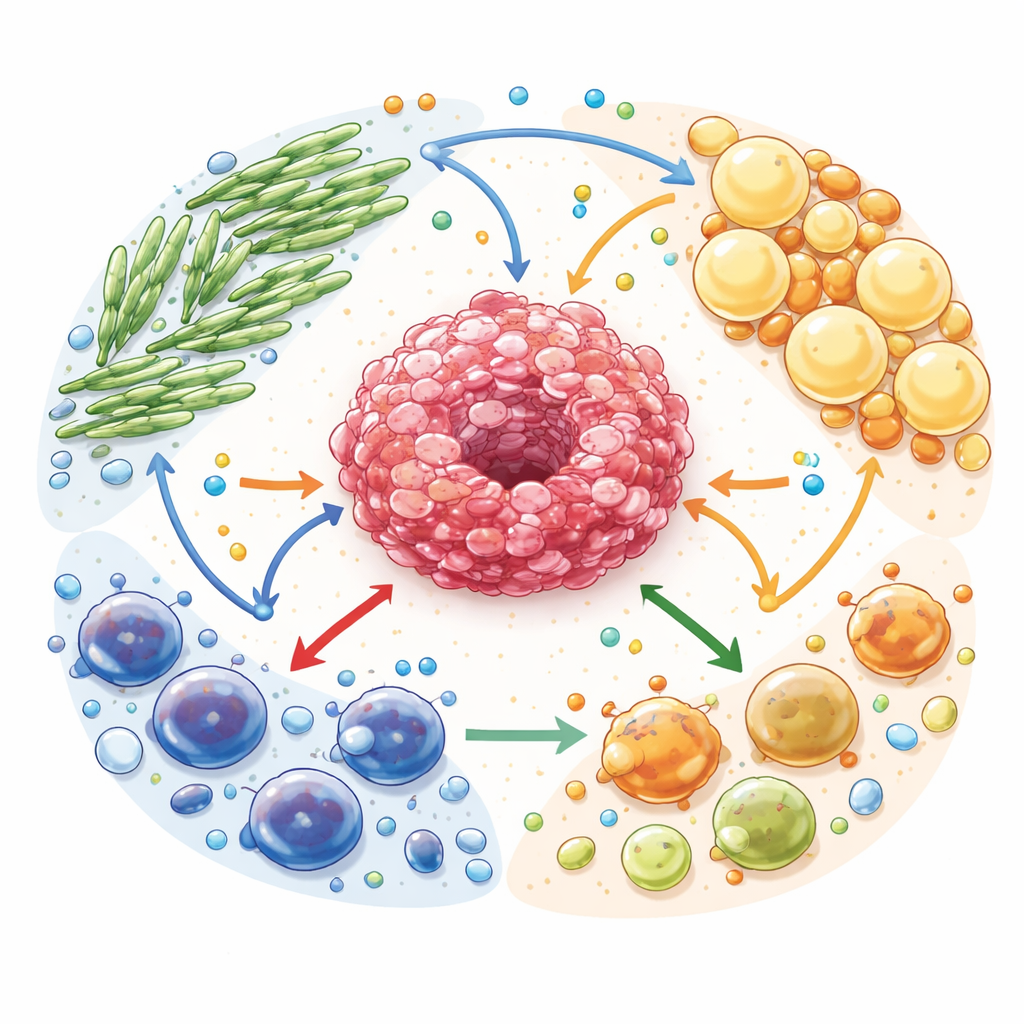
Ressourcenteilung in einem Krebs‑Ökosystem
Die Autoren beschreiben das Tumormikromilieu als ein komplexes Ökosystem. Krebszellen sind umgeben von tumorassoziierten Fibroblasten (narbenähnliche Stützzellen), tumorassoziierten Adipozyten (umprogrammierten Fettzellen) und vielen Typen von Immunzellen. All diese Zellen konkurrieren um und tauschen Brennstoffe wie Glukose, Fettsäuren und Aminosäuren aus. Dieser Handel ist jedoch nicht neutral: Stütz‑ und Nebenzellen werden umprogrammiert, ihre eigenen Reserven aufzubrechen und energiereiche Moleküle zu exportieren, die Krebszellen nähren. Gleichzeitig sammeln sich abfallähnliche Nebenprodukte, darunter Laktat und Adenosin, an und wirken als starke Signale, die schützende Immunzellen schwächen, während sie jene begünstigen, die die Immunantwort dämpfen.
Wie Fettzellen Tumoren helfen und Abwehrkräfte schwächen
Nahegelegene Fettpolster tun weit mehr, als nur Kalorien zu speichern. Unter dem Einfluss von Tumorsignalen und Sauerstoffmangel verwandeln sich normale Fettzellen in tumorassoziierte Adipozyten. Sie verkleinern ihre Fetttropfen, erhöhen den Fettabbau und geben freie Fettsäuren, entzündungsfördernde Moleküle und kleine vesikelartige Ladungen ab. Krebszellen nehmen diese Fette gierig auf und verbrennen sie in ihren Mitochondrien, wodurch sie eine flexible, lang anhaltende Energiequelle gewinnen, die ihnen hilft, Stress zu überstehen, zu metastasieren und Therapien zu widerstehen. Immunzellen in fettreichen Regionen haben weniger Glück: zytotoxische T‑Zellen und natürliche Killerzellen überladen sich mit Lipiden, erleiden oxidativen Stress und geraten in einen „erschöpften“ Zustand mit verminderter Fähigkeit, Tumorzellen zu zerstören. Dagegen gedeihen regulatorische T‑Zellen und bestimmte myeloide Zellen auf diesen Lipiden, werden unterdrückender und dämpfen die Immunantwort weiter.
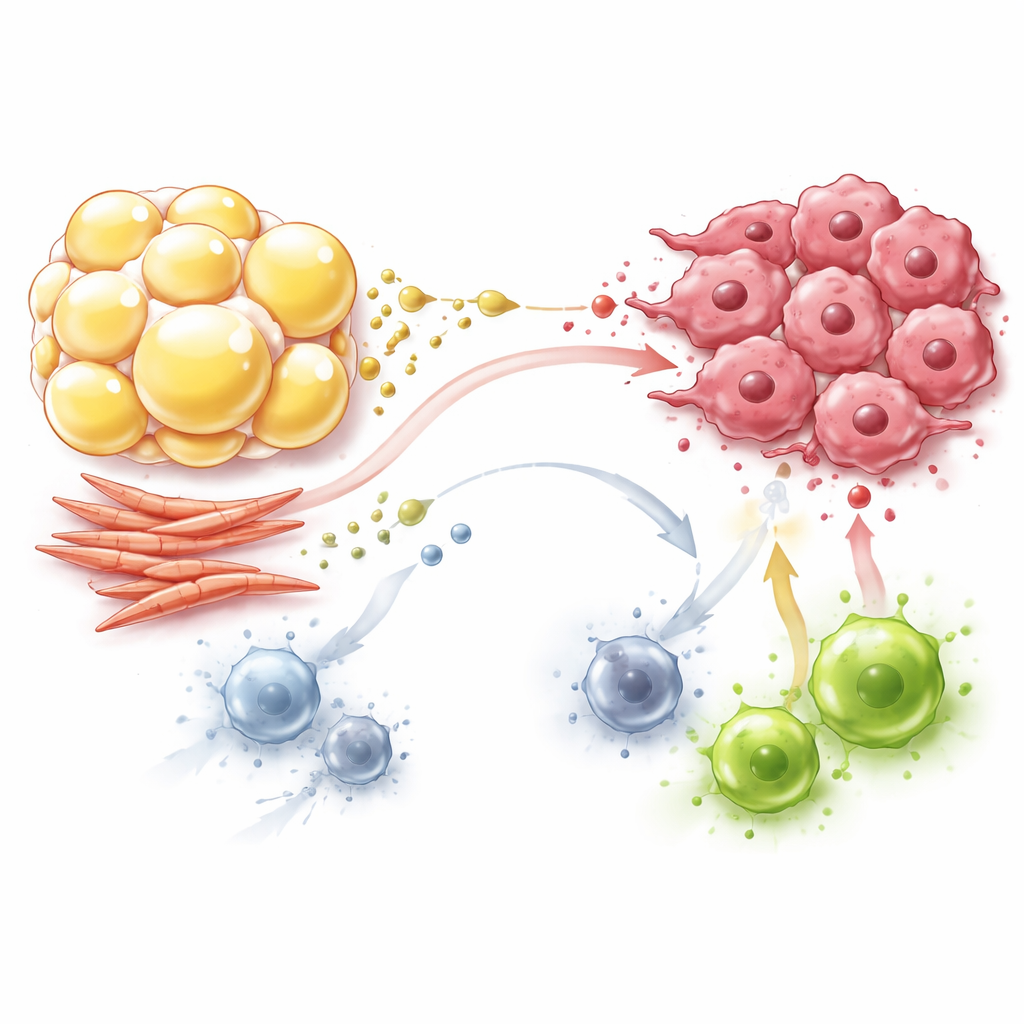
Fibroblasten: Baumeister, die auch den Stoffwechsel umlenken
Fibroblasten, lange bekannt als Baumeister narbenähnlichen Gewebes um Tumoren, spielen auch in diesem metabolischen Drama eine aktive Rolle. Tumorassoziierte Fibroblasten verlagern ihr Verhalten in eine zuckergierige Richtung und wandeln große Mengen Glukose in Laktat und Pyruvat um, selbst wenn ausreichend Sauerstoff vorhanden ist. Sie exportieren diese Produkte in den umgebenden Raum, wo Krebszellen sie als Brennstoff für ihre eigenen Kraftwerke wiederverwenden und so Glukose für Wachstum sparen. Fibroblasten stellen außerdem Aminosäuren wie Glutamin, Prolin und Asparagin her und tauschen sie aus, was sowohl die Struktur des Tumors als auch sein Wachstum unter Nährstoffstress unterstützt. Gleichzeitig verbrauchen Fibroblasten wichtige Nährstoffe und geben Laktat frei, wodurch Effektorzellen, die auf Glukose angewiesen sind, verdrängt werden und Makrophagen sowie T‑Zellen in tolerantere, weniger aggressive Zustände gedrängt werden.
Immunzellen in einer metabolischen Falle
Das Immunsystem im Tumor wird ebenso stark von der Verfügbarkeit von Brennstoffen geprägt wie von Antigenen. Zytotoxische T‑Zellen und natürliche Killerzellen, die für ihren Angriff schnelle Zuckerverbrennung benötigen, finden sich in einer Landschaft wieder, der Glukose entzogen und die mit Laktat, Fetten und anderen unterdrückenden Metaboliten überschwemmt ist. Ihre Energiesysteme stottern, ihre Mitochondrien werden geschädigt und inhibitorische „Bremsen“ auf ihrer Oberfläche nehmen zu. Unterdessen sind regulatorische T‑Zellen und tumorassoziierte Makrophagen gut an diese raue Umgebung angepasst. Sie bevorzugen Fettverbrennung und oxidative Stoffwechselwege, was ihnen erlaubt, dort zu gedeihen, wo andere versagen. Unterstützt von Fibroblasten und Adipozyten verstärken diese Zellen einen toleranten, wundheilungsähnlichen Zustand, der den Tumor schützt und die Wirkung von Checkpoint‑Inhibitoren und anderen Immuntherapien abschwächt.
Den Stoffwechsel als therapeutisches Ziel nutzen
Das Review hebt ein wachsendes Arsenal experimenteller Wirkstoffe hervor, die darauf abzielen, dieses Unterstützungsnetzwerk zu stören, ohne einfach nur teilende Zellen zu vergiften. Manche Ansätze versuchen, die Fettfreisetzung aus Adipozyten oder die Fettaufnahme und -verwertung in Krebszellen zu blockieren. Andere zielen auf fibroblastengetriebene Wege, die Laktat erzeugen, die extrazelluläre Matrix umgestalten oder suppressive myeloide Zellen anziehen. Durch die Senkung von Laktatspiegeln, das Blockieren spezifischer Brennstofftransporter oder das Umpolen lipid‑sensitiver Schaltstellen in Zellen wollen diese Strategien wieder Glukosezugang und mitochondriale Gesundheit für erschöpfte T‑ und natürliche Killerzellen herstellen. Das übergeordnete Ziel ist nicht nur, den Tumor auszuhungern, sondern seine Nachbarschaft so „umzubilden“, dass Immunzellen Tumorzellen wieder erkennen, erreichen und wirksam angreifen können.
Zitation: Kim, T.H., Lim, S.H., Lee, H. et al. Metabolic crosstalk among cancer-associated fibroblasts, adipocytes and immune cells as an immunosuppressive tumor microenvironment driver. Exp Mol Med 58, 366–381 (2026). https://doi.org/10.1038/s12276-026-01650-1
Schlüsselwörter: Tumormikromilieu, Krebsstoffwechsel, tumorassoziierte Fibroblasten, tumorassoziierte Adipozyten, Tumorimmunsuppression