Clear Sky Science · de
Der Mangel an Exocyst-Komponentenprotein Exoc5 verschärft den Verlauf der Nierenfibrose
Warum Narben in der Niere wichtig sind
Chronische Nierenerkrankungen betreffen weltweit Hunderte Millionen Menschen. Ein wesentlicher Grund für ihr Fortschreiten ist Fibrose — Narbengewebe, das nach und nach funktionierendes Nierengewebe ersetzt. Diese Studie untersucht eine weniger bekannte zelluläre Maschine, das Exocyst, und eines ihrer Bauteile namens Exoc5, mit einer praktischen Fragestellung: Hilft dieses Protein den Nieren, nach einer Verletzung sauber zu heilen, oder treibt es sie zur Vernarbung und zum Versagen?
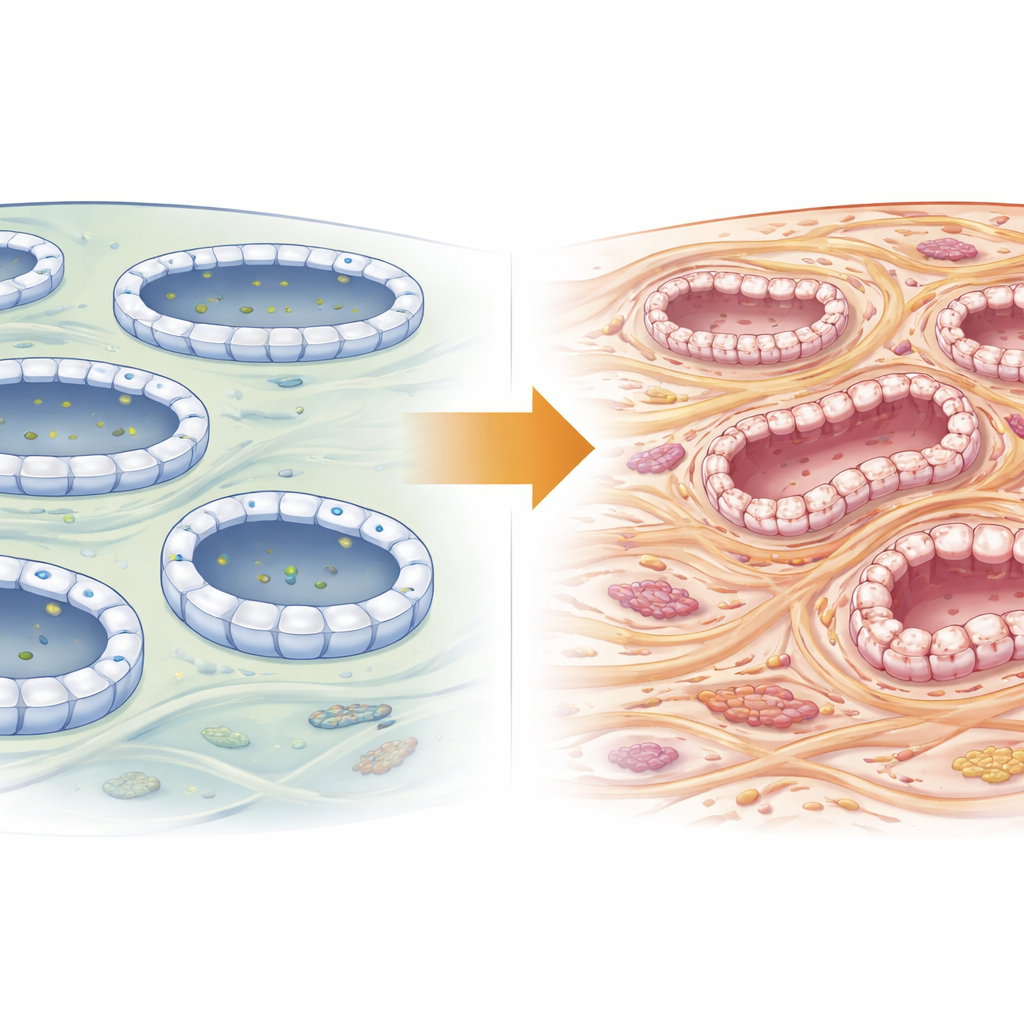
Ein zelluläres Versandzentrum in Nierenzellen
Jede Tubuluszelle in der Niere ist ein geschäftiges Logistikzentrum und transportiert ständig winzige, mit Fracht gefüllte Bläschen zu exakt definierten Stellen an ihrer Oberfläche. Dieser Verkehr wird vom Exocyst organisiert, einem achtteiligen Andockkomplex. Exoc5 sitzt im Zentrum dieser Maschine und vermittelt zwischen von innen kommenden Frachtkörnern und den Andockstellen an der Außenmembran. Frühere Arbeiten zeigten, dass eine Störung von Exoc5 verschiedene Organe schädigt und dass es den Tubuluszellen der Niere hilft, ihre enge, geordnete Struktur zu bewahren. Da eine gestörte Struktur ein Kennzeichen der Fibrose ist, vermuteten die Autorinnen und Autoren, dass Exoc5 stillschweigend mitentscheidet, ob verletzte Nieren sich erholen oder vernarben.
Untersuchung der Rolle von Exoc5 in Mäusen
Die Forschenden erzeugten Mäuse, bei denen Exoc5 nur in proximalen Tubuluszellen gelöscht wurde — den Abschnitten, die den Großteil der Filter- und Rückgewinnungsarbeit der Niere leisten. Überraschenderweise wuchsen diese Tiere normal und zeigten unter Alltagsbedingungen normale Nierenstruktur, korrekte Verteilung von Transportern und normale Funktion. Um eine starke, lokal begrenzte Verletzung nachzuahmen, die oft zur Vernarbung führt, verschlossen die Forschenden ein Harnleiter — ein Standardverfahren, das innerhalb einer Woche zu Druckaufbau, Entzündung und Fibrose in der betroffenen Niere führt. Sowohl bei normalen als auch bei Exoc5-defizienten Mäusen verringerte dieser Verschluss die Exoc5-Spiegel, doch die Knockout-Tiere entwickelten deutlich stärkere Rückbildung der Tubuli, vermehrte Kollagenablagerungen und stärkere Infiltration durch entzündungsassoziierte Zellen.
Von geordneten Röhren zu wandernden Zellen
Gesunde Tubuluszellen sind eng miteinander verbunden und weisen klar definierte Ober- und Unterseiten auf. Bei Fibrose durchlaufen sie oft eine „Epithel-zu-Mesenchym-Transition“ (EMT), einen Wechsel von einem verankerten, blattartigen Zustand zu einem beweglicheren, faserbildenden Zustand. Die Autorinnen und Autoren fanden, dass nach der Obstruktion die Nieren ohne Exoc5 eine stärkere Aktivierung zentraler EMT-Treiber und höhere Spiegel von Proteinen aufwiesen, die typisch für wandernde, Faser produzierende Zellen sind, sowie einen ausgeprägteren Verlust von Junction-Proteinen, die normalerweise die Polarität der Tubuluszellen bewahren. Außerdem beobachteten sie das Wiederauftreten von Pax2, einem Entwicklungsregulator, der normalerweise ausgeschaltet wird, sobald sich Tubuli ausgereift haben. Pax2 kehrte in den Exoc5-defizienten Tubuli stärker zurück, insbesondere in gestressten Zellen, die sich nicht erfolgreich teilten, was darauf hindeutet, dass der Verlust von Exoc5 Zellen in einen halb reparierten, dedifferenzierten Zustand treibt, der zur Vernarbung neigt.
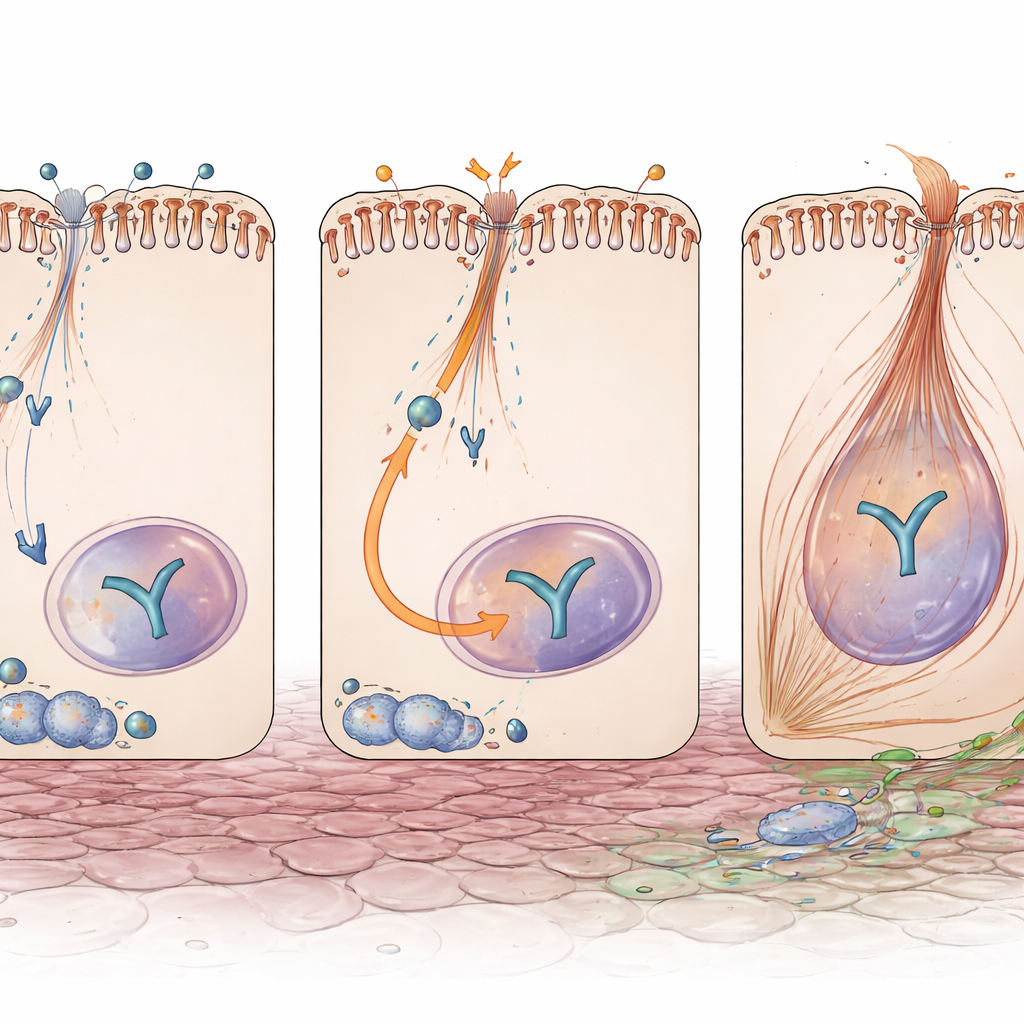
Ein Schalter, der Verletzung mit Vernarbungssignalen verbindet
Ein weiterer zentraler Akteur bei Fibrose ist YAP, ein signalreaktives Protein, das in den Zellkern wandert, um Gene für Wachstum und Matrixproduktion einzuschalten. Selbst ohne Schaden wiesen Tubuli ohne Exoc5 höhere YAP-Proteinspiegel auf. Nach der Obstruktion war YAP in diesen Nieren stärker aktiviert und stärker in Zellkernen konzentriert, und seine nachgeschalteten Produkte — Moleküle, die für die fibrotische Umgestaltung bekannt sind — waren erhöht. Wichtig ist, dass dies nicht auf eine erhöhte YAP-Genaktivität zurückgeführt werden konnte, was darauf hindeutet, dass Exoc5 YAP auf Protein- oder Transportebene normalerweise bremst. In kultivierten menschlichen Tubuluszellen führte das Herunterregeln von EXOC5 mittels RNA-Interferenz zu höheren YAP- und Pax2-Werten und ließ die Zellen stärker auf das fibrotische Signal TGF-β reagieren, mit ausgeprägteren EMT-ähnlichen Veränderungen und mehr Zellen, die kontraktile Fasern annahmen, wie sie für Myofibroblasten typisch sind.
Was das für künftige Behandlungen bedeutet
In der Summe zeichnen die Befunde Exoc5 als stillen Wächter: Unter Stress hilft es den Tubuluszellen, ihre organisierte Identität zu bewahren, und hält pro-fibrotische Signale wie YAP und Pax2 in Schach. Fallen Exoc5-Spiegel — sei es durch genetischen Verlust oder Verletzung — verlieren Tubuluszellen leichter ihre Polarität, rutschen in einen entwicklungsähnlichen Zustand und befeuern den fibrotischen Prozess. Da die Entfernung von Exoc5 in proximalen Tubuli gesunde Nieren nicht schädigte, aber die Vernarbung nach einer Verletzung deutlich verschlechterte, deuten die Ergebnisse darauf hin, dass Exoc5 und seine Signalpartner vielversprechende Ziele für Therapien sein könnten, die darauf abzielen, Nierenfibrose zu verlangsamen oder umzukehren, bevor sie zur Niereninsuffizienz fortschreitet.
Zitation: Lim, H.J., Han, Y.K., Noh, M.R. et al. Deficiency of exocyst complex component Exoc5 exacerbates the progression of kidney fibrosis. Exp Mol Med 58, 681–695 (2026). https://doi.org/10.1038/s12276-026-01649-8
Schlüsselwörter: Nierenfibrose, Exoc5, Epithel-zu-Mesenchym-Transition, YAP-Signalgebung, chronische Nierenerkrankung