Clear Sky Science · de
Mit Mikroglia verbundene Progression der Multiplen Sklerose: Zielidentifikation und therapeutische Ansprache in humanen In-vitro-Modellen
Warum Immunzellen des Gehirns bei Multipler Sklerose wichtig sind
Multiple Sklerose (MS) wird oft als Erkrankung beschrieben, bei der das Immunsystem des Körpers Gehirn und Rückenmark angreift. Viele der heute verfügbaren Medikamente verringern akute Schübe erfolgreich, doch sie stoppen nicht das langsame, schleichende Fortschreiten, das viele Patientinnen und Patienten über Jahre erleben. Diese Übersichtsarbeit erklärt, wie winzige, dauerhaft im Gehirn lebende Immunzellen, die Mikroglia genannt werden, diesen langfristigen Abbau antreiben können — und wie neue im Labor gezüchtete menschliche Gehirnmodelle Forschenden helfen, Behandlungen zu finden, die das Fortschreiten verzögern oder stoppen könnten.
Der verborgene Motor des andauernden Schadens
MS wurde traditionell in schubförmige und progrediente Formen unterteilt, doch zeigen Befunde inzwischen, dass die Progression bei nahezu allen Erkrankten sehr früh beginnt, selbst wenn zunächst nur Schübe sichtbar sind. Während Schübe durch aus dem Blut eindringende Immunzellen angetrieben werden, scheint die Progression durch entzündliche Prozesse zu entstehen, die im Inneren von Gehirn und Rückenmark eingeschlossen sind. In diesem abgeriegelten Milieu sind Mikroglia an vielen schädlichen Vorgängen beteiligt: anhaltende Entzündung, Verlust der isolierenden Myelinschicht an Nervenfasern in Weiß- und Grauer Substanz, Anhäufung schädlicher sauerstoffbezogener Moleküle und versagende Reparaturmechanismen. Das Endergebnis ist der allmähliche Verlust von Nervenzellen und ihrer Verbindungen. Normalerweise tragen Mikroglia zur Hirngesundheit bei, indem sie Trümmer entfernen und Nervenzellen unterstützen, doch bei MS neigen sie dazu, in aggressivere Zustände umzuschalten und einige ihrer schützenden Funktionen zu verlieren, was sie zu Hauptverdächtigen für die Progression macht.
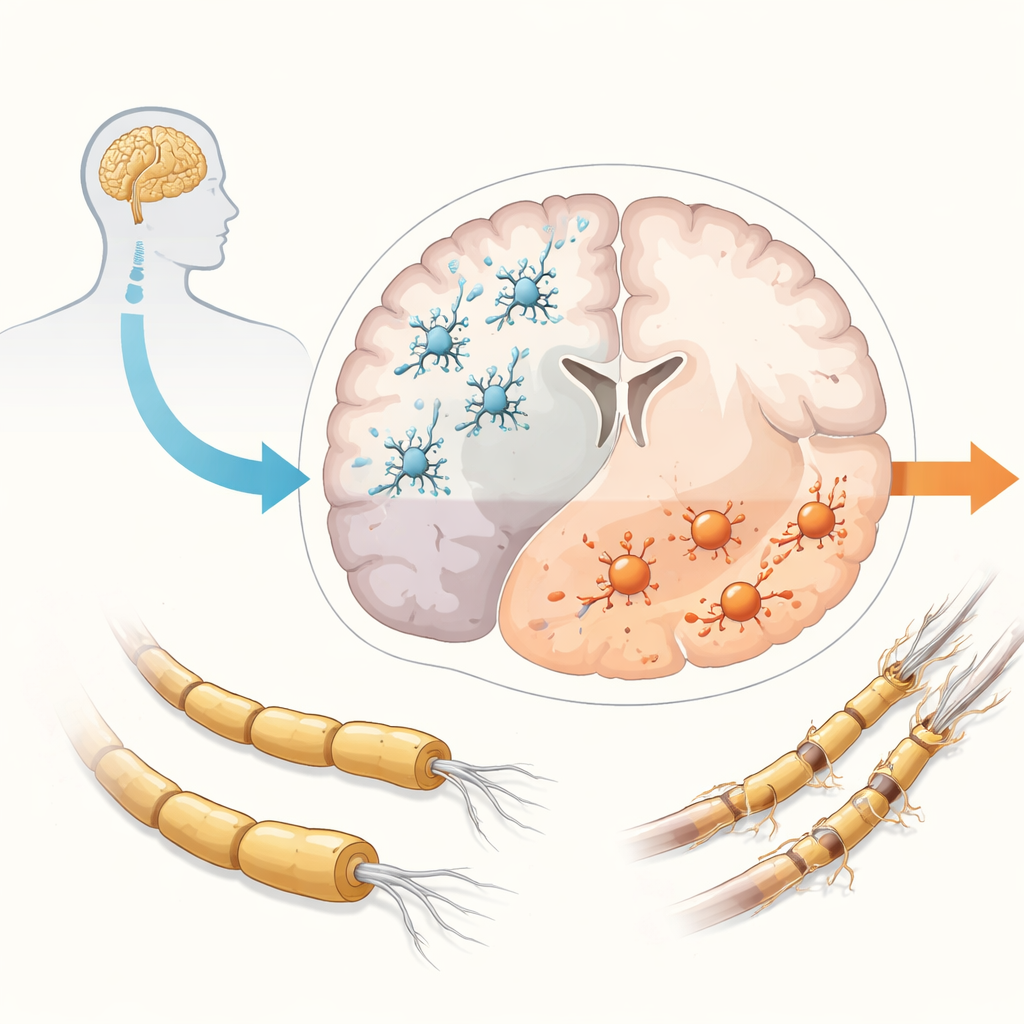
Warum traditionelle Tiermodelle nicht ausreichen
Jahrzehntelang waren Studien an Mäusen und anderen Tieren entscheidend für die Entwicklung von Medikamenten, die Schübe begrenzen, doch sie haben weitgehend versagt, Therapien hervorzubringen, die das Fortschreiten stoppen. Ein Grund ist, dass Tiermodelle die menschliche MS nur teilweise nachbilden und die komplexe, lang anhaltende Entzündung im Gehirn von Patientinnen und Patienten nicht vollständig reproduzieren. Mikroglia von Nagetieren unterscheiden sich zudem in wichtigen Genen und Reaktionen von menschlichen Mikroglia. Infolgedessen wirken Behandlungen, die in Tieren vielversprechend erscheinen, beim Menschen oft nicht. Der Mangel an Tiermodellen, die die progrediente MS wirklich erfassen, hat Forschende dazu veranlasst, neue, menschliche Systeme im Labor zu entwickeln, in denen Mikroglia und andere Gehirnzellen direkter untersucht werden können.
Aufbau humaner Gehirnmodelle auf der Petrischale
Wissenschaftlerinnen und Wissenschaftler nutzen heute mehrere Ebenen von Labormodellen, um humane Mikroglia zu untersuchen. Primärzellen, die direkt aus Gehirngewebe von Nagetieren oder Menschen entnommen werden, bewahren viele natürliche Eigenschaften, sind jedoch schwer zu gewinnen, verändern sich außerhalb ihres natürlichen Umfelds schnell und lassen sich nicht leicht hochskalieren. Um diese Hürden zu überwinden, wenden Forschende induzierte pluripotente Stammzellen (iPS-Zellen) an — erwachsene Zellen, die zurück in einen flexiblen, stammezellähnlichen Zustand reprogrammiert wurden. Diese iPS-Zellen können gezielt zu Mikroglia, Neuronen oder anderen Gehirnzellen differenziert werden. In einfachen zweidimensionalen Kulturen erfassen iPS‑abgeleitete Mikroglia viele Schlüsselfunktionen und lassen sich in großer Zahl produzieren, was detaillierte Experimente und Wirkstoffscreenings ermöglicht. Sie können sogar aus einzelnen MS-Patientinnen und -Patienten gewonnen werden und damit angeborene Unterschiede offenbaren, etwa veränderte Genaktivität und Unterschiede in der Reaktion auf Stress oder der Beseitigung von Zelltrümmern.
Realistischere Gehirn-Nachbarschaften hinzufügen
Da das Verhalten von Mikroglia stark von ihrer Umgebung geprägt wird, sind Forschende über Einzelzell-Schichten hinausgegangen und nutzen realistischere Anordnungen. In zweidimensionalen Kokulturen wachsen Mikroglia gemeinsam mit Neuronen und Stützzellen, was ihnen hilft, natürlichere Formen und Verhaltensweisen anzunehmen, und erlaubt es, die Wechselwirkungen zwischen Zelltypen zu untersuchen. Dreidimensionale Sphäroide und Organoide — winzige, selbstorganisierende Stücke gehirnähnlichen Gewebes — gehen noch weiter und bieten eine weiche, dichte Umgebung, die dem tatsächlichen Hirngewebe näherkommt. Wenn Mikroglia in diese Strukturen eingebettet werden, zeigen sie komplex verzweigte Formen, reagieren auf Verletzungen, interagieren mit einer blut‑hirn‑schrankenähnlichen Schicht und sprechen auf entzündliche Signale aus dem Nervenwasser von Menschen mit MS an. Solche Modelle wurden genutzt, um zu untersuchen, wie chronische Entzündung einen „müden, aber entzündeten“ Zustand namens zelluläre Seneszenz in Mikroglia und Astrozyten auslöst und wie Veränderungen im Fettstoffwechsel der Mikroglia die Myelinreparatur beeinträchtigen können. Parallel dazu erlaubt die Transplantation menschlicher, iPS‑abgeleiteter Mikroglia oder Organoide in Mäusehirne, dass diese Zellen innerhalb eines lebenden Netzwerks weiter reifen und in etablierten MS‑ähnlichen Krankheitsmodellen getestet werden können.
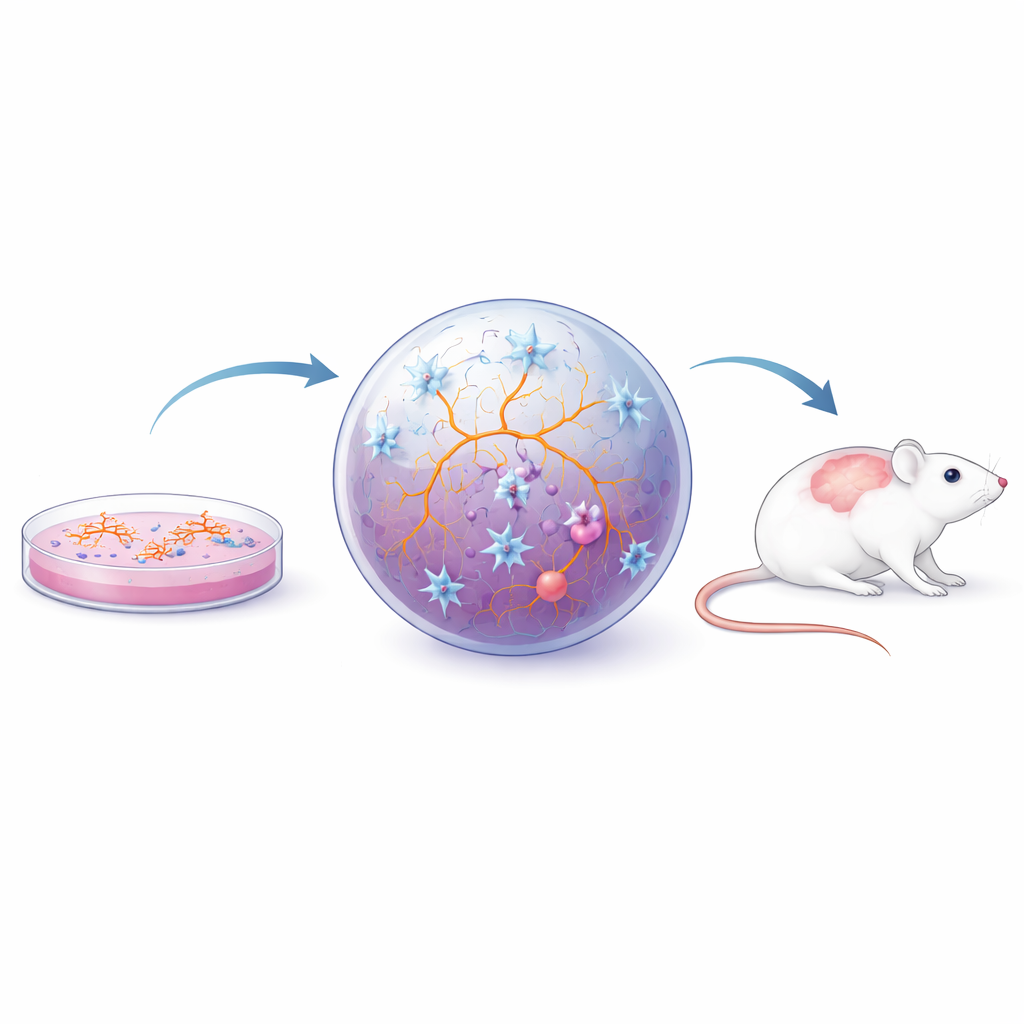
Von Labormodellen zu künftigen Therapien
Zusammen bilden diese humanbasierten In‑vitro‑ und chimären Modelle ein Werkzeugset, um zu analysieren, wie Mikroglia zur MS‑Progression beitragen, und um neue Therapien zu testen, die schädliche mikrogliale Aktivität beruhigen und gleichzeitig schützende Funktionen wiederherstellen sollen. Zwar reproduziert keines der Modelle das menschliche Gehirn vollständig, doch jedes erfasst unterschiedliche Puzzleteile, und gemeinsam überbrücken sie die Lücke zwischen einfachen Zellkulturen und unvollkommenen Tiermodellen. Durch die Kombination von Erkenntnissen aus diesen Systemen hoffen Forschende, präzise Wirkstoffziele zu identifizieren — etwa Signalwege, die Entzündung, altersähnliche Veränderungen und Lipidstoffwechsel in Mikroglia steuern — die schließlich in Behandlungen münden könnten, die die schrittweise Behinderungsentwicklung verlangsamen oder stoppen, die die progrediente MS kennzeichnet.
Zitation: Blenkle, A., Geladaris, A. & Weber, M.S. Microglia-associated progression of multiple sclerosis: target identification and therapeutic engagement in human in vitro models. Exp Mol Med 58, 357–365 (2026). https://doi.org/10.1038/s12276-026-01647-w
Schlüsselwörter: Progression der Multiplen Sklerose, Mikroglia, induzierte pluripotente Stammzellen, Gehirnorganoide, Neuroinflammation