Clear Sky Science · de
Eine ESRP1/circPHGDH/miR-149/RAP1B positive Rückkopplungsschleife fördert das maligne Verhalten und die Glykolyse von Prostatakrebszellen
Warum diese Forschung für die Gesundheit von Männern wichtig ist
Prostatakrebs ist eine der häufigsten Krebserkrankungen bei Männern; viele Tumoren werden schließlich aggressiv und therapieresistent. Diese Studie deckt einen bisher verborgenen Steuerkreis in Prostatakrebszellen auf, der ihr schnelleres Wachstum, ihre leichtere Ausbreitung und die Umprogrammierung ihres Zuckerstoffwechsels fördert. Durch das Aufzeigen dieser molekularen Schleife weisen die Forschenden auf neue Schwachstellen hin, die möglicherweise angegriffen werden können, um das Fortschreiten der Erkrankung zu verlangsamen oder bestehende Therapien wirksamer zu machen.
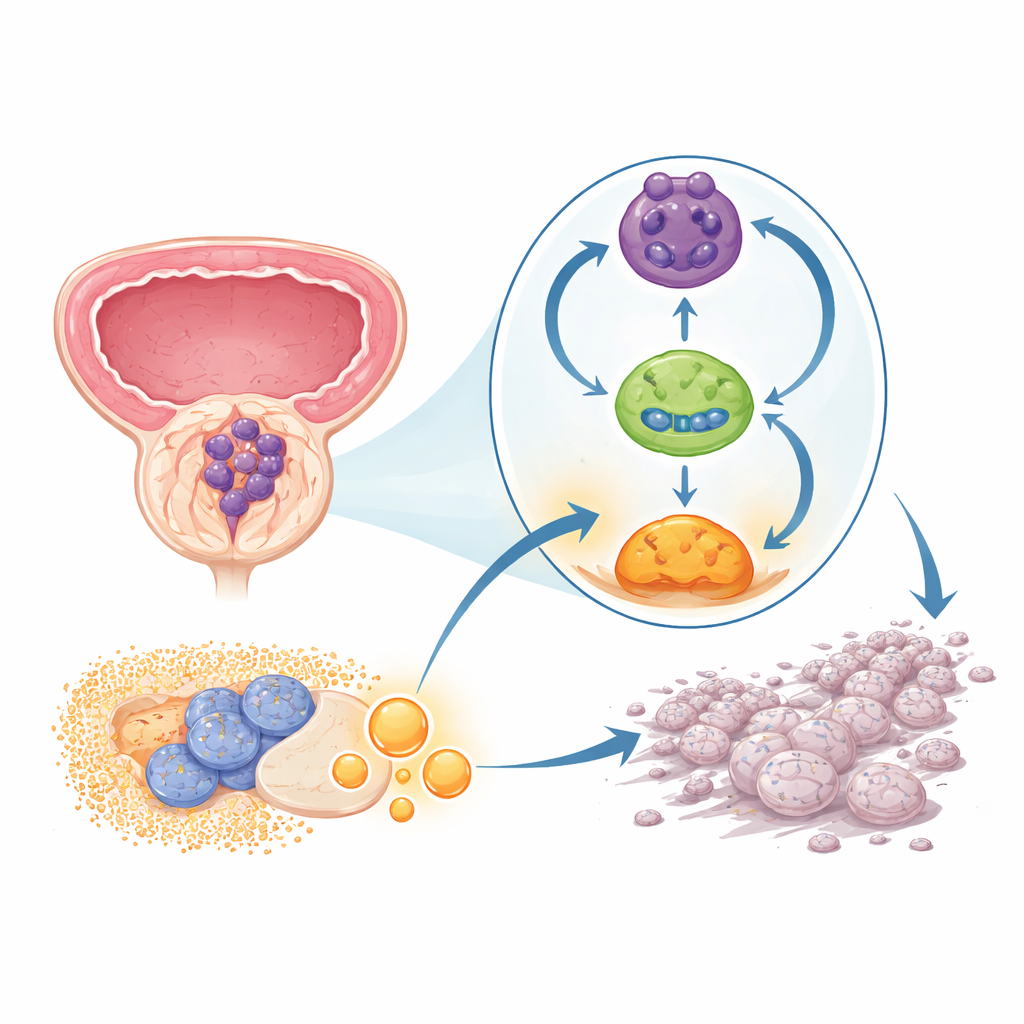
Eine verborgene Schleife, die Krebs eingeschaltet hält
Das Team konzentrierte sich auf eine neu beachtete Klasse genetischen Materials, die sogenannten zirkulären RNAs. Im Gegensatz zu den üblichen linearen Strängen bilden diese Moleküle geschlossene Ringe und sind bemerkenswert stabil. In Prostatatumorproben und Zelllinien fanden die Forschenden eine bestimmte zirkuläre RNA, genannt circPHGDH, die durchgehend höher war als im umliegenden gesunden Gewebe. Patienten, deren Tumoren vermehrt dieses RNA-Molekül enthielten, hatten tendenziell größere Tumoren, weiter fortgeschrittenes örtliches Wachstum und Fernmetastasen, was darauf hindeutet, dass circPHGDH eine treibende Rolle bei einer gefährlicheren Form der Erkrankung spielt.
Wie Krebszellen ihr Verhalten ändern
Um herauszufinden, was circPHGDH tatsächlich bewirkt, veränderten die Wissenschaftlerinnen und Wissenschaftler dessen Menge in im Labor kultivierten Prostatakrebszellen. Bei Reduktion von circPHGDH bildeten die Zellen weniger Kolonien, bewegten sich und invasierten Membranen weniger effizient und zeigten Anzeichen dafür, in einem eher „epithelialen“ Zustand zu verbleiben, der weniger zur Ausbreitung neigt. Gleichzeitig verschoben sich die Zellen weg von einem zuckerhungrigen Stoffwechselstil, wie er für viele Tumoren typisch ist: ihre Abhängigkeit von der Glykolyse sank, und sie nutzten vermehrt die sauerstoffabhängige Energiegewinnung. Wurde circPHGDH hingegen erhöht, bewegten sich all diese krebsfördernden Eigenschaften in die entgegengesetzte Richtung.
Kleine RNAs und eine Wachstums-Signalweiterleitung
Die Studie verfolgte anschließend nach, wie circPHGDH diese Effekte ausübt. Im wässrigen Innenraum der Zelle wirkt circPHGDH wie ein Schwamm für eine kleine regulatorische RNA namens miR-149: Es bindet sie und verhindert so, dass sie ihre üblichen Zielmoleküle hemmt. Ein wichtiges Ziel ist RAP1B, ein Signalmolekül, das in einen zentralen Wachstums- und Überlebensweg einspeist, der für Prostatakrebs bedeutsam ist. Wenn miR-149 durch circPHGDH gebunden wird, steigen die RAP1B-Spiegel an und schalten nachgeschaltete Signale ein, die Zellteilung, Bewegung und einen glykolyselastigen Stoffwechsel fördern. Die Wiederherstellung von miR-149 oder die direkte Reduktion von RAP1B kehrte viele der schädlichen Effekte um, sowohl in Zellkulturen als auch in Mäusen mit menschlichen Prostatatumoren.
Metabolischer Abfall, der das Feuer schürt
Eine weitere Ebene der Geschichte betrifft die Entstehung von circPHGDH selbst. Seine Bildung hängt von einem Spleißprotein namens ESRP1 ab, das mitentscheidet, wie Vorläufer-RNA geschnitten und wieder zusammengefügt wird. Die Forschenden zeigten, dass ESRP1 an spezifische Stellen rund um den circPHGDH-Bereich bindet und dessen zirkuläre Form gegenüber der üblichen linearen Variante bevorzugt. Entscheidenderweise entdeckten sie, dass Lactat — das Endprodukt der Glykolyse — ESRP1 an einer einzigen Stelle chemisch modifiziert und das Protein dadurch stabiler macht. Da circPHGDH die Zellen selbst in Richtung verstärkter Glykolyse und damit zu mehr Lactat treibt, entsteht eine sich selbst verstärkende Schleife: ESRP1 erhöht circPHGDH, circPHGDH steigert RAP1B und die Glykolyse, die Glykolyse erzeugt Lactat, und Lactat stabilisiert wiederum ESRP1.
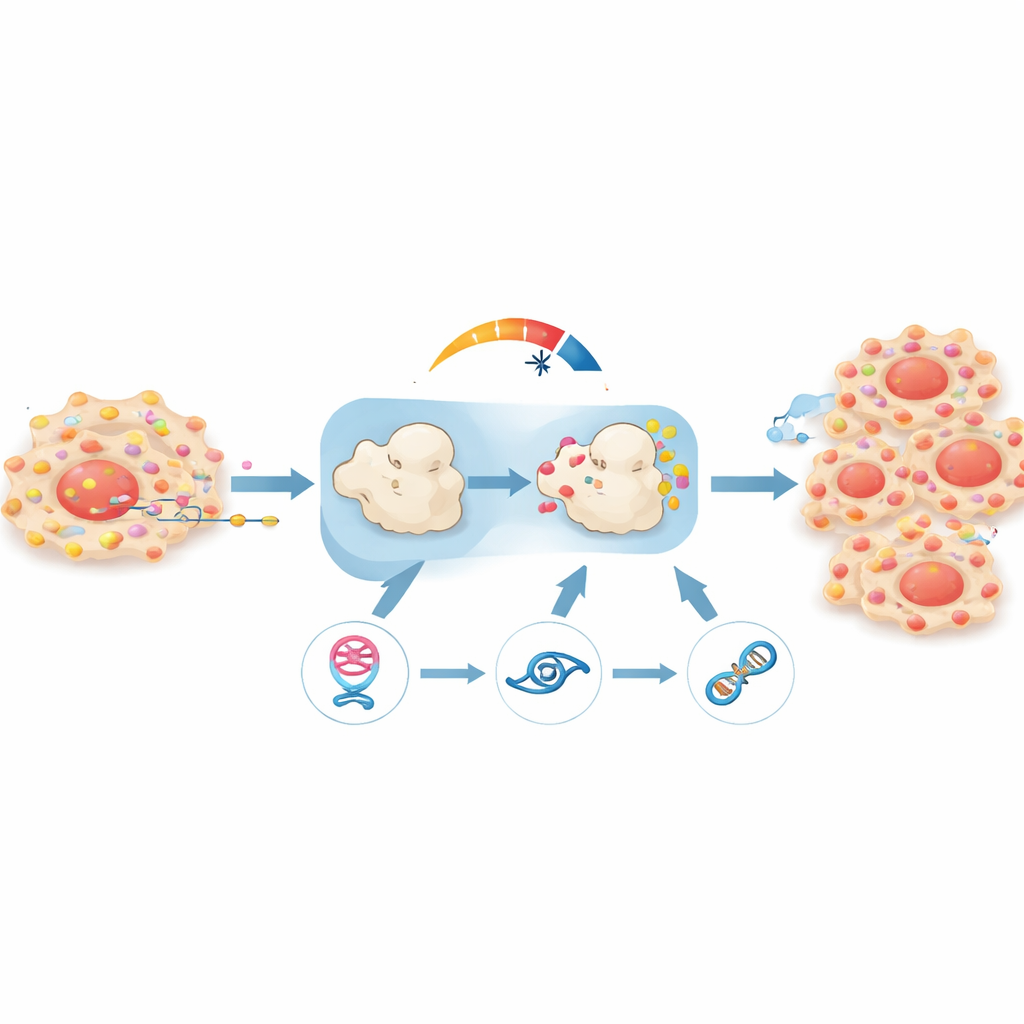
Belege aus Tiermodellen
Um zu prüfen, ob diese Schleife in einem lebenden Organismus tatsächlich von Bedeutung ist, setzten die Forschenden menschliche Prostatakrebszellen in Mäuse ein. Tumoren, in denen circPHGDH ausgeschaltet worden war, wuchsen langsamer, wogen weniger und zeigten weniger Anzeichen von Ausbreitung, gemessen durch Ganzkörperbildgebung und Gewebeanalysen. Proliferationsmarker waren niedriger, und die Tumorstruktur wirkte unter dem Mikroskop weniger aggressiv. Als die Forschenden in denselben Tumoren entweder miR-149 blockierten oder RAP1B wieder hochregulierten, kehrten viel von Wachstum und Ausbreitung zurück, was bestätigt, dass die circPHGDH–miR-149–RAP1B-Kette ein zentraler Treiber des Krankheitsverhaltens ist.
Was das für zukünftige Behandlungen bedeutet
Insgesamt zeigen die Ergebnisse eine positive Rückkopplungsschleife, in der ein Spleißprotein, eine zirkuläre RNA, eine kleine regulatorische RNA und ein Signalmolekül zusammenwirken, um Prostatakrebszellen zu schnellem Wachstum, Invasion und einem zuckerintensiven Stoffwechsel zu treiben. Für Nichtfachleute ist die Kernbotschaft, dass Krebszellen ihre genetischen und metabolischen Kontrollen zu selbstverstärkenden Schaltkreisen verknüpfen können, die das Fortschreiten der Krankheit vorantreiben. Das Unterbrechen dieser Schleife — durch das Stören von circPHGDH, die Wiederherstellung von miR-149, das Blockieren von RAP1B oder das Eingreifen in die lactatabhängige Modifikation von ESRP1 — eröffnet mehrere vielversprechende Ansätze für zukünftige Wirkstoffe, die darauf zielen, aggressiven Prostatakrebs zu verlangsamen oder aufzuhalten.
Zitation: Wang, X., Yu, L., Qian, X. et al. A ESRP1/circPHGDH/miR-149/RAP1B positive feedback loop promotes the malignant behaviors and glycolysis of prostate cancer cell. Exp Mol Med 58, 622–635 (2026). https://doi.org/10.1038/s12276-026-01646-x
Schlüsselwörter: Prostatakrebs, zirkuläre RNA, Tumormetabolismus, MicroRNA, Signalwege