Clear Sky Science · de
PAK4 bei Stoffwechselerkrankungen: Regulation durch Nährstoffsignale und therapeutische Implikationen
Warum ein zellulärer Schalter für die Gesundheit im Alltag wichtig ist
Adipositas, Typ‑2‑Diabetes und Fettleber werden oft allein den Kalorien zugeschrieben, doch tief in unseren Zellen entscheiden molekulare Schalter, ob wir Energie verbrennen oder speichern. Dieses Review konzentriert sich auf einen solchen Schalter, ein Protein namens PAK4, und erklärt, wie es auf wechselnde Nährstoff‑ und Hormon‑Signale reagiert und dadurch den Stoffwechsel von Fett, Leber und Muskel umgestaltet. Das Verständnis dieses verborgenen Kontrollsystems könnte den Weg für neue Behandlungen eröffnen, die mehrere Stoffwechselerkrankungen gleichzeitig angehen statt einzelne Symptome isoliert zu behandeln. 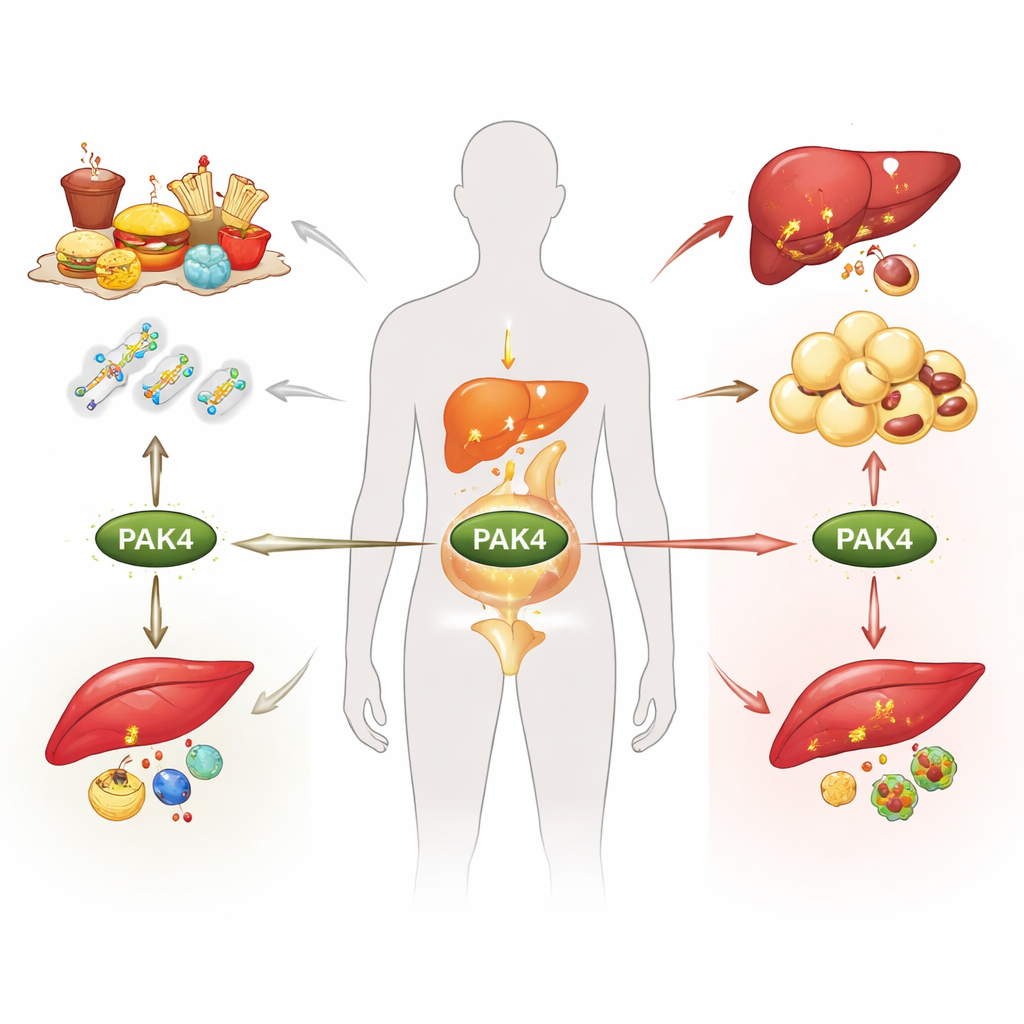
Ein zentraler Schalter, verborgen in unseren Zellen
PAK4 gehört zu einer Familie von Enzymen, die Signale von kleinen molekularen „Botenstoffen“ innerhalb der Zelle weiterleiten. Unter gesunden Bedingungen liegt PAK4 in wichtigen Stoffwechselorganen nur in geringen Mengen vor. Wenn das Energiegleichgewicht gestört ist, etwa bei Adipositas oder Typ‑2‑Diabetes, steigen seine Konzentrationen in Fettgewebe, Leber und Skelettmuskel an. Die Aktivität von PAK4 wird auf mehreren Ebenen gesteuert: durch aufwärts liegende Botenstoffe, die seine Form verändern, und durch chemische Anhängsel, die nach der Proteinsynthese angefügt oder entfernt werden. Dazu gehören Phosphatgruppen, die PAK4 entweder aktivieren oder für den Abbau markieren, sowie Modifikationen, die seine Stabilität oder Aktivität beeinflussen. Fasten, Nahrungsaufnahme, Hormone und Stress beeinflussen diese Markierungen, sodass PAK4 effektiv den Ernährungszustand des Körpers „erfasst“ und diese Information an zentrale Stoffwechselwege weitergibt.
Wie PAK4 Fettzellen zur Speicherung neigen lässt
In Fettzellen wirkt PAK4 wie eine Bremse für die Fettverbrennung. Normalerweise löst Fasten oder ein Anstieg von Stresshormonen die kontrollierte Aufspaltung gespeicherter Fette in kleinen Tropfen aus, vermittelt durch ein Enzym namens PKA. Das Review beschreibt, wie PAK4 diesen Prozess kontert, indem es hemmende Phosphatgruppen direkt an die hormonempfindliche Lipase und an ein fettsäurebindendes Protein anbringt, das beim Transport von Fettsäuren hilft. Diese Veränderungen schwächen die Mechanik, die Fett aus den Speichern freisetzt. PAK4 unterstützt außerdem die Bildung neuer Fettzellen in früheren Lebensphasen, indem es Zellzyklus‑Proteine fördert, die Vorläuferzellen zur Ausreifung zu speichernden Fettzellen treiben. Wenn PAK4 in Tiermodellen entfernt oder blockiert wird, verbrennen Fettzellen mehr Energie, zeigen Merkmale des „Browning“, die den Energieverbrauch erhöhen, und die Tiere sind vor gewichtszunahme durch die Ernährung geschützt. 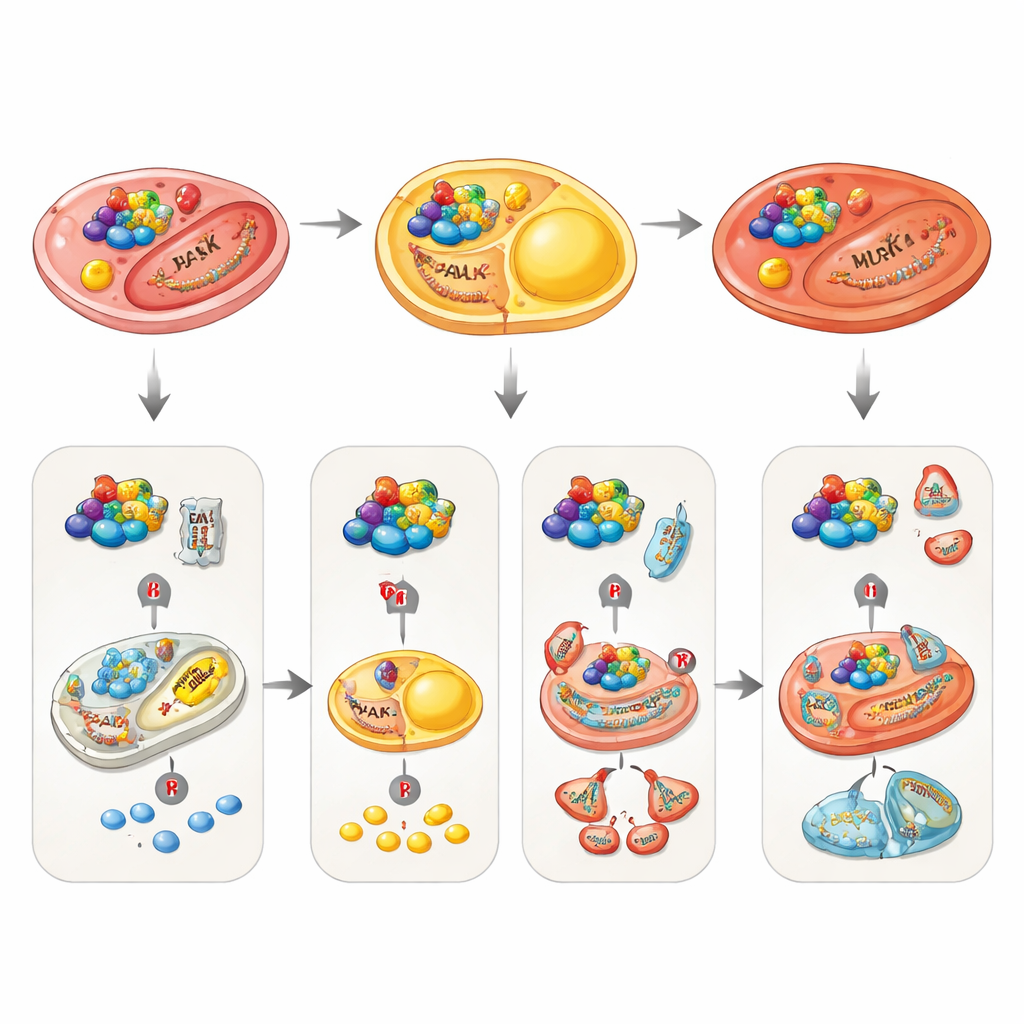
PAK4s Rolle bei Fettleber und Zucker‑Handling im Muskel
In der Leber begünstigt PAK4 ebenfalls das Speichern statt das Verbrennen. Während des Fastens oder bei ketogener Ernährung fallen die PAK4‑Spiegel, was den Leberzellen erlaubt, die Fettspaltung und Ketonkörperbildung hochzufahren; diese liefern anderen Geweben Energie und können sogar das Tumorwachstum bremsen. Wenn PAK4 reichlich vorhanden ist, fügt es Phosphatgruppen an einen nukleären Korepressor an, der dann PPARα, einen zentralen Regulator der Fettoxidation und Ketogenese, dämpft. Das Ergebnis ist mehr in der Leber eingeschlossenes Fett und weniger schützende Ketone im Blut. Im Skelettmuskel stört PAK4 den zentralen Energiesensor AMPK, der sowohl die Zuckeraufnahme als auch die mitochondriale Aktivität fördert. Durch eine Markierung, die dessen Aktivierung blockiert, reduziert PAK4 die Menge an Glukosetransportern an der Muskelzelloberfläche und trägt so zur Insulinresistenz bei. Ein musclespezifischer Verlust von PAK4 in Mäusen kehrt diese Effekte um und verbessert die Blutzuckerregulation selbst unter fettleibigen Bedingungen.
Stress, Schutzmechanismen und Verbindungen zu anderen zellulären Schaltern
Das Review hebt außerdem PAK4s Auswirkungen über den Alltagstoffwechsel hinaus hervor. Bei Episoden reduzierter Durchblutung und anschließender Wiederherstellung des Blutflusses in Organen wie der Leber schwächt PAK4 die antioxidativen Abwehrmechanismen, indem es Nrf2, einen wichtigen Schutzfaktor gegen oxidativen Stress, markiert und destabilisiert. Gleichzeitig übernimmt ein anderes Familienmitglied, PAK1, in Herz‑ und Skelettmuskel sowie in insulinsezernierenden Zellen der Bauchspeicheldrüse oft unterstützende Rollen und trägt zur normalen Glukoseverarbeitung bei. Dieser Gegensatz zwischen schädlicher PAK4‑Signalgebung in Stoffwechselerkrankungen und den zumeist vorteilhaften Wirkungen von PAK1 unterstreicht die Notwendigkeit hoch selektiver Medikamente, die PAK4 ausschalten, ohne verwandte Proteine zu stören, die für Herz‑ und endokrine Gesundheit essenziell sind.
Aus einer Entdeckung eine Therapie machen
Da PAK4 sowohl bei Krebs als auch bei Stoffwechselstörungen überaktiv ist, haben Wirkstoffentwickler kleine Moleküle entwickelt, die seine Aktivität blockieren, sowie neue „Degrader“‑Medikamente, die PAK4 selbst für den Abbau markieren. Frühe PAK4‑Blocker zeigten antitumorales Potenzial, stießen jedoch auf Probleme mit Selektivität und Pharmakokinetik. Neuere Moleküle, die PAK4 präziser anvisieren, erzielten in übergewichtigen Mäusen beeindruckende Ergebnisse: geringeres Körpergewicht bei unverändertem Futterkonsum, gesündere Lebern, aktivere Muskeln und verbesserte Blutzuckerwerte. Degrader‑Medikamente gehen einen Schritt weiter, indem sie PAK4 physisch eliminieren; frühe Tierstudien deuten darauf hin, dass sie vor Muskelabbau und bestimmten Krebsarten schützen können. Zusammengenommen stützen diese Befunde das Bild, dass eine Reduktion von PAK4 gleichzeitig Adipositas, Diabetes und Fettleber lindern könnte und einen einst wenig beachteten zellulären Schalter zu einem vielversprechenden Ziel künftiger metabolischer Therapien macht.
Zitation: Bang, I.H., Park, BH. & Bae, E.J. PAK4 in metabolic diseases: regulation by nutrient signals and therapeutic implications. Exp Mol Med 58, 416–424 (2026). https://doi.org/10.1038/s12276-026-01645-y
Schlüsselwörter: PAK4, Stoffwechselerkrankung, Adipositas, Fettleber, Insulinresistenz