Clear Sky Science · de
Das redox-sensible Protein HMGB1: intrazelluläre und extrazelluläre Rollen
Warum ein Formwandler-Protein für die Gesundheit wichtig ist
In fast jeder Zelle Ihres Körpers sitzt ein kleines Protein namens HMGB1, das ein wenig wie ein Multifunktionswerkzeug agiert. Unter ruhigen Bedingungen hilft es leise bei der Organisation der DNA. Wenn Zellen jedoch gestresst oder geschädigt sind, kann HMGB1 aus dem Zellkern austreten, ins umgebende Gewebe gelangen und als Alarmzeichen für das Immunsystem wirken. Dieser Übersichtsartikel erklärt, wie winzige chemische Veränderungen durch Oxidation HMGB1 in sehr unterschiedliche biologische Persönlichkeiten verwandeln können — solche, die Gewebe schützen, Entzündungen antreiben oder sogar zu chronischen Erkrankungen beitragen. Das Verständnis dieses molekularen „Stimmungsrings“ könnte neue Wege eröffnen, übermäßige Entzündungsreaktionen zu dämpfen, ohne das Immunsystem vollständig auszuschalten.
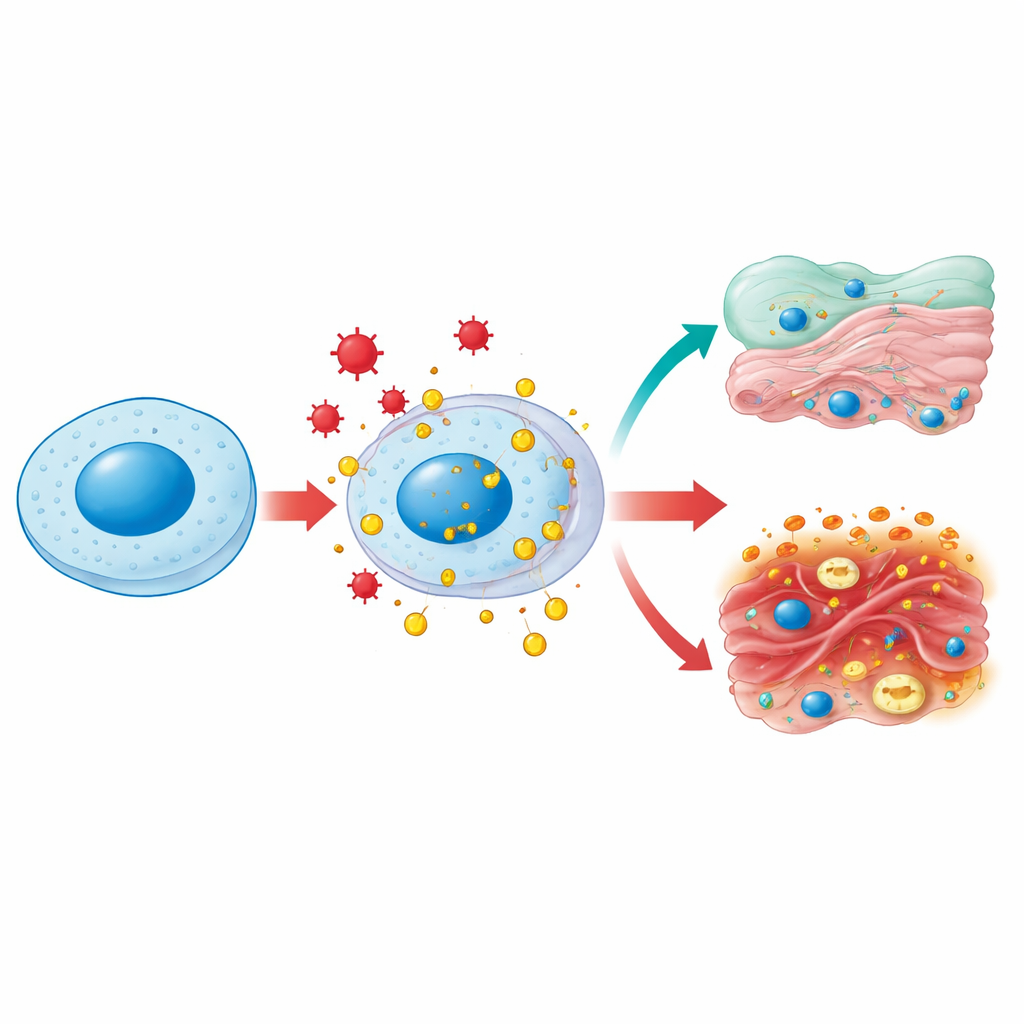
Ein Protein, viele Aufenthaltsorte
HMGB1 lebt normalerweise im Zellkern, wo es die DNA biegt und lockert, damit Gene kopiert und repariert werden können. Unter Stress — etwa durch Infektionen, hohen Blutzucker oder toxische Schäden — kann es chemisch modifiziert und aus dem Kern in das wässrige Zellinnere und schließlich nach außen transportiert werden. Im Zytoplasma hilft HMGB1, die Mitochondrien, die Kraftwerke der Zelle, gesund zu erhalten, indem es einen Reinigungsprozess namens Autophagie fördert und übermäßige Fragmentierung dieser Organellen verhindert. Wird HMGB1 außerhalb der Zelle freigesetzt, wird es zum klassischen „Gefahrensignal“: Immunzellen erkennen es als Hinweis auf Gewebeschäden und eilen herbei. Dasselbe Molekül übernimmt also je nach Aufenthaltsort und chemischer Modifikation sowohl Haushaltsaufgaben innerhalb der Zelle als auch Alarmfunktionen außerhalb.
Wie Oxidation sein Verhalten umschreibt
Der zentrale Punkt dieser Übersicht ist, wie Oxidation — Reaktionen, die durch reaktive Sauerstoffspezies (ROS) angetrieben werden — HMGB1 umformt. Das Protein enthält drei schwefelhaltige Bausteine, die als winzige Schalter fungieren. Im vollständig reduzierten Zustand fördert HMGB1 eher das Überleben von Zellen und die Rekrutierung von Reparaturzellen. Milde Oxidation kann zwei dieser Stellen innerhalb desselben Proteins miteinander verbinden und eine „Disulfid“-Form erzeugen, die besonders gut an Immunrezeptoren wie Toll‑like‑Rezeptoren und RAGE an Zelloberflächen bindet. Diese Version stimuliert stark die Produktion entzündlicher Botenstoffe. Stärkerer oxidativer Stress kann das Molekül weiter in eine überoxidierte Form treiben, die DNA oder Rezeptoren nicht mehr effektiv binden kann; diese „ausgebrannte“ Form wird immunologisch still und ist mit der Auflösungsphase der Entzündung und mit zellulären Todesprogrammen verbunden, die keine Immunreaktion provozieren.
Von Todeszeichen der Zelle zu Krankheitsmotoren
HMGB1 ist eng mit den verschiedenen Formen des Zelltods verknüpft. Bei gewaltsamen Formen des Todes wie Nekrose, Nekroptose, Ferroptose und Pyroptose tritt HMGB1 aus der Zelle aus oder wird aktiv nach außen transportiert und trägt dabei eine Redox-Signatur, die die umgebenden oxidativen Bedingungen widerspiegelt. Früh in der Nekrose liegt es tendenziell in reduzierter Form vor, während andauernder Stress es in stärker oxidierte Zustände treibt. Außerhalb der Zelle kann reduziertes HMGB1 in einigen Krebszellen schützende Autophagie fördern und so deren Überleben unter Chemotherapie unterstützen, während disulfidreiche und dimerisierte Formen entzündliche Kaskaden und Komplementaktivierung verstärken, die Gewebeschäden verschlimmern können. HMGB1 kann auch Rückkopplungen fördern, die bestimmte Todeswege antreiben — zum Beispiel durch Partnerschaften mit bakteriellen Lipiden, die Nekroptose auslösen, oder indem es nach Schlaganfällen eisenabhängigen Zelltod in Stützzellen des Gehirns fördert. Auf diese Weise markiert und moduliert HMGB1 das Gleichgewicht von Leben und Tod im Gewebe.
Verbindungen zu Entzündung, Autoimmunität und Krebs
Da sein Verhalten so empfindlich gegenüber Oxidation ist, treten verschiedene HMGB1‑Varianten in unterschiedlichen Mustern bei Krankheiten auf. Disulfidreiches HMGB1 wird stark mit chronischer Entzündung assoziiert: Es findet sich in entzündeten Gelenken bei rheumatoider Arthritis, in fibrotischem Lebergewebe, bei Lungenschäden, bei Ischämie‑Reperfusionsschäden nach Operationen und beim Sepsisgeschehen, wo seine Blutspiegel mit Schwere und Sterberisiko korrelieren. Reduziertes HMGB1 steht dagegen oft im Zusammenhang mit Zellmigration und Gewebsumbau, etwa bei der Bewegung von Herzfibroblasten oder Monozyten, die durch den Chemokinstoff CXCL12 geleitet werden. Überoxidiertes, immunologisch ruhiges HMGB1 ist in Situationen wie dem späten Apoptose‑Stadium angereichert, wenn der Körper sterbende Zellen ohne Entzündungsreaktion entfernen möchte. In Tumoren fördert die Disulfid‑Form ein unterdrückendes, wachstumsförderndes Immunumfeld, während die Blockade von HMGB1 Tumoren verkleinern und Checkpoint‑Immuntherapien wirksamer machen kann.
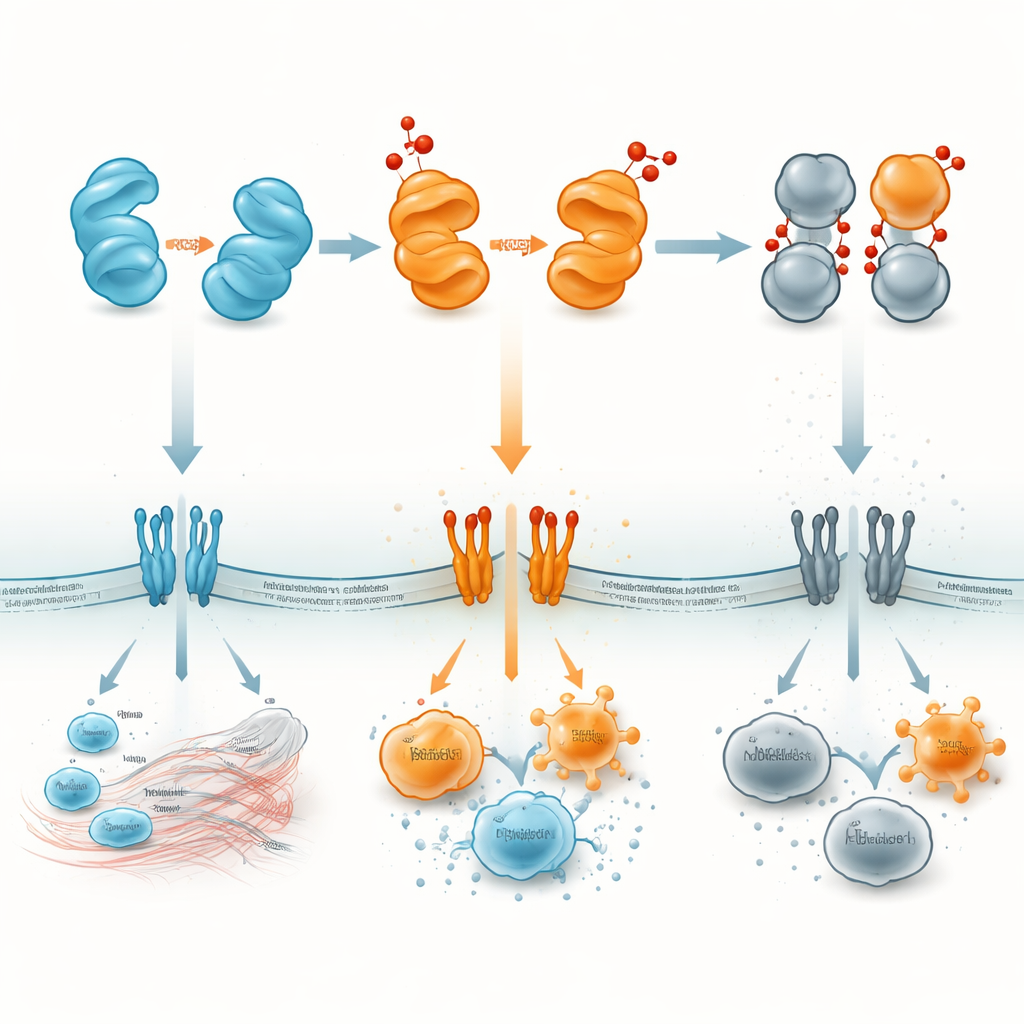
Aus einem molekularen Alarm ein therapeutisches Ziel machen
Für einen Laien lässt sich HMGB1 als kleines Protein‑Alarmgerät verstehen, dessen Lautstärke und Botschaft sich mit seinem chemischen Zustand ändern. Reduziertes HMGB1 ruft tendenziell Reparaturmannschaften herbei; die Disulfid‑ und Dimerformen können einen scharfen Alarm blasen, der schädliche Entzündungen nährt; und die vollständig oxidierte Form verstummt praktisch und hilft, Entzündungen abklingen zu lassen. Indem Forscher kartieren, wo und wann jede Version auftritt — in Kernen, im Zytoplasma, im Blut oder in bestimmten Organen — hoffen sie, Medikamente zu entwickeln, die entweder die schädlichen Formen blockieren oder die nützlichen stabilisieren. Solche Strategien könnten es Ärzten ermöglichen, Sepsis, Autoimmunerkrankungen, Schlaganfall, Lungenschäden oder Krebs zu behandeln, indem sie nicht nur HMGB1 selbst, sondern den oxidativen „Dimmer“ anvisieren, der bestimmt, wie dieses Protein mit dem Immunsystem kommuniziert.
Zitation: Kwak, M.S., Jung, S.F., Park, I.H. et al. The redox-sensitive protein HMGB1: intracellular and extracellular roles. Exp Mol Med 58, 345–356 (2026). https://doi.org/10.1038/s12276-026-01640-3
Schlüsselwörter: HMGB1, Entzündung, oxidativer Stress, Zelltod, Autoimmunerkrankung