Clear Sky Science · de
Mechanotransduktion durch T-Zell-Rezeptoren: Konsens, Kontroversen und Ausblick
Wie Immunzellen ihre Umgebung ertasten
Unser Immunsystem macht mehr, als nur chemische Signale zu erschnüffeln; es nimmt auch physikalische Kräfte wahr. Dieser Übersichtsartikel untersucht, wie T‑Zellen — weiße Blutkörperchen, die Viren und Krebszellen aufspüren — winzige Zug‑ und Druckkräfte an ihren Oberflächenrezeptoren nutzen könnten, um zu entscheiden, ob sie angreifen. Das Verständnis dieses "Tastsinns" auf molekularer Ebene könnte unser Denken über Impfstoffe, Krebsimmuntherapien und Autoimmunerkrankungen verändern.
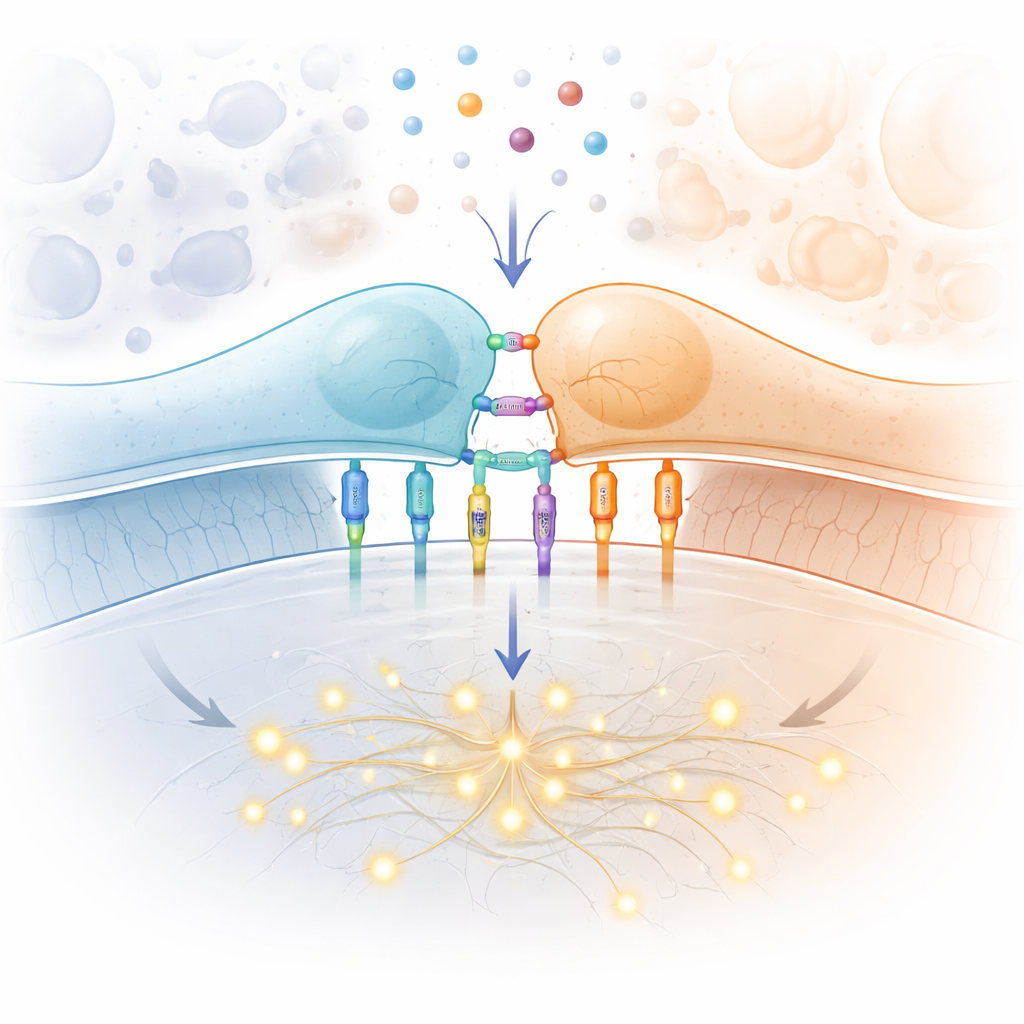
Die besondere Aufgabe des T‑Zell‑Rezeptors
Im Zentrum der Geschichte steht der T‑Zell‑Rezeptor, eine molekulare Maschine auf der T‑Zell‑Oberfläche, die Proteinfragmente inspiziert, die von anderen Zellen präsentiert werden. Wird das richtige Fragment erkannt, kann die T‑Zelle aktiv werden, sich vermehren und infizierte oder krebsartige Zielzellen abtöten. Dieser Rezeptor muss ein schwieriges Anforderungsprofil erfüllen: Er muss auf äußerst wenige fremde Fragmente reagieren, ein Meer harmloser Selbstfragmente ignorieren, schnell arbeiten, während T‑Zellen den Körper patrouillieren, und dies für Millionen verschiedener Rezeptorvarianten pro Person leisten. Die klassische Verkabelung des Signalwegs innerhalb der Zelle — mit Proteinkinasen, Gerüstproteinen und Transkriptionsfaktoren — ist gut kartiert. Was rätselhaft bleibt, ist der allererste Schritt: wie der einfache Akt des Bindens eines Fragments an der Zelloberfläche den Rezeptor vom stillen in den aktiven Zustand umschaltet.
Wettbewerb der Ideen für den ersten Funken
Forscher haben mehrere Modelle vorgeschlagen, wie der T‑Zell‑Rezeptor zunächst aktiviert wird. Nach einer Sichtweise beginnt die Signalübertragung, wenn Rezeptoren zusammen in kleine Cluster gebracht werden, was die lokale Konzentration erhöht und Signalkaskaden effizienter ablaufen lässt. Eine andere Idee betont Gestaltänderungen: Die Bindung könnte Teile des Rezeptorkomplexes verdrehen oder entspannen und dadurch verborgene Segmente im Zellinneren freilegen, die dann von Enzymen modifiziert werden können. Ein drittes Modell hebt Überfüllung an der Zell‑Zell‑Kontaktstelle hervor. Hier packen sich kurze Rezeptor‑Ligand‑Paare in enge Zonen, die sperrige Enzyme physikalisch ausschließen, die normalerweise Signale abschalten, und so das Gleichgewicht in Richtung Aktivierung verschieben. Jedes Modell wird durch Experimente gestützt und erklärt einen Teil des Puzzles, aber keines allein erklärt vollständig die außergewöhnliche Empfindlichkeit des Rezeptors und seine Fähigkeit, sehr ähnliche Proteinfragmente zu unterscheiden.
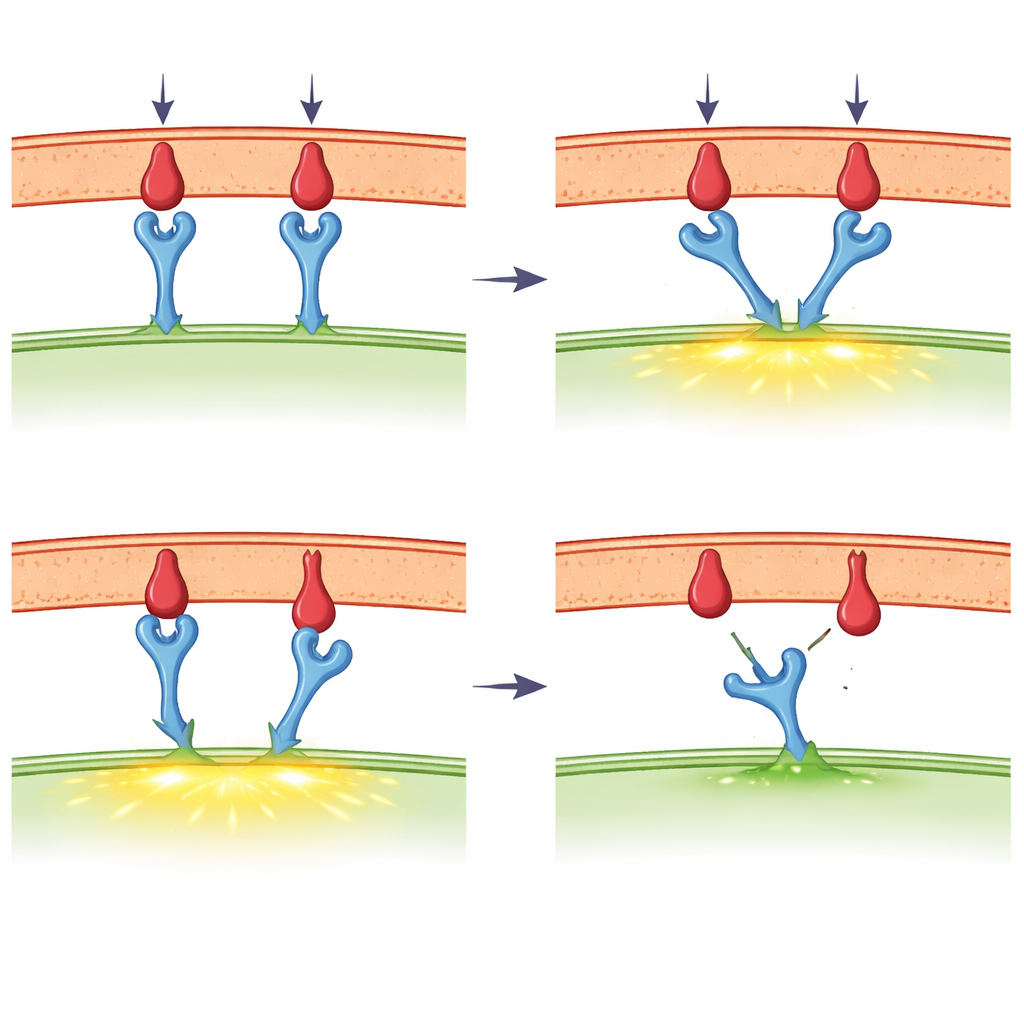
Wenn Tasten und Kraft ins Spiel kommen
Ein Schwerpunkt der Übersicht ist die aufkommende Idee, dass der T‑Zell‑Rezeptor als Mechanosensor fungiert — ein Gerät, das auf Kraft reagiert. Mit ultrasensitiven Instrumenten haben Wissenschaftler einzelne Rezeptor‑Ligand‑Bindungen mit Kräften gezogen, die eine Billion Mal kleiner sind als das Gewicht eines Apfels. Sie fanden, dass bei starken fremden Fragmenten ein moderater Zug die Lebensdauer der Bindung tatsächlich verlängern kann, ein Verhalten, das als "Catch"‑Antwort bekannt ist. Schwächere oder Selbstfragmente zeigen dagegen ein "Slip"‑Verhalten: Sie lösen sich beim Ziehen schneller. T‑Zellen erzeugen solche Kräfte selbst über ihr inneres Skelett aus Aktinfilamenten und Motorproteinen, insbesondere in der engen Kontaktzone, der Immun‑Synapse. Neue molekulare Spannungssonden zeigen, dass Kräfte im Bereich, in dem Catch‑Verhalten auftritt, tatsächlich während der frühen T‑Zell‑Aktivierung vorhanden sind, obwohl verschiedene experimentelle Methoden manchmal unterschiedliche Werte berichten und eine lebhafte Debatte ausgelöst haben.
Selbst von Nichtselbst im Zeitverlauf entschlüsseln
Der Artikel beleuchtet auch, wie T‑Zellen laute, flüchtige Kontaktereignisse in verlässliche Entscheidungen verwandeln könnten. Eine langjährige Idee, das kinetische Proofreading, besagt, dass die Signalübertragung durch eine Abfolge von Schritten verläuft, die Zeit erfordert; nur Fragmente, die den Rezeptor lange genug gebunden halten, erlauben der Kette, einen Punkt ohne Rückkehr zu erreichen. Die Autoren diskutieren, wie mechanische Effekte diesen Zeitfilter schärfen können: Zugkräfte verlängern die Lebensdauer produktiver Bindungen und verkürzen die unproduktiven, wodurch die Lücke zwischen starken und schwachen Stimuli vergrößert wird. Sie betrachten außerdem, wie T‑Zellen viele kurze Kontakte integrieren könnten, statt sich auf einen einzigen langen zu verlassen, und wie Rückkopplungen im Signalnetzwerk eine Art molekularer "Gedächtnis" jüngster Begegnungen speichern können. Diese Verfeinerungen helfen zu erklären, wie T‑Zellen sowohl Geschwindigkeit als auch Genauigkeit in komplexen Gewebeumgebungen erreichen.
Geteilte Prinzipien bei Immunrezeptoren
Obwohl der T‑Zell‑Rezeptor außergewöhnlich hohe Anforderungen erfüllen muss, erscheinen viele seiner Gestaltungsprinzipien auch bei anderen Immunrezeptoren. B‑Zell‑Rezeptoren und Antikörperrezeptoren auf angeborenen Immunzellen teilen ähnliche Signalmotive und operieren oft in Nahkontaktzonen, in denen Überfüllung, Clusterbildung und zytoskelettale Kräfte eine Rolle spielen. Catch‑ähnliche Reaktionen auf Kraft wurden mittlerweile für mehrere solcher Rezeptor‑Ligand‑Paare berichtet. Das deutet darauf hin, dass das Wahrnehmen mechanischer Hinweise eine allgemeine Strategie des Immunsystems sein könnte, um zu prüfen, ob ein Ziel fest verankert, korrekt präsentiert und eine Reaktion wert ist.
Warum das für Gesundheit und Therapien wichtig ist
Für eine allgemein interessierte Leserschaft lautet die Quintessenz: T‑Zellen riechen nicht nur nach fremden Molekülen — sie prüfen auch, wie sich diese Moleküle beim Ziehen anfühlen. Indem Chemie, Physik und Zellbiologie kombiniert werden, argumentiert diese Übersichtsarbeit, dass Immunrezeptoren subtile Unterschiede in Bindung und Kraft in lebensentscheidende Zellantworten umwandeln. Ein tieferes Verständnis dieser mechanobiologischen Regeln könnte die Entwicklung besserer T‑Zell‑basierter Therapien, präziserer Impfstoffe und neuer Behandlungen leiten, die Immunantworten hoch- oder herunterregulieren, indem sie nicht nur verändern, was Rezeptoren binden, sondern wie sie mechanisch eingebunden werden.
Zitation: Travaglino, S., Jeon, Y., Kim, Y. et al. Mechanotransduction through T cell receptors: consensus, controversies and future outlooks. Exp Mol Med 58, 319–335 (2026). https://doi.org/10.1038/s12276-026-01639-w
Schlüsselwörter: T-Zell-Rezeptor, Mechanotransduktion, Catch-Bonds, Immun-Synapse, Kinetische Proofreading