Clear Sky Science · de
UBE2M als Brücke zwischen Neddylierung und Zellzyklusregulation beim kolorektalen Adenokarzinom
Warum diese Forschung für Darmkrebs wichtig ist
Kolorektales Karzinom zählt zu den häufigsten und tödlichsten Krebsarten weltweit, maßgeblich weil Tumorzellen lernen, sich unaufhörlich zu teilen. Diese Studie enthüllt einen bislang verborgenen Schaltmechanismus, der Krebszellen im Darm hilft, eine kritische Kontrollstation der Zellteilung zu durchlaufen. Indem sie aufzeigt, wie dieser Schalter auf molekularer Ebene funktioniert — und dass ein bereits zugelassenes Antipilzmittel ihn stören kann — weist die Arbeit auf eine potenzielle neue Möglichkeit hin, Tumorwachstum zu verlangsamen oder zu stoppen.
Eine verborgene Kontrollschicht innerhalb von Tumorzellen
Zellen teilen sich nicht zufällig; sie durchlaufen einen geordneten Zyklus mit Kontrollpunkten, die prüfen, ob es sicher ist, DNA zu kopieren und sich zu teilen. Krebszellen manipulieren diese Kontrollpunkte häufig. Die Forschenden konzentrierten sich auf einen chemischen Markierungsprozess namens Neddylierung, der Proteine nach ihrer Synthese subtil verändert. Frühere Studien deuteten darauf hin, dass die Neddylierung in vielen Krebsarten verstärkt ist, doch wie sie mit dem Teilungszyklus kolorektaler Krebszellen verknüpft ist, war unklar. Mit Hilfe großer Einzelzell-Datensätze aus humanen Tumoren sowie aggregierten Genexpressionsdaten von mehr als 1.800 Patientinnen und Patienten fanden die Forschenden heraus, dass die Neddylierungsaktivität besonders hoch in malignen Darmszellen ist, die sich in der G2/M-Phase befinden — dem letzten Tor vor der Zellteilung.
Im Fokus: ein molekulares „Brücken“-Protein
Um herauszufinden, welche Moleküle Neddylierung und Zellteilung verbinden, nutzten die Forschenden netzwerkartige rechnerische Analysen, um Tausende von Genen zu durchsieben. Ein Protein trat dabei hervor: UBE2M, ein Enzym, das beim Anheften des kleinen NEDD8-Tags an andere Proteine hilft. UBE2M war in den Daten nicht nur stark mit Neddylierungs- und Zellzykluswegen verknüpft; es wurde auch in deutlich höherer Menge in kolorektalen Tumoren als im umgebenden normalem Gewebe gefunden. Patientinnen und Patienten mit Tumoren, die mehr UBE2M aufwiesen, hatten tendenziell eine schlechtere Überlebensprognose, was es eher zu einem Treiber als zu einem Unbeteiligten macht. Reduzierte man UBE2M in Krebszelllinien und in Maus-Tumormodellen, verlangsamte sich das Tumorwachstum, die Zellteilung nahm ab und mehr Zellen durchliefen programmierte Zellsterbewege. Umgekehrt beschleunigte eine künstliche Überexpression von UBE2M Wachstum und Zellzyklusfortschritt.
Eine Kette, die ein wichtiges wachstumsförderndes Protein schützt
Bei tiefergehenden Untersuchungen fragten die Forschenden, wie UBE2M die Zellteilung fördert. Sie entdeckten, dass UBE2M nicht allein wirkt, sondern eine Kaskade in Gang setzt, an der zwei weitere Proteine beteiligt sind: USP39 und PABPC1. Normalerweise wird PABPC1 durch eine Kette von Ubiquitin-Molekülen markiert und so zum Protein-Recyclingsystem der Zelle geschickt. Die Gruppe zeigte, dass UBE2M USP39 mit dem NEDD8-Tag chemisch modifiziert. Diese Modifikation steigert USP39s Fähigkeit, Ubiquitin-Ketten von PABPC1 abzuschneiden, wodurch PABPC1 vor dem Abbau bewahrt und stabilisiert wird. Mit mehr vorhandenem PABPC1 kann die Zelle bestimmte mRNAs besser in Protein übersetzen, darunter die mRNA für CCNB1, ein Cyclin, das als Beschleuniger für die G2/M-Kontrollstation fungiert. Im Kern stabilisiert UBE2M also PABPC1, was wiederum die Produktion von CCNB1 erhöht und Zellen leichter in die Teilung treibt.
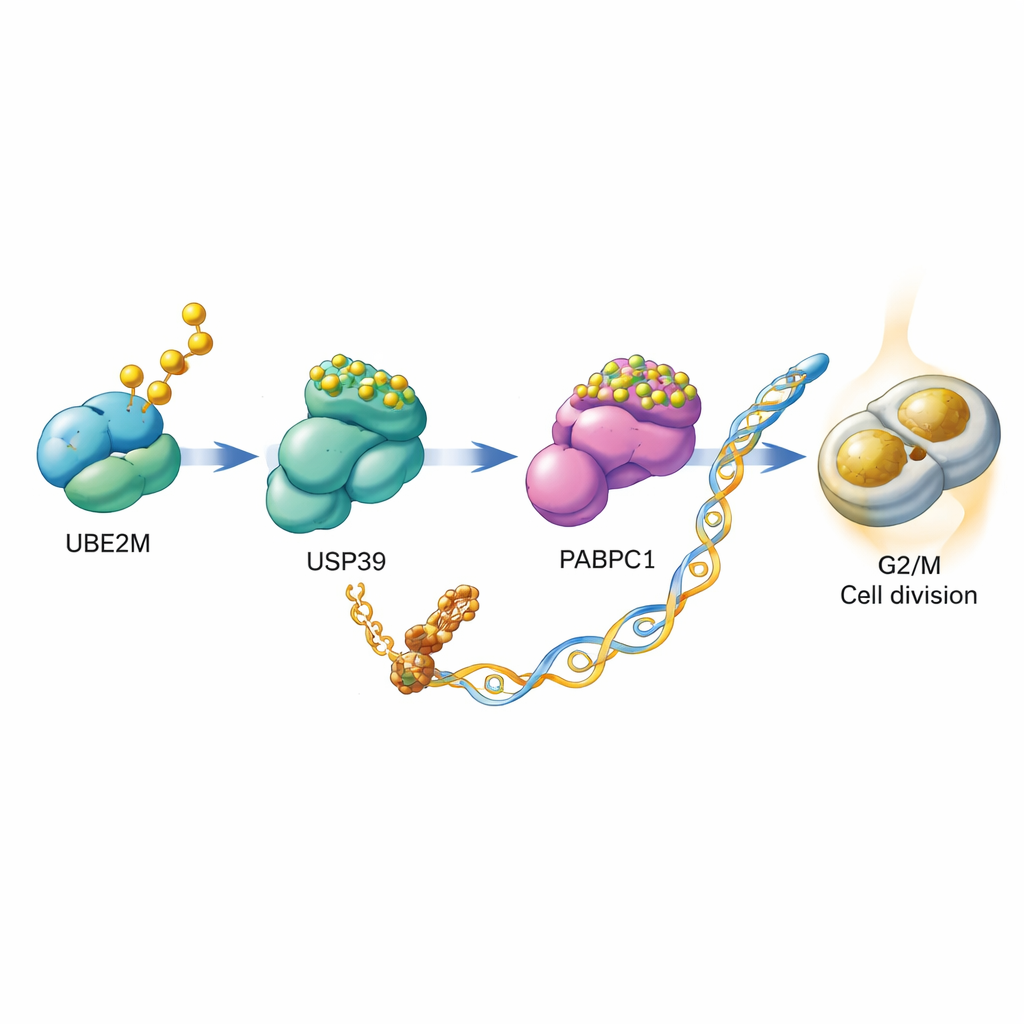
Vom molekularen Mechanismus zur Arzneioption
Die Entdeckung dieser UBE2M–USP39–PABPC1–CCNB1-Kette wies auf eine neue Verwundbarkeit kolorektaler Krebszellen hin. Die Autorinnen und Autoren wandten sich Micafungin zu, einem Medikament, das bereits gegen Pilzinfektionen eingesetzt wird und kürzlich als Inhibitor der neddylierenden Aktivität von UBE2M identifiziert wurde. In im Labor gezüchteten Darmkrebszellen schwächte Micafungin die Neddylierung von USP39, förderte den Abbau von PABPC1 und senkte die CCNB1-Proteinspiegel. Infolgedessen verlangsamte sich die Zellteilung, mehr Zellen blieben an der G2/M-Kontrollstation stehen, und die Apoptose nahm zu. In Mäusen, die mit kolorektalen Krebszellen transplantiert waren, verringerte tägliche Micafungin-Gabe die Tumorgröße signifikant im Vergleich zu unbehandelten Tieren, ohne dass UBE2M selbst entfernt werden musste.
Was das langfristig für Patientinnen und Patienten bedeuten könnte
Diese Arbeit zeichnet ein klares Bild davon, wie ein einzelnes Enzym, UBE2M, ein subtiles Protein-Markierungssystem mit der Entscheidung einer Darmkrebszelle zu teilen verknüpfen kann. Indem UBE2M über USP39 einen Translationsfaktor (PABPC1) stabilisiert, erhöht es indirekt die Menge eines starken Zellzyklustreibers, CCNB1, und ermöglicht so ein schnelleres Tumorwachstum. Obwohl weitere Forschung und klinische Prüfungen nötig sind, deuten die Ergebnisse darauf hin, dass das Blockieren dieser Kaskade — möglicherweise mit umgenutzten Wirkstoffen wie Micafungin — eine neue gezielte Strategie bieten könnte, um das Fortschreiten kolorektaler Karzinome zu bremsen und die Ergebnisse für Patientinnen und Patienten zu verbessern.
Zitation: Wang, Z., Wang, Y., Chen, Y. et al. UBE2M as a bridge spanning neddylation and cell cycle regulation in colorectal adenocarcinoma. Exp Mol Med 58, 501–518 (2026). https://doi.org/10.1038/s12276-026-01636-z
Schlüsselwörter: kolorektales Karzinom, Zellzyklus, Neddylierung, UBE2M, zielgerichtete Therapie