Clear Sky Science · de
Arzneimittelbedingte gastrointestinale Toxizität und Barriereintegrität: zytoskelettvermittelte Beeinträchtigung in einem klinisch relevanten humanen Darmepithelmodell
Warum Darm‑Nebenwirkungen wichtig sind
Viele Medikamente, die gegen Krebs, Entzündungen oder andere Krankheiten eingesetzt werden, können unbeabsichtigt die Auskleidung unseres Darms schädigen. Wenn diese innere "Haut" des Darms verletzt wird, leiden Betroffene an Durchfall, Schmerzen, Übelkeit und schlechter Nährstoffaufnahme — manchmal so stark, dass Ärzte lebensrettende Therapien abbrechen oder reduzieren müssen. Dennoch übersehen heutige Labortests diese Probleme oft, bevor Medikamente Patienten erreichen. Diese Studie stellt ein realistischeres Labor‑Modell des menschlichen Darms vor und zeigt, wie es darm‑schädigende Medikamente früher erkennt und offenlegt, wie sie die natürliche Barriere schwächen.
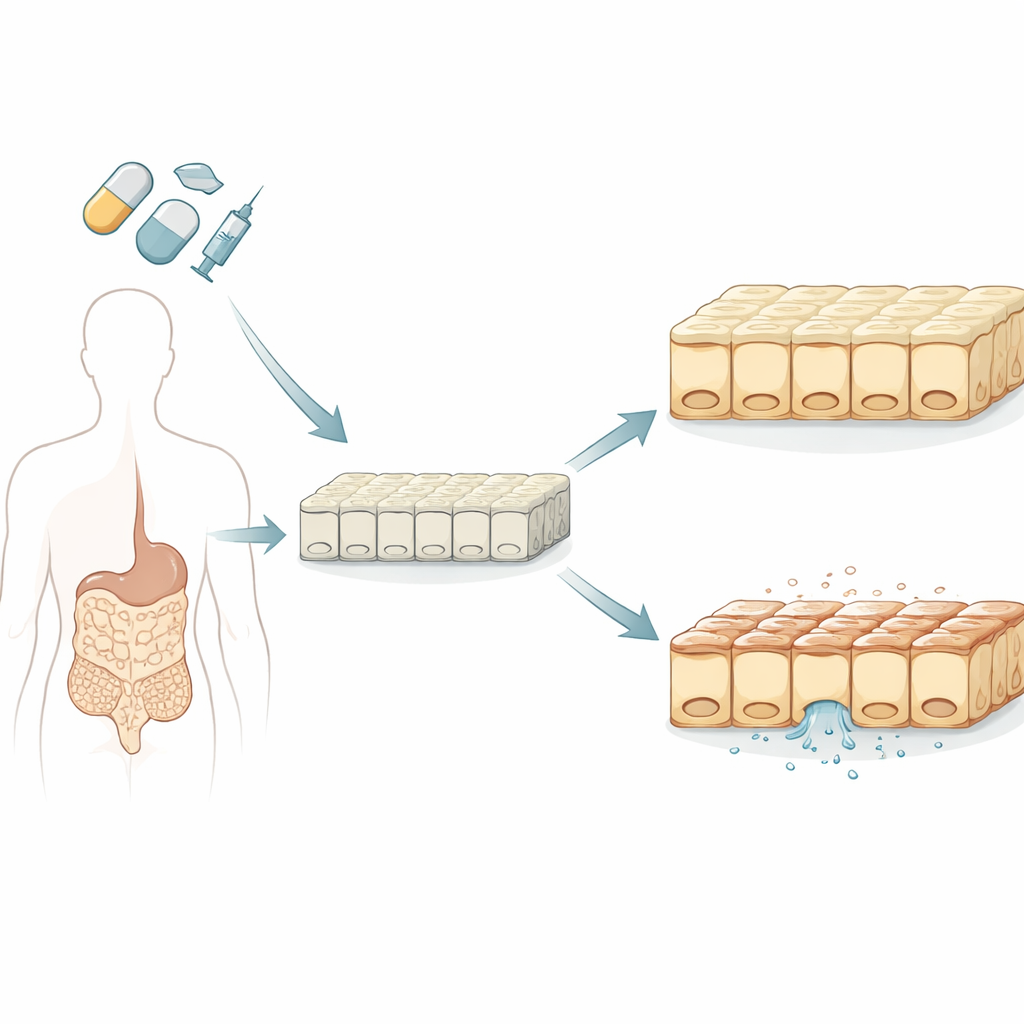
Aufbau eines besseren Mini‑Darms
Die Forschenden begannen damit, Laborschichten aus menschlichen Darmszellen mithilfe von Stammzellen zu kultivieren, die sich zu verschiedenen Gewebetypen entwickeln können. Im Gegensatz zu einer traditionellen, krebsabgeleiteten Zelllinie, die lange Zeit für Arzneimitteltests verwendet wurde, bildeten diese aus Stammzellen gewonnenen Zellen eine gemischte Zellgemeinschaft, die dem echten Dünndarm näherkommt, einschließlich schleimproduzierender und hormonproduzierender Zellen. Das Team bestätigte, dass diese im Labor gezüchteten Schleimhäute realistische Dichtheit, eine ausgeprägte Polarität von oben nach unten sowie zentrale Transport‑ und Stoffwechselfunktionen aufwiesen, die beeinflussen, wie Arzneimittel durch den Darm gelangen und dort verarbeitet werden.
Messen der elektrischen Dichtheit der Barriere
Um die Darmverträglichkeit zu prüfen, konzentrierte sich die Gruppe auf die transepitheliale elektrische Resistenz, kurz TEER, eine nichtinvasive Messgröße dafür, wie gut benachbarte Zellen miteinander abdichten. Hohe TEER steht für eine dichte, schützende Barriere; sinkende TEER bedeutet, dass die Wand zwischen Darm und Blutbahn undicht wird. Die Forschenden verglichen TEER mit einem standardmäßigen Zell‑Überlebenstest, der Energieträger wie ATP misst. Sie setzten sowohl ihr neues Darmmodell als auch das ältere Krebszellmodell 17 Wirkstoffen aus, die unterschiedlich häufig gastrointestinale Nebenwirkungen hervorrufen — darunter gängige Chemotherapeutika, zielgerichtete Krebsmedikamente und Schmerzmittel wie Ibuprofen sowie andere entzündungshemmende Arzneien.
Verborgene Schäden erkennen, bevor Zellen sterben
Über dieses Spektrum an Wirkstoffen hinweg schnitten TEER‑Messungen in der aus Stammzellen abgeleiteten Darmschicht besser ab als der traditionelle ATP‑Test und die ältere Krebszellbarriere. Mehrere Chemotherapeutika zeigten nur geringe Veränderungen im ATP, was suggeriert, dass die Zellen noch lebten, verursachten jedoch große Abfälle der TEER und offensichtliche Schäden in Lebend‑/Tot‑Färbungsbildern. Das bedeutet, dass die Barriere versagen kann, bevor Zellen vollständig absterben — eine frühe Warnung, die klassische Vitalitätstests übersehen. Als das Team seine Laborergebnisse mit klinischen Daten darüber verglich, wie häufig jedes Medikament Darmbeschwerden auslöst, markierte der neue TEER‑Assay fast alle höher‑risikobehafteten Mittel korrekt und bestätigte bei den Niedrigrisiko‑Substanzen die Unbedenklichkeit, womit eine sehr hohe Genauigkeit erzielt wurde.
Wie Medikamente das innere Gerüst untergraben
Um zu ergründen, was in den Zellen schief lief, analysierten die Wissenschaftler die Genaktivität nach der Behandlung mit zwei chemotherapeutischen Wirkstoffen, die Mikrotubuli angreifen — ein zentraler Bestandteil des zellulären Innen‑Gerüsts. Sie fanden weitreichende Verringerungen der Expression von Genen, die am Zytoskelett, an Zell‑zu‑Zell‑Adhäsionen und an der extrazellulären Matrix beteiligt sind — dem Netz, das Zellen hilft, sich an ihrer Umgebung zu verankern. Zusätzliche Experimente zeigten konzentrationsabhängige Zunahmen reaktiver Sauerstoffspezies, instabile sauerstoffhaltige Moleküle, die zelluläre Strukturen schädigen können. Zusammengenommen deuten diese Veränderungen auf eine Kaskade hin, in der bestimmte Medikamente das innere Gerüst und die Verbindungen von Darmzellen stören, die Barriere lockern und dadurch das Zwischenzell-Lecken von Substanzen ermöglichen.
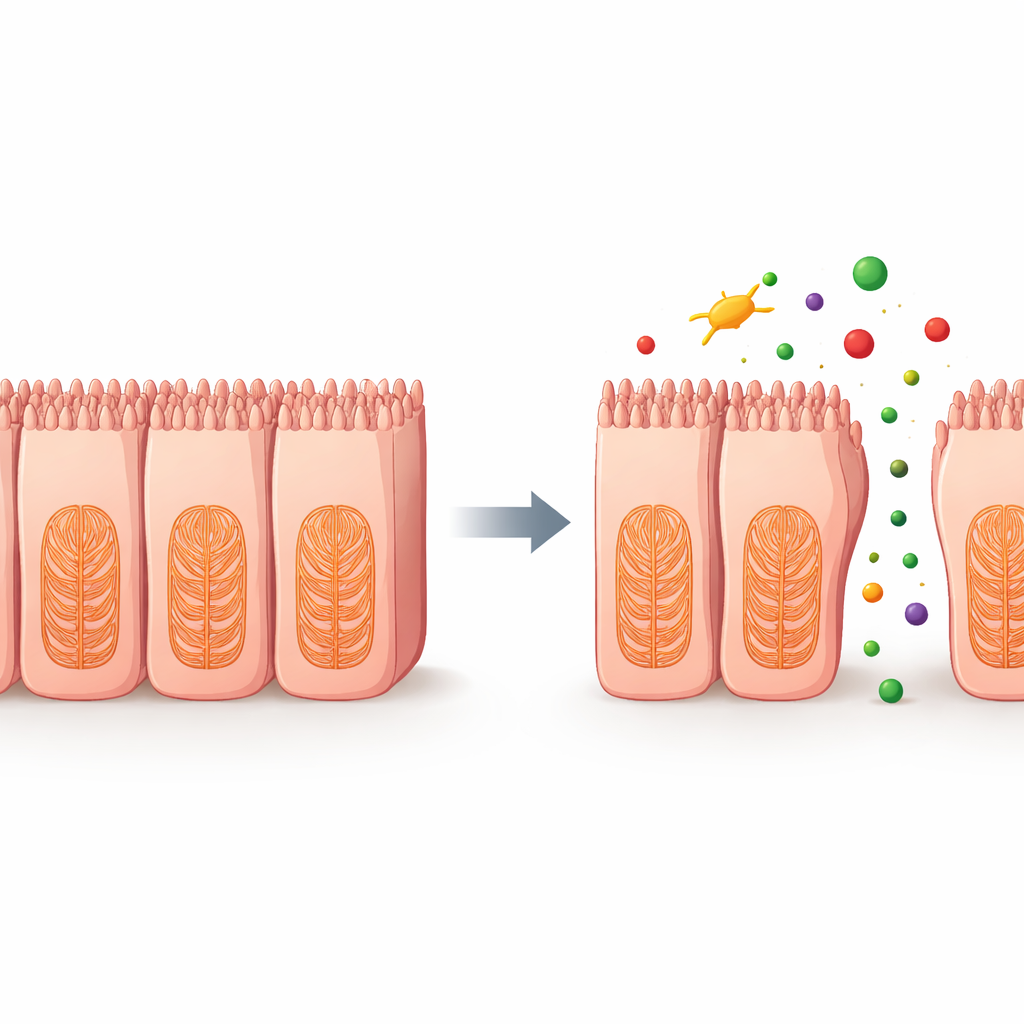
Was das für Patientinnen und Patienten bedeutet
Diese Arbeit zeigt, dass ein auf Stammzellen basierendes menschliches Darmepithel in Kombination mit einfachen elektrischen Messungen der Barrieredichtheit zuverlässiger vorhersagen kann, welche Medikamente wahrscheinlich Darmverletzungen verursachen, als langjährig verwendete Labormethoden. Indem es eine Schwächung der Barriere früh erkennt — und sie mit zugrunde liegenden Schäden am zellulären Gerüst verknüpft — kann diese Plattform Arzneimittelentwicklerinnen und ‑entwickler dabei unterstützen, riskante Verbindungen auszusortieren oder neu zu gestalten, bevor sie in die Klinik gelangen. Langfristig könnten solche realistischen "Mini‑Darm"‑Tests unangenehme oder gefährliche gastrointestinale Nebenwirkungen für Patientinnen und Patienten verringern und gleichzeitig erlauben, wirksame Therapien sicherer einzusetzen.
Zitation: Yu, W.D., Lee, S., Cho, HS. et al. Drug-induced gastrointestinal toxicity and barrier integrity: cytoskeleton-mediated impairment in a clinically relevant human intestinal epithelium model. Exp Mol Med 58, 487–500 (2026). https://doi.org/10.1038/s12276-025-01635-6
Schlüsselwörter: gastrointestinale Toxizität, Darmbarriere, Stammzellmodell, Arzneimittelsicherheit, Nebenwirkungen von Chemotherapien