Clear Sky Science · de
Zwei Codes der RNA‑Bearbeitung durch Desaminierung bei menschlichen Krankheiten
Wie Zellen ihre eigenen Botschaften umschreiben
Jede Zelle in Ihrem Körper liest ständig Anweisungen aus der DNA, um Ihnen Form und Funktion zu verleihen. Jahrzehntelang nahm man an, diese Anweisungen würden in RNA kopiert und dann treu in Proteine übersetzt. Dieser Übersichtsartikel zeigt, dass die Wirklichkeit deutlich flexibler ist: Zellen „schreiben“ viele RNA‑Botschaften nach ihrer Entstehung um und tauschen einzelne chemische Buchstaben aus, was feinere oder gravierende Änderungen der Körperfunktionen bewirken kann. Das Verständnis dieser verborgenen Bearbeitungsebene hilft zu erklären, warum Menschen Autoimmunerkrankungen, neurologische Störungen, Stoffwechselprobleme, Infektionen und Krebs entwickeln und wie man sie möglicherweise behandeln könnte.
Zwei Wege, einen einzelnen Buchstaben zu verändern
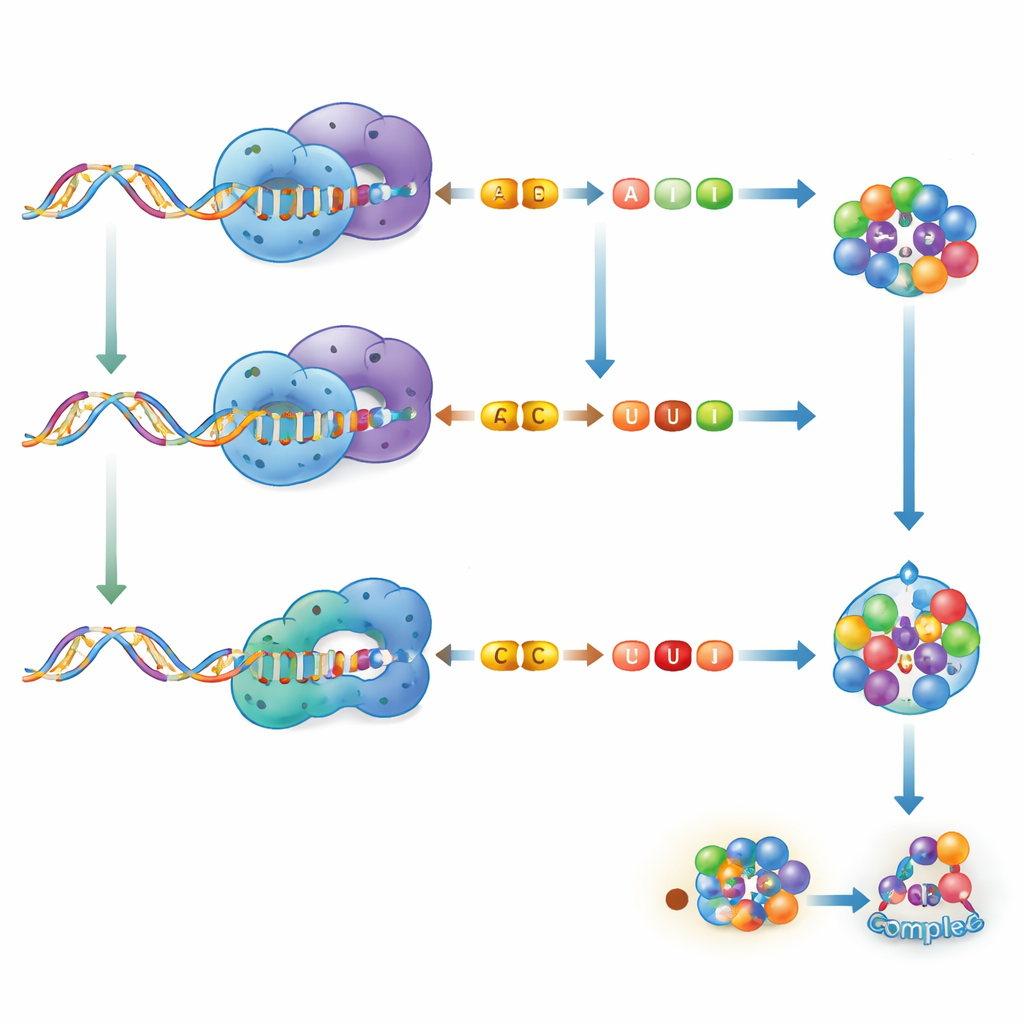
Die Autoren konzentrieren sich auf zwei Haupttypen der RNA‑Bearbeitung beim Menschen. Der eine heißt A‑zu‑I‑Editing und wird von Enzymen der ADAR‑Familie durchgeführt. Sie wandeln die Base Adenosin (A) in Inosin (I) um, das die zelluläre Maschinerie größtenteils wie Guanosin (G) liest. Der andere ist C‑zu‑U‑Editing, vermittelt durch Enzyme der APOBEC‑Familie, die Cytidin (C) in Uridin (U) umwandeln. Beide Prozesse entfernen eine kleine chemische Gruppe von einer einzelnen Base, unterscheiden sich aber darin, wo sie wirken, welche RNAs sie bevorzugen und wie stark sie die RNA‑Struktur umformen. A‑zu‑I‑Editing verändert oft die Paarung von RNA‑Strängen und kann Proteine diversifizieren oder die Bindung anderer Moleküle an RNA verändern. C‑zu‑U‑Editing wirkt strukturell tendenziell subtiler, kann aber dennoch Stopp‑Signale einführen, Proteinsequenzen anpassen oder regulatorische Regionen der RNA feinabstimmen.
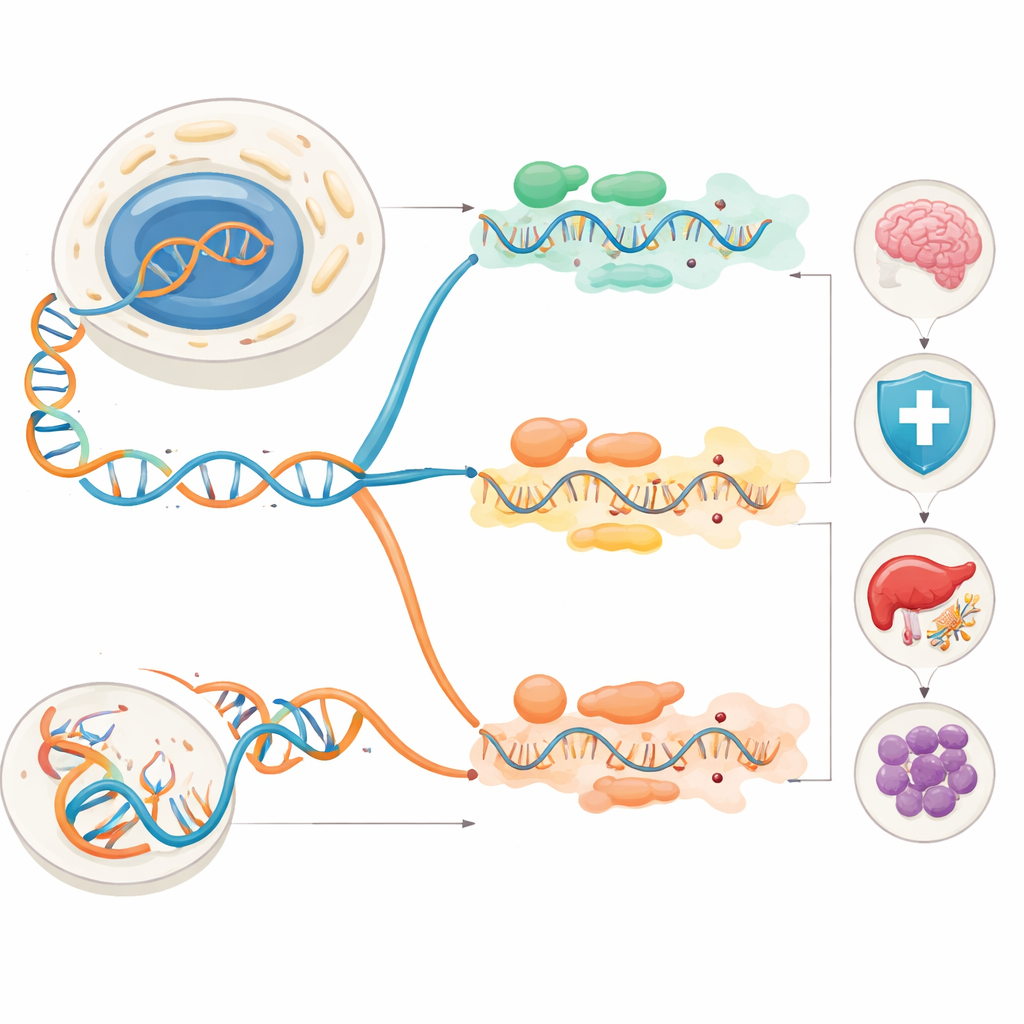
Von bearbeiteten Botschaften zu Gesundheit und Krankheit
Weil diese Editierungen Proteinabschnitte oder deren regulatorische Regionen verändern können, betreffen sie viele Aspekte der normalen Biologie. Im Immunsystem bearbeitet ADAR1 selbst erzeugte doppelsträngige RNAs, damit virale Sensoren sie nicht fälschlich als Fremdkörper erkennen. Versagt ADAR1, bleiben Immunalarme dauerhaft „an“, was zu chronischer Interferon‑Signalisierung und Autoimmunerkrankungen wie dem Aicardi–Goutières‑Syndrom führt. APOBEC‑Enzyme editieren ebenfalls RNA in Immunzellen, beeinflussen, wie Makrophagen auf Stress und Entzündung reagieren, und können zu Erkrankungen wie systemischem Lupus beitragen. Im Nervensystem ist das ADAR2‑Editing entscheidend für die Feinabstimmung von Gehirnrezeptoren, die den Calciumfluss steuern; ohne dieses Editing leiden Mäuse unter Anfällen und sterben früh. APOBEC‑vermitteltes Editing bestimmter Rezeptor‑RNAs in Neuronen kann deren Empfindlichkeit erhöhen und steht im Zusammenhang mit Epilepsie, Degeneration und kognitiven Problemen.
Viren, Stoffwechsel und die Verbindung zu Krebs
RNA‑Editing beeinflusst auch den Umgang mit Viren, die Energieverwaltung und die Krebsentstehung. ADAR1 kann virale Genome direkt editieren, wodurch das Virus manchmal geschwächt wird, in anderen Fällen — etwa beim Hepatitis‑Delta‑Virus — seine Lebenszyklen kompletterlaufen. APOBEC‑Enzyme, bekannt für ihre Aktivität gegen Retroviren, hinterlassen ein ausgeprägtes C‑zu‑U‑Muster in der RNA von SARS‑CoV‑2, begrenzen damit das Virus, erzeugen aber gleichzeitig Mutationen, die der viralen Evolution dienen können. Im Stoffwechsel hilft ADAR2 den pankreatischen Beta‑Zellen, die Insulinsekretion an die Ernährung anzupassen, während ADAR1‑ und ADAR2‑Aktivität das Diabetesrisiko und Fettleber beeinflussen. Die klassische Rolle von APOBEC1 ist das Editing der RNA für Apolipoprotein B, wodurch ein verkürztes Protein entsteht, das für den Transport von Nahrungsfetten essenziell ist; fehlt dieses Editing, entwickeln Mäuse schwere Lipid‑ und Cholesterinprobleme.
Wie bearbeitete RNA Tumoren formt
Die gleichen Enzyme, die uns schützen, können bei Fehlregulierung Krebs fördern. Große Krebssequenzierungsprojekte haben Zehntausende A‑zu‑I‑Editing‑Stellen und weitverbreitete APOBEC‑assoziierte Mutationen aufgedeckt. Beim Brustkrebs kann ADAR1‑Editing je nach Ziel‑RNA das Tumorverhalten antreiben oder hemmen und Einfluss auf Zellinvasion, Metastasierung und Überleben haben. Im Glioblastom, einem tödlichen Hirntumor, unterstützt ADAR1 krebsartige Stammzellen, während ADAR2 allgemein als Wachstumspuffer wirkt, indem es sowohl proteincodierende RNAs als auch krebsfördernde microRNAs editiert. In Leukämien fördert ADAR1 oft maligne, stammpzellähnliche Populationen und dämpft tumorunterdrückende microRNAs, während ADAR2 spezifische Ziele so editiert, dass das Fortschreiten gebremst wird. APOBEC‑vermitteltes C‑zu‑U‑Editing bestimmter RNAs in Bluttumoren kann die Patientenprognose verschlechtern oder verbessern — ein Hinweis auf die starke Kontextabhängigkeit dieser Veränderungen.
Offene Fragen und künftige Möglichkeiten
Trotz einer Flut katalogisierter Editierungsstellen fällt es Wissenschaftern noch schwer, aussagekräftige Edits von Hintergrundrauschen zu trennen. Viele detektierte Veränderungen mögen wenig Wirkung haben, doch eine Minderheit hat eindeutig lebenswichtige Konsequenzen für Zellen und Organismen. Die Autoren plädieren dafür, künftig genau zu bestimmen, welche Enzyme und Hilfsproteine einzelne Stellen steuern, und dann zu testen, welche Folgen es hat, wenn diese Basen gezwungenermaßen immer oder niemals editiert werden. Solche Studien werden klären, wie RNA‑Editing zu bestimmten Krankheiten beiträgt, und zeigen, ob die Anpassung von Editing‑Mustern zu einer neuen Klasse präziser Therapien werden kann — sei es zur Beruhigung eines überaktiven Immunsystems, zur Feinabstimmung neuronaler Schaltkreise, zur Korrektur metabolischer Ungleichgewichte oder zur Erhöhung der Verwundbarkeit von Tumoren gegenüber Therapien.
Warum das für die alltägliche Gesundheit wichtig ist
Kurz gesagt zeigt dieser Artikel, dass unsere Zellen den genetischen Code nicht nur lesen; sie lektorieren und überarbeiten ihn aktiv auf der RNA‑Ebene mit zwei parallelen „Editiercodes“. Treten diese winzigen Änderungen am richtigen Ort und im richtigen Maß auf, helfen sie, das Immunsystem im Gleichgewicht zu halten, die Gehirnfunktion stabil, den Stoffwechsel anpassungsfähig und die Abwehr gegen Viren scharf zu halten. Ist die Editiermaschinerie überaktiv, fehlgeleitet oder beschädigt, können dieselben Änderungen uns in Richtung Autoimmunität, Infektion, Demenz, Stoffwechselerkrankung oder Krebs treiben. Durch das Kartieren und Verstehen dieser Ein‑Buchstaben‑Umschreibungen hoffen Forscher, Krankheiten früher zu diagnostizieren, Risikopersonen zu identifizieren und schließlich Behandlungen zu entwickeln, die den Editierprozess wieder in Richtung Gesundheit lenken.
Zitation: Min, D.J., Lee, S., Lee, Ys. et al. Two codes of RNA editing by deamination in human diseases. Exp Mol Med 58, 382–395 (2026). https://doi.org/10.1038/s12276-025-01633-8
Schlüsselwörter: RNA‑Editing, ADAR, APOBEC, Autoimmunität, Krebs