Clear Sky Science · ar
كشف مؤشرات حيوية لمرض الزهايمر بحساسية فائقة باستخدام مجسّات حيوية فوتونيّة نانويّة على أعمدة دقيقة
لماذا يهم اختبار دم بسيط لفقدان الذاكرة
مع ظهور أدوية جديدة يمكنها إبطاء تقدم مرض الزهايمر، بات الأطباء بحاجة ماسة إلى اختبارات بسيطة تكشف من هم في خطر طويلًا قبل أن تظهر الأعراض بوضوح. اليوم، تأكيد تشخيص الزهايمر عادة ما يتطلب تصويرًا دماغيًا مكلفًا أو بزلًا قطنيًا لا يخضع له معظم الناس في الرعاية الروتينية. تصف هذه الدراسة مجسًا صغيرًا يعمل بالضوء يمكنه كشف جزيئات مرتبطة بالزهايمر في قطرة دم بمستويات ذات دلالة سريرية، مما يمهد الطريق لاختبارات سريعة ومنخفضة التكلفة قد تُستخدم في العيادات اليومية أو حتى بجانب السرير.
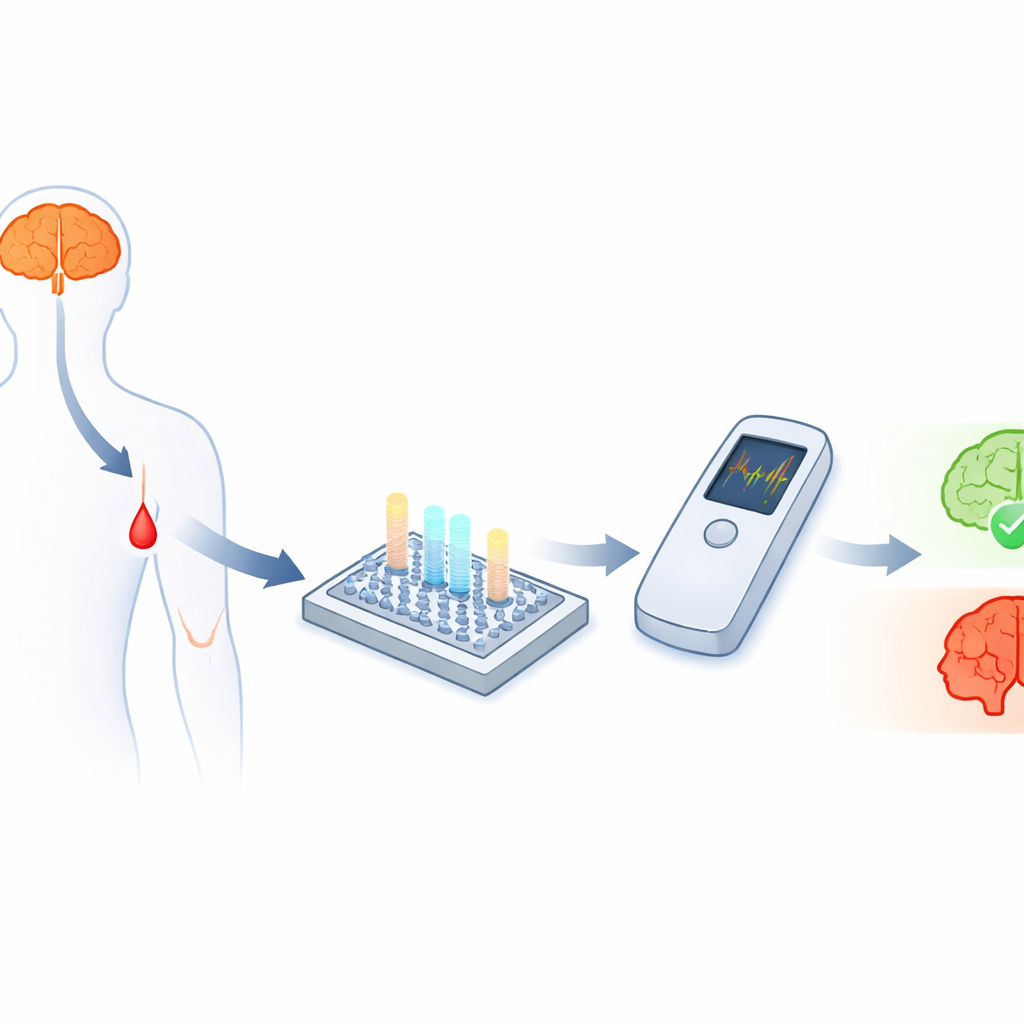
البحث عن أدلة في الدم
يرتبط مرض الزهايمر ارتباطًا وثيقًا بشظايا بروتينية صغيرة تُسمى أميلويد‑بيتا، خاصة شكلين يعرفان باسم Aβ40 وAβ42. تحمل كمياتهما، وخصوصًا نسبتهما، دلائل مهمة حول وجود المرض ومدى تقدمه. والتحدي هو أن هذه الشظايا صغيرة جدًا وتدور في الدم بمستويات منخفضة للغاية—تريليون من الغرام لكل مليلتر—مما يجعل قياسها بدقة خارج المختبرات المتخصصة صعبًا للغاية. وبينما يمكن للمستشعرات الكهروكيميائية نظريًا رصد مثل هذه التركيزات المنخفضة، فإن تحويلها إلى اختبارات نقطية قوية وبأسعار معقولة قادرة على تتبع عدة مؤشرات حيوية في آن واحد أثبت أنه صعب.
توجيه الضوء عبر أعمدة دقيقة
واجه الفريق هذا التحدي باستخدام النانوفوتونيك—هياكل تتحكم بالضوء على مقياس أصغر من طول موجته. بنوا رقاقة مغطاة بشبكة منتظمة من أزواج أعمدة رفيعة جدًا من السيليكون على الزجاج. عندما يسقط الضوء على هذه السطح المنقوش، يُحاصر في وضع رنان خاص يكون حساسًا للغاية للتغيرات قرب قمم الأعمدة، تمامًا كما يتغير صوت شوكة رنانة إذا أضيفت مادة إليها. من خلال ضبط المسافة بين الأعمدة في كل زوج بعناية، وزّن الباحثون ثلاث خصائص حاسمة في آن واحد: مدى حدة الرنين البصري، ومدى تغيره مع المحيط، وحجم الإشارة الناتجة. هذا التصميم عند "النقطة المثلى" يجعل الرقاقة ملائمة بشكل خاص لاستشعار كميات ضئيلة من المادة.
جعل الجزيئات غير المرئية مرئية
حتى مع هذا التصميم المحسّن، لن تُحدث مؤشرات الزهايمر وحدها سوى إزعاج طفيف للضوء. لتضخيم التأثير، استخدم الباحثون استراتيجية على شكل ساندويتش مع جسيمات ذهبية نانوية. أولًا، غطّوا سطح المستشعر بطبقات من كيمياء لاصقة توجه الأجسام المضادة المتخصصة بحيث تكون مواقع الربط متجهة إلى السائل. تلتقط هذه الأجسام المضادة إما Aβ40 أو Aβ42 من العيّنة. بعد ذلك، تُدفق جسيمات ذهبية مزينة بكل منها بجسم مضاد ثانٍ يتعرّف على نهاية مختلفة من نفس شظية الأميلويد على الرقاقة. كلما وُجدت شظية أميلويد، تُشكّل جسرًا بين السطح والجسيم الذهبي، مُعلنةً بذلك وجودها. وبما أن الذهب يغير بيئته البصرية المحلية بقوة، فإن كل شظية محتجَزة تُحدث انزياحًا أكبر بكثير في رنين المستشعر مقارنة بالببتيد لوحده، مما يزيد الحساسية بحوالي درجة إلى درجتين ويفضل الحفاظ على إشارة بصرية نظيفة.
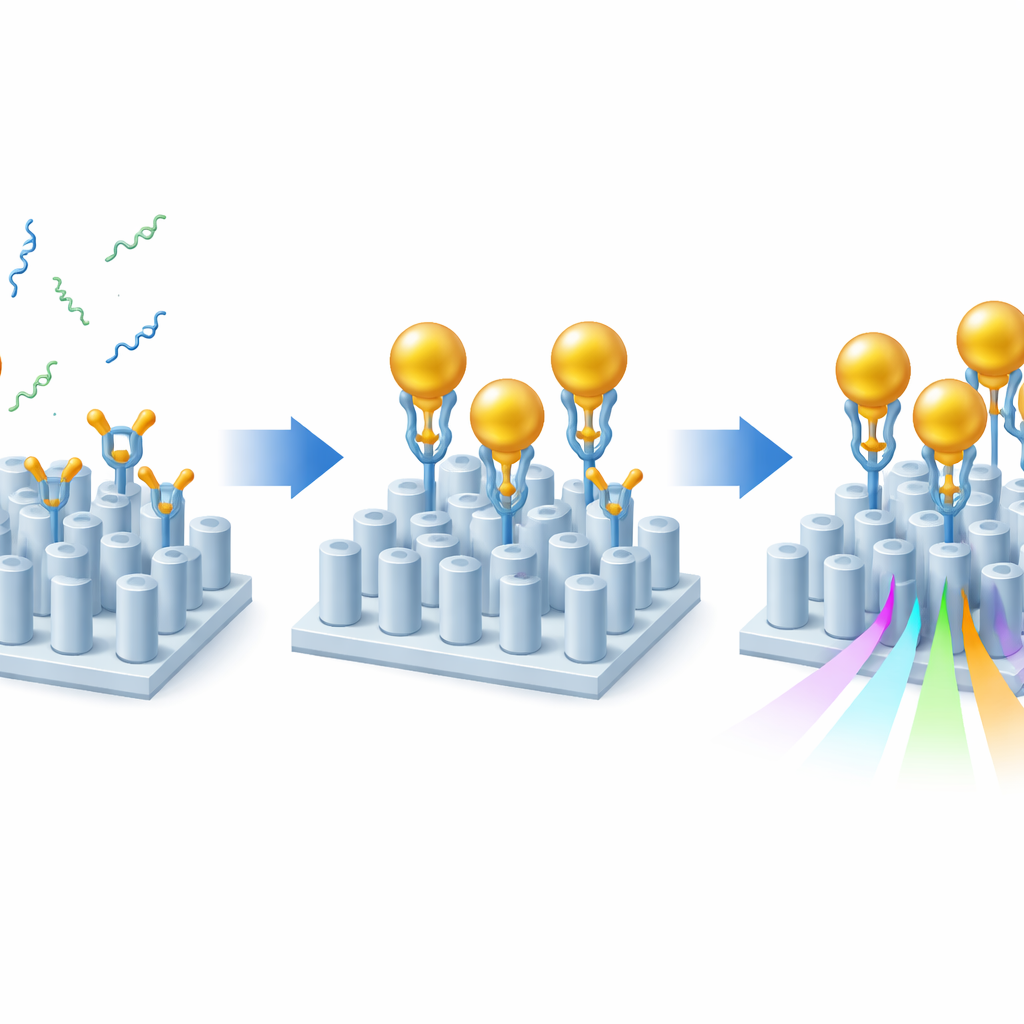
اختبار عينات واقعية
لإظهار أن النهج يعمل خارج محاليل المختبر البسيطة، اختبر الفريق مستشعرهم بمصل دم بشري. قاموا بتخفيف المصل ليتوافق مع التعامل الميكروفلويدي مع الحفاظ على مستويات الأميلويد ممثلة لتلك الموجودة لدى المرضى. والأهم من ذلك، تمكنوا من كشف كل من Aβ40 وAβ42 عند 0.2 بيكوغرام لكل مليلتر في هذا المصل المخفف—ما يعادل المستوى السريري ذي العلاقة وهو 20 بيكوغرامًا لكل مليلتر في الدم الكامل. من خلال وضع أضداد التقاط مختلفة في مناطق منفصلة على نفس الرقاقة، قاسوا الشكلين من الأميلويد في آن واحد داخل قناة صغيرة واحدة، وهي خطوة رئيسية نحو تقييم نسبتهما من عينة صغيرة واحدة. ميزت الإشارات بوضوح العينات المغشوشة بمزيد من الأميلويد عن تلك التي تحتوي فقط على مستويات الخلفية الطبيعية الموجودة حتى لدى الأشخاص الأصحاء.
ماذا قد يعني هذا لرعاية المستقبل
تُظهر هذه التقدّمات مجتمعة أن مستشعرًا مدمجًا يعمل بالضوء، مدعومًا بجسيمات ذهبية نانوية، يمكنه الوصول إلى الحساسية اللازمة لاختبارات دم ذات مغزى للزهايمر مع التعامل مع أكثر من مؤشر حيوي في آن واحد. وعلى الرغم من أن هناك حاجة إلى عمل إضافي لتحويل هذا إلى جهاز تجاري متين ولإضافة علامات أخرى مثل أشكال بروتين تاو، فإن التكنولوجيا الأساسية مبنية من مواد قابلة للتوسع ويمكن إقرانها بأبصار بسيطة محمولة باليد. إذا نُفِّذت بالكامل، فقد تتيح للأطباء مراقبة صحة الدماغ باستخدام عينة دم صغيرة فقط، مما يسهل كثيرًا الكشف المبكر عن الزهايمر وتتبع مدى فاعلية العلاجات مع مرور الوقت.
الاستشهاد: Guilherme S. Arruda, Katie Morris, Augusto Martins, Yue Wang, Sian Sloan-Dennison, Duncan Graham, Steven D. Quinn, Emiliano R. Martins, and Thomas F. Krauss, "Ultrasensitive Alzheimer’s disease biomarker detection with nanopillar photonic crystal biosensors," Optica 12, 1587-1596 (2025). https://doi.org/10.1364/OPTICA.566672
الكلمات المفتاحية: اختبار دم للزهايمر, مستشعر حيوي نانوفوتوني, أميلويد بيتا, جسيمات الذهب النانوية, التشخيص المبكر