Clear Sky Science · ar
الأصل رباعي البنية لتَخَثُّر هيموغلوبين المنجلي: دراسة ديناميكيات جزيئية
لماذا تهمنا هذه الحكاية الدموية
يبدأ مرض الخلايا المنجلية بتغيير طفيف في بروتين دموي واحد، ومع ذلك يمكن لهذا التغيير أن يعيد تشكيل خلايا الدم الحمراء، يسد الأوعية الدموية، ويسبب ألماً مستمراً مدى الحياة. تنظر هذه الدراسة عن كثب وبمنظار فيزيائي إلى كيفية جعل ذلك التغيير الوحيد للبروتين الهيموغلوبين يتكدس ليشكل أليافاً صلبة داخل الخلية. من خلال استخدام محاكيات حاسوبية متقدمة، يربط المؤلفون التفاصيل الذرية بمشكلات الخلية الكاملة، مقدمين دلائل جديدة حول كيفية منع أدوية مستقبلية للهيموغلوبين من أن تعطل مجرى الدم.
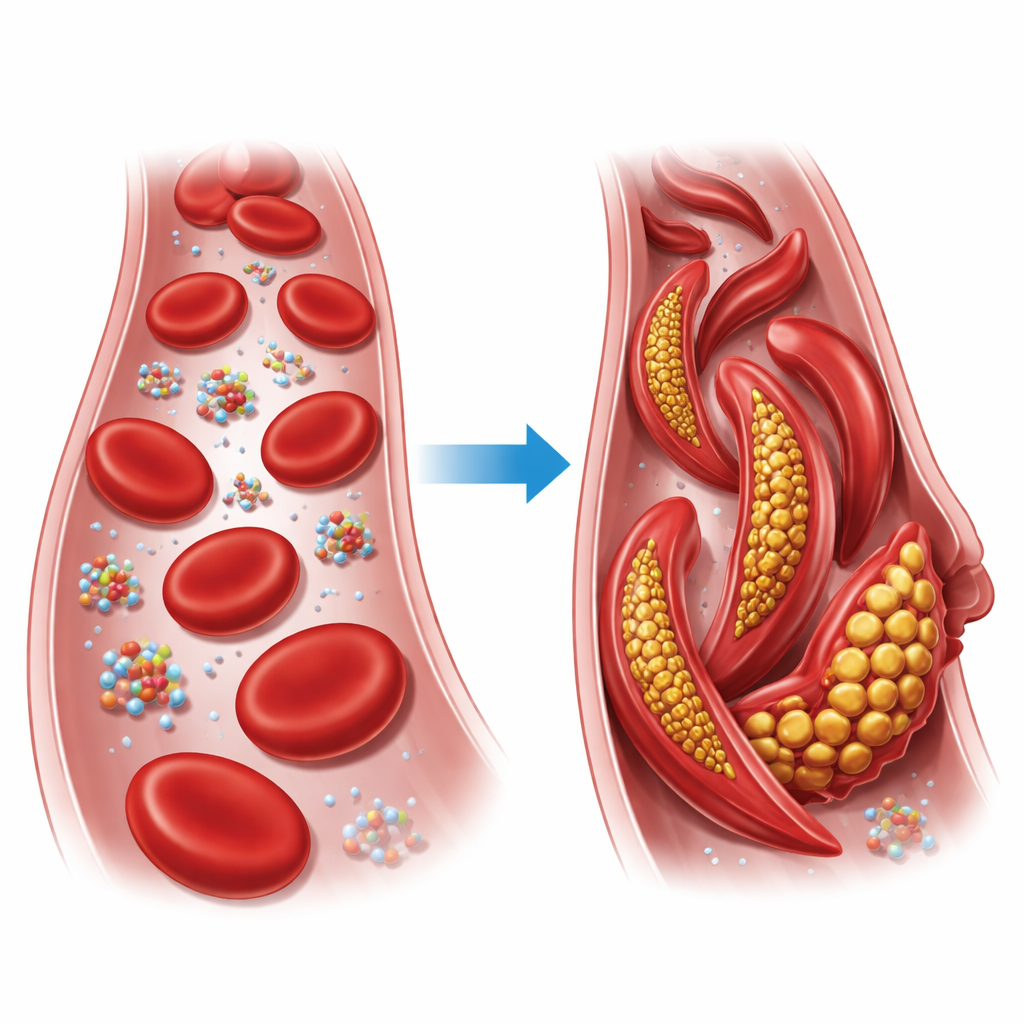
استبدال صغير بعواقب كبيرة
الهيموغلوبين هو البروتين الحامل للأكسجين الذي يملأ خلايا الدم الحمراء. كل وحدة هيموغلوبين مبنية من أربع سلاسل يمكن أن ترتب نفسها في شكلين عامَّين رئيسيين، يعرفان بالحالة المسترخية (R) والحالة المتوترة (T). في مرض الخلايا المنجلية، يتحول لبنة واحدة فقط في إحدى هذه السلاسل: حمض الغلوتاميك المشحون يُستبدل بفالين الدهني في الموضع السادس من سلسلة بيتا. تحت ظروف الأكسجين المنخفضة، يرتبط هذا الشكل المعدل، المسمى هيموغلوبين المنجلي، ليشكّل أليافًا طويلة تُشوّه خلايا الدم الحمراء المستديرة إلى أشكال صلبة تشبه المنجل، والتي يمكن أن تسد الأوعية الصغيرة وتحرم الأنسجة من الأكسجين.
متابعة تغير شكل الهيموغلوبين
يركز المؤلفون على كيفية دوران ووضع وحدات الهيموغلوبين الكاملة معاً داخل الليف. يتتبعون هذا التغير واسع النطاق في الشكل بزاوية واحدة تقيس كيفية التواء نصفَي البروتين بالنسبة لبعضهما. باستخدام محاكاة الديناميكيات الجزيئية — تجارب افتراضية تحسب كيف تتحرك الذرات مع مرور الوقت في الماء والملح — يدفعون هذه الزاوية بلطف عبر نطاق واسع ويحسبون مقدار الطاقة اللازمة لكل شكل. يجدون أن كلاً من الهيموغلوبين الطبيعي والمنجلي يمكن أن يستكشفا العديد من هذه الأشكال عند درجة حرارة الجسم. يظهر هيموغلوبين المنجلي تفضيلاً زاويًا طفيفًا، لكن تفضيلات الشكل هذه وحدها لا تكفي لتفسير لماذا يتكوَّن الليف المستقر فقط من الشكل المنجلي.
لماذا تلتصق ألياف المنجل وتتفكك ألياف الطبيعي
للوصول إلى جوهر تكوين الليف، تقيس الدراسة مدى قوة جذب وحدات الهيموغلوبين المجاورة بعضها لبعض على طول الليف وعبره. تحسب المجموعة طاقة التماسك — السحب الصافي الذي يمسك الوحدات معًا — لعدة أشكال عامة مختلفة. في حالة هيموغلوبين المنجلي، تبقى هذه طاقة التماسك سالبة (مما يعني تجاذباً) عبر النطاق الكامل للأشكال التي اختبروها، لذا تظل الألياف مستقرة ولا تنهار بسهولة. في المقابل، لدى الهيموغلوبين الطبيعي بعض الأشكال التي تظهر طاقة تماسك موجبة، مما يجعل الألياف عند تلك الزوايا غير مستقرة ومعرضة للتفكك التلقائي. الاختلاف الرئيسي هو كيفية انغماس مجموعات الفالين الدهنية المتحولة في البروتينات المجاورة: في الهيموغلوبين المنجلي، تشكّل هذه البقع الدهنية تلامسات قوية سواء جانبياً أو على طول محور الليف، مما يعزز مباشرة نمو الليف.
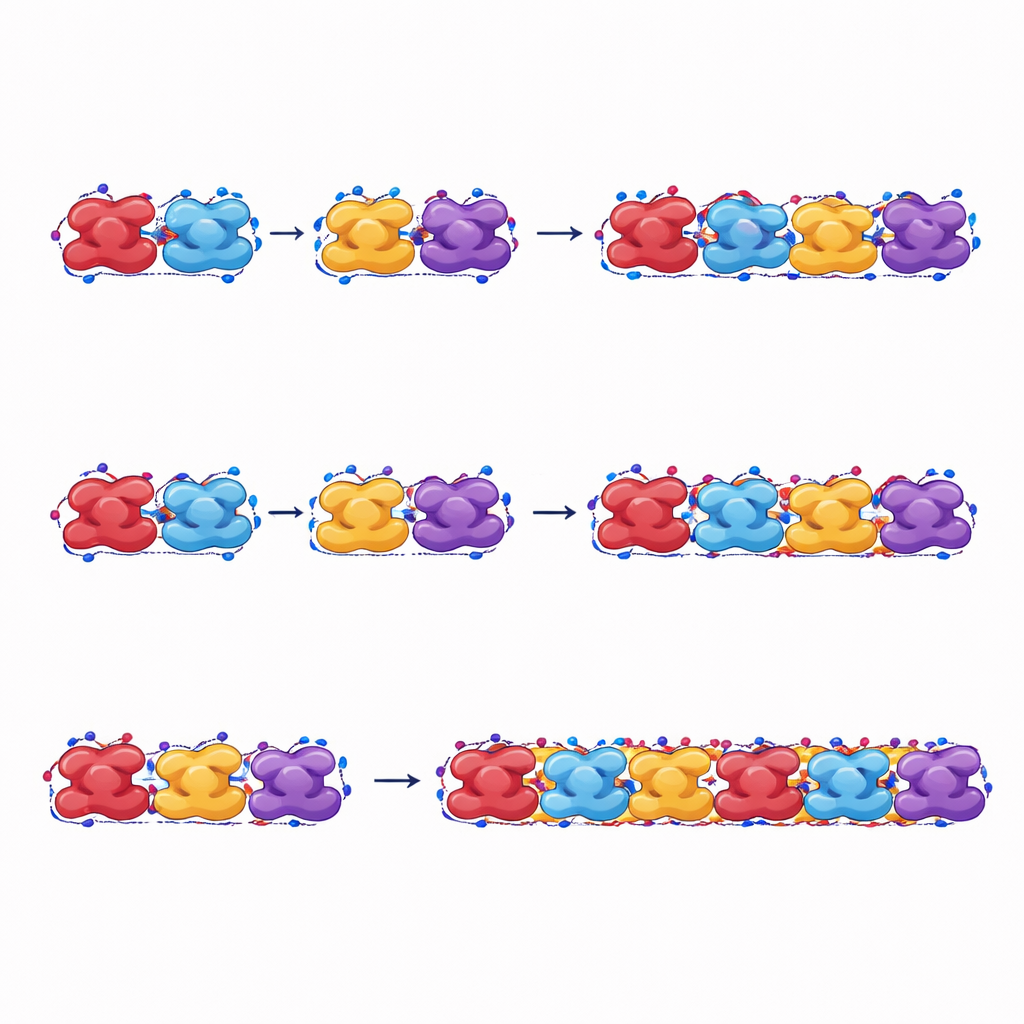
كيف تتحمّل هذه الألياف الحمولة وكيف تنكسر
كما يقوم المؤلفون بتمطيط أليافهم المحاكاة لتقليد الضغط الميكانيكي. عند السحب على طول طولها، تتحمل الألياف المصنوعة من هيموغلوبين المنجلي قوى وانفعالات أعلى وتبدد طاقة أكثر قبل الانهيار مقارنة بتلك المصنوعة من الهيموغلوبين الطبيعي. حتى الشكل المسترخِي من ألياف المنجل، الذي ليس الشكل الذي تظهر فيه الألياف أولاً، يمكنه الحفاظ على السلسلة من خلال تغيرات بلاستيكية في الشكل، مما يساعد على بقاء الليف متماسكًا بعد تكونه. أما ألياف الهيموغلوبين الطبيعي، فيتفكك اتصالها بسهولة أكبر بين الوحدات المجاورة وتمتص طاقة أقل قبل الفشل، مؤكدًا أنها أقل استقرارًا تحت الإجهاد.
دلائل لعلاجات مستقبلية ومواد جديدة
تُظهر المحاكاة مجتمعة أن تغيير حمض أميني واحد يعيد تشكيل الطريقة التي تلتقي بها وحدات الهيموغلوبين، مُلوِّحًا بالتفاف التجميع العام إلى زوايا تُفضّل التجاذب القوي، خصوصاً في الحالة المتوترة. يتيح هذا الجمع من الهندسة واللزوجة لهيموغلوبين المنجل تكوين ألياف طويلة وصلبة تقاوم كلًا من الحركة الحرارية والسحب الميكانيكي، مما يشوّه خلايا الدم الحمراء ويعيق تدفق الدم. من خلال الإشارة إلى خصائص محددة في ترتيب البروتين الكلي التي تتحكم في استقرار الليف، تقترح الدراسة أن الأدوية المضادة للمنجل قد تعمل عن طريق دفع الهيموغلوبين نحو أشكال تصبح فيها الألياف غير مرغوبة من الناحية الطاقية وهشة ميكانيكيًا — محولةً هذا الانسداد الجزيئي القاتل إلى تيار دموي متدفق بحرية.
الاستشهاد: Jiang, M., Qin, Z. The quaternary structure origin of the fibrillation of sickle hemoglobin: a molecular dynamics study. npj Soft Matter 2, 7 (2026). https://doi.org/10.1038/s44431-026-00019-8
الكلمات المفتاحية: مرض الخلايا المنجلية, ألياف الهيموغلوبين, تجَمُّع البروتينات, ديناميكيات جزيئية, اضطرابات دموية