Clear Sky Science · ar
جسر الفجوة بين الحوسبة والتجارب: الاستفادة من نماذج اللغة الكبيرة لتحديد أولويات علاجات مرض ألزهايمر بناءً على مقارنة نماذج التعلم
لماذا يهم هذا العائلات والمرضى
يسلب مرض ألزهايمر الناس ذاكرتهم واستقلاليتهم وجودة حياتهم، ومع ذلك لا تزال العلاجات الفعالة نادرة. تستكشف هذه الدراسة طريقة أسرع للعثور على علاجات جديدة باستخدام أدوية موجودة بالفعل، من خلال الجمع بين نماذج حاسوبية قوية ونموذج لغة كبير — نفس نوع الذكاء الاصطناعي المستخدم الآن في الدردشات اليومية — لتمشيط كميات هائلة من البيانات الطبية والأوراق البحثية. الهدف هو تضييق قائمة طويلة من الأدوية المحتملة إلى مجموعة صغيرة وواقعية يمكن للعلماء والأطباء اختبارها فعليًا على المرضى.
إعادة استخدام الأدوية القديمة لغرض جديد
قد يستغرق تطوير دواء جديد بالكامل أكثر من عقد من الزمن ويكلف مليارات الدولارات، مع عدم وجود ضمان للنجاح. البديل هو «إعادة توظيف الأدوية»، التي تبحث عن استخدامات جديدة لأدوية معتمدة بالفعل لحالات أخرى مثل مرض باركنسون أو الاكتئاب. وبما أن هذه الأدوية لها ملفات سلامة معروفة، فغالبًا ما يمكن أن تنتقل بسرعة أكبر إلى التجارب السريرية لمرض ألزهايمر. لكن الأساليب الحاسوبية الحديثة التي تفحص قواعد البيانات البيولوجية والأدبيات الطبية تنتج الآن قوائم مرشحين هائلة — أكثر بكثير مما يمكن للباحثين تقييمه يدويًا — مما يخلق عنق زجاجة جديدًا في العملية.
جمع عدة نماذج ذكية معًا
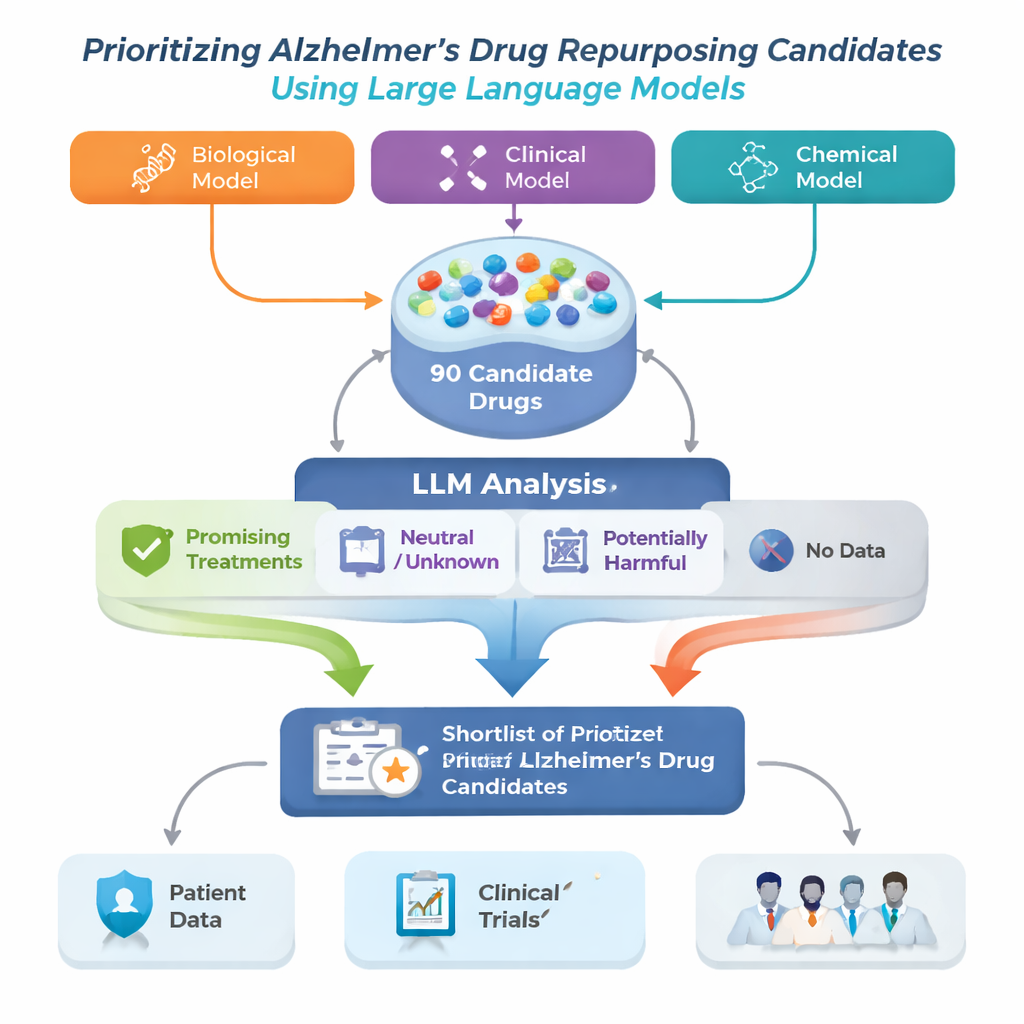
تصدى فريق البحث لهذه المشكلة من خلال بناء إطار لإعادة توظيف أدوية ألزهايمر يبدأ بثلاثة نماذج حاسوبية متقدمة مختلفة. يفحص كل نموذج «خريطة» بيولوجية كبيرة تسمى الرسم المعرفي، والتي تربط الأمراض والأدوية والجينات ومفاهيم طبية أخرى، ويقترح أدوية قد تساعد في ألزهايمر. ولأن كل نموذج يَرَ الأنماط بشكل مختلف، فإن قوائمهم لا تتطابق بالكامل. جمع المؤلفون أعلى 30 اقتراحًا من كل نموذج في مجموعة واحدة مكونة من 90 دواءً مرشحًا، ثم استخدموا نموذج لغة كبيرًا ليقوم بدور المراجع الآلي الحذر، يقرأ الدراسات المنشورة لكل دواء ويقيّم ما إذا كانت الأدلة تبدو مفيدة أو محايدة أو ضارة بالنسبة لألزهايمر.
كيف يقرأ الذكاء الاصطناعي الأدبيات الطبية
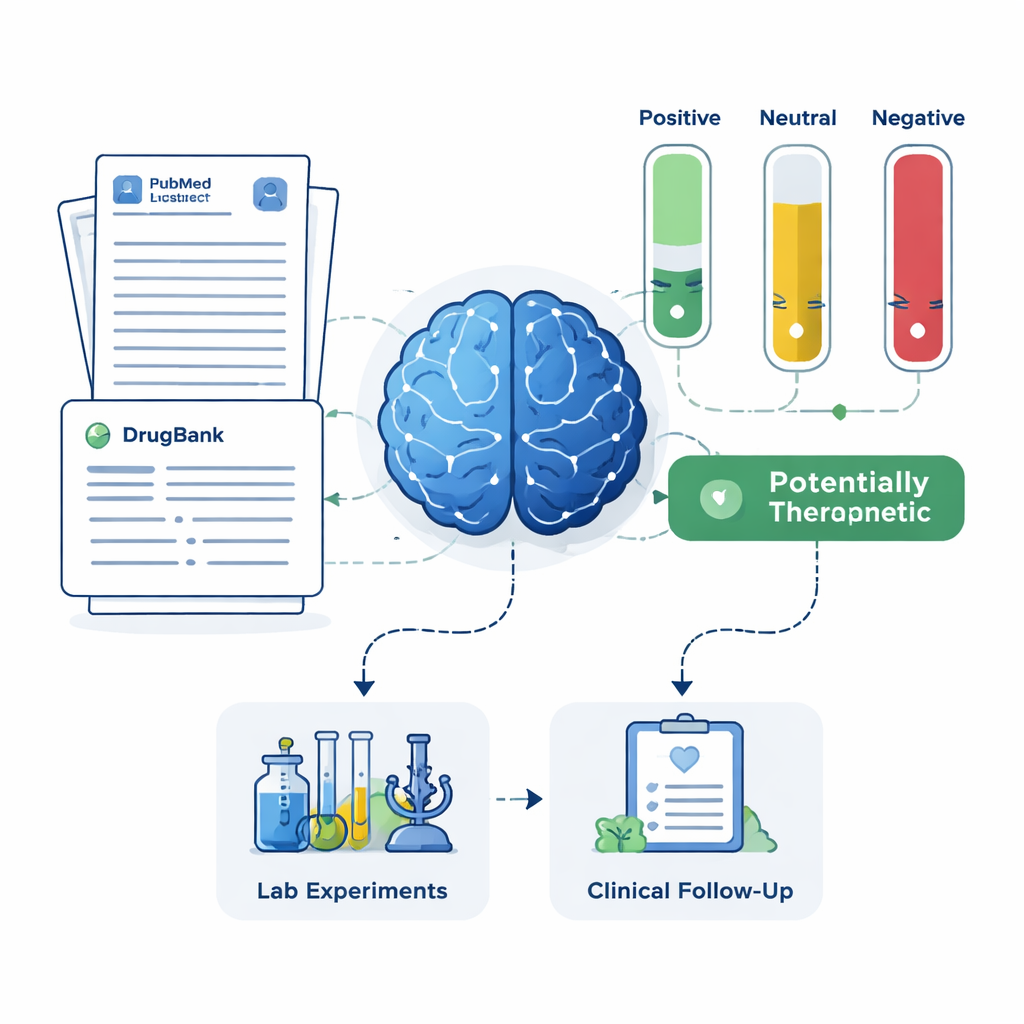
لكل دواء مرشح، سحب النظام ما يصل إلى 200 ملخص علمي من PubMed بالإضافة إلى أوصاف مفصلة للأدوية من قاعدة بيانات صيدلانية. طُلب من نموذج اللغة الكبير أن يؤسس حكمه فقط على النص المعروض له، وأن يصنف كل ملخص على أنه إيجابي أو محايد أو سلبي بالنسبة لعلاج ألزهايمر. ثم حُولت هذه التصنيفات إلى درجات بسيطة: نسبة الملخصات الإيجابية والمحايدة والسلبية. باستخدام مجموعتين من القواعد — واحدة أكثر تشددًا تطلبت دليلًا إيجابيًا واضحًا، وأخرى أكثر تساهلًا أبلغت عن أي إشارة لفائدة — صنف الإطار الأدوية إلى أربع مجموعات: علاجات واعدة، قد تكون ضارة، غير واضحة أو محايدة، وأدوية لا توجد لها أي أوراق مرتبطة بألزهايمر على الإطلاق. قد تحمل هذه المجموعة الأخيرة، رغم قلة دراستها، فرصًا جديدة خاصة.
التحقق مقابل مرضى حقيقيين والتجارب السريرية
لمعرفة ما إذا كانت القائمة القصيرة للذكاء الاصطناعي منطقية في العالم الحقيقي، قارن الفريق نتائجه بمصدرين مستقلين: سجل كبير لمرضى ألزهايمر وسجلات التجارب السريرية المسجلة. نجح الإطار في استرجاع ميمانتين، وهو دواء موجود لألزهايمر له إشارات وقائية قوية في بيانات المرضى وسجل تجريبي واسع، كمرشح عالي الأولوية. كما أبرز أدوية مثل المغنيسيوم والمينوسيكلاين والبيمافانسيرين والتستوستيرون والدوكسيسيكلين، التي لديها مستويات متفاوتة من الأبحاث الداعمة ولكنها كانت تعتبر واعدة من قبل أطباء خبراء. في الوقت نفسه، حدد النظام أدوية تُشير الأدبيات إلى احتمال إلحاق ضرر أو عدم وجود فائدة، موصيًا بتقليل أولويتها أو فحصها للتأثيرات الجانبية بدلاً من استخدامها كعلاج.
من تنبؤات الحاسوب إلى خطوات عملية لاحقة
بعبارات بسيطة، يعمل هذا الإطار مثل مساعد بحثي فائق السرعة والحذر يقرأ آلاف الأوراق، يتحقق من الأنماط عبر قواعد بيانات طبية كبيرة، ويقدّم للخبراء البشريين قائمة أقصر وأكثر تنظيمًا من مرشحي أدوية ألزهايمر للتركيز عليها. تُظهر الدراسة أنه من خلال الجمع بين أنواع مختلفة من الذكاء الاصطناعي — نماذج قائمة على الرسوم لإنتاج الأفكار ونموذج لغة لتقييم الأدلة — يمكن للباحثين العثور بسرعة أكبر على الأدوية المدعومة جيدًا وخيارات جديدة مثيرة للاختبار. وبينما لا يشفي هذا النهج ألزهايمر بحد ذاته، إلا أنه يقدم طريقة قوية جديدة لربط الأفكار المولدة حاسوبيًا بالعمل الصعب للتجارب المعملية والسريرية، مما قد يسرع الطريق نحو علاجات أكثر فعالية.
الاستشهاد: Li, M., Niu, S., Xu, Y. et al. Bridging the computational-experimental gap: leveraging large language model to prioritize Alzheimer’s therapeutics based on comparison of learning models. npj Health Syst. 3, 20 (2026). https://doi.org/10.1038/s44401-026-00074-3
الكلمات المفتاحية: مرض ألزهايمر, إعادة توظيف الأدوية, الذكاء الاصطناعي, نماذج اللغة الكبيرة, رسوم بيانية معرفية