Clear Sky Science · ar
طفرة APP E590D تزيد إنتاج ببتيدات Aβ وAη وتفاقم التاوباثي (تشابك تاو)
لماذا تهم هذه الطفرة النادرة
عادة ما يُنظر إلى داء ألزهايمر باعتباره تراكمًا بطيئًا لبروتينين ضارين في الدماغ، الأميلويد وتاو. يصاب معظم الأشخاص بالمرض دون سبب واضح واحد، لكن بعض العائلات تحمل تغييرات جينية نادرة يمكن أن تغيّر التوازن بشكل كبير. تفحص هذه الدراسة أحد هذه التغيرات غير الشائعة في جين بروتين السلف الأميلويد (APP) وتبيّن كيف يمكنها تعزيز إنتاج شظايا بروتينية سامة وتفاقم عملية تشابك التاو المعروفة بالتاوباثي. فهم هذه الحالة النادرة يقدم دلائل قد تنطبق بشكل أوسع على كيفية بدء ألزهايمر ثم تسارعه.
تغيير جيني صغير بتأثيرات كبيرة
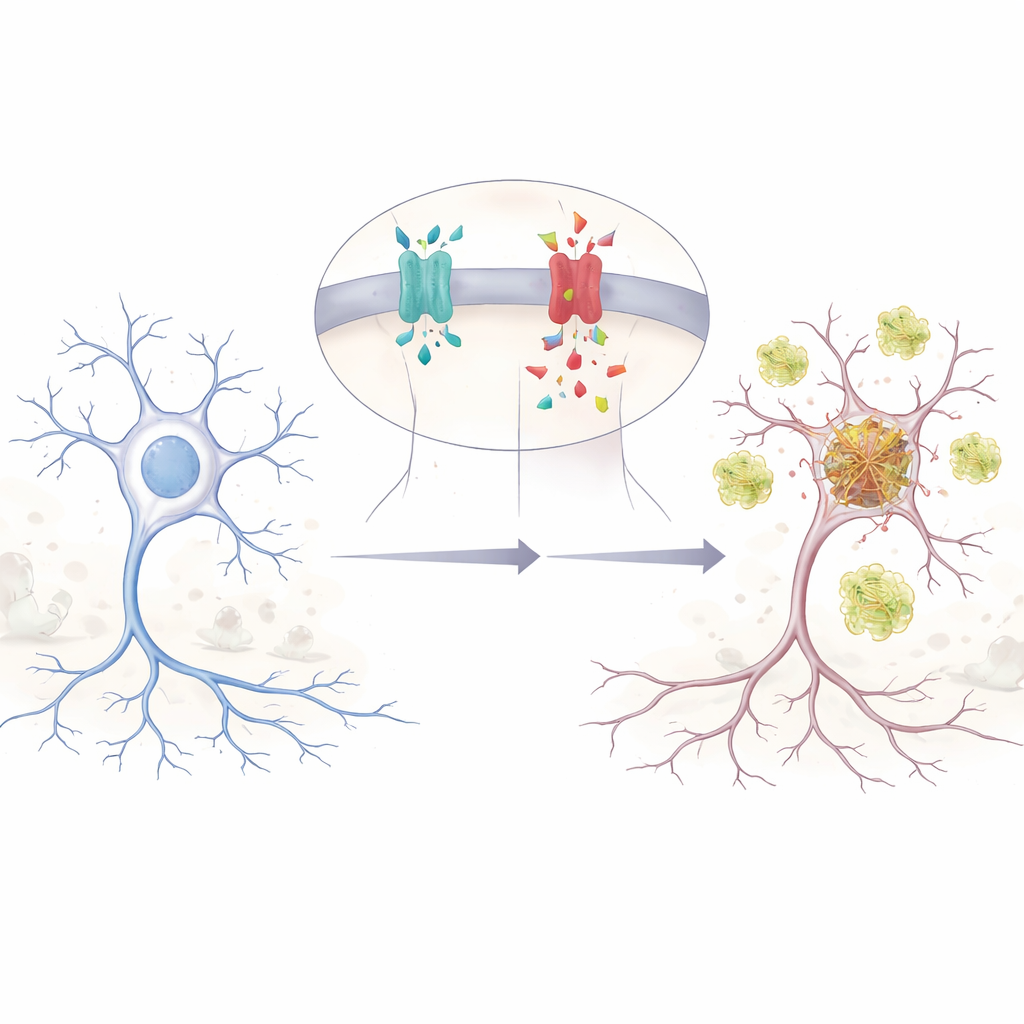
يركز المؤلفون على تغيير حرف واحد في جين APP، يُسمى E590D في الشكل الرئيسي للـ APP في المخ. تم الإبلاغ عن هذه الطفرة في شخصين فقط، كلاهما مُشخَّص بداء ألزهايمر في أعمار منخفضة نسبيًا ومع مشكلات مبكرة غير اعتيادية في الذاكرة والسلوك. وبما أنها نادرة جدًا، لم يكن العلماء متأكدين مما إذا كانت السبب الفعلي للمرض أم مجرد طيف جانبي غير ذي أثر. لاكتشاف ذلك، أعاد الفريق تركيب الطفرة في خلايا بشرية وعصبونات فأرية، ثم تتبع كيفية تقطيع APP إلى شظايا متعددة. اكتشفوا أن APP المطوّر ينتج كمية أكبر بكثير من بيتا الأميلويد (Aβ)، الببتيد اللاصق المرتبط منذ زمن طويل بألزهايمر، مقارنةً بـ APP الطبيعي عند المقارنة المنصفة للمستويات.
ببتيدان سامان بدلاً من واحد
يمكن قطع APP بعدة طرق، مثل جذع يُقَطّع عند نقاط مختلفة. المسار الكلاسيكي لمرض ألزهايمر يولد Aβ، لكن قطعًا آخر يُنتج شظية أقل شهرة تسمى Aη. أظهرت أعمال سابقة أن Aη يمكن أن يضر اتصالات الخلايا العصبية ويضعف قدرة الدماغ على تعزيز الذاكرة. في تجاربهم، وجد الباحثون أن طفرة E590D لا ترفع مستوى Aβ فحسب؛ بل تزيد أيضًا بشكل قوي من Aη ومن شظية سابقة تغذي كلا المسارين. هذا يعني أن الطفرة تُزحزح معالجة APP نحو ضربة مزدوجة من الببتيدات الضارة، مما قد يزعج دوائر الدماغ حتى قبل توقع ظهور لُويحات أميلويد الكلاسيكية.
كيف تسرّع الطفرة حركة الخلية
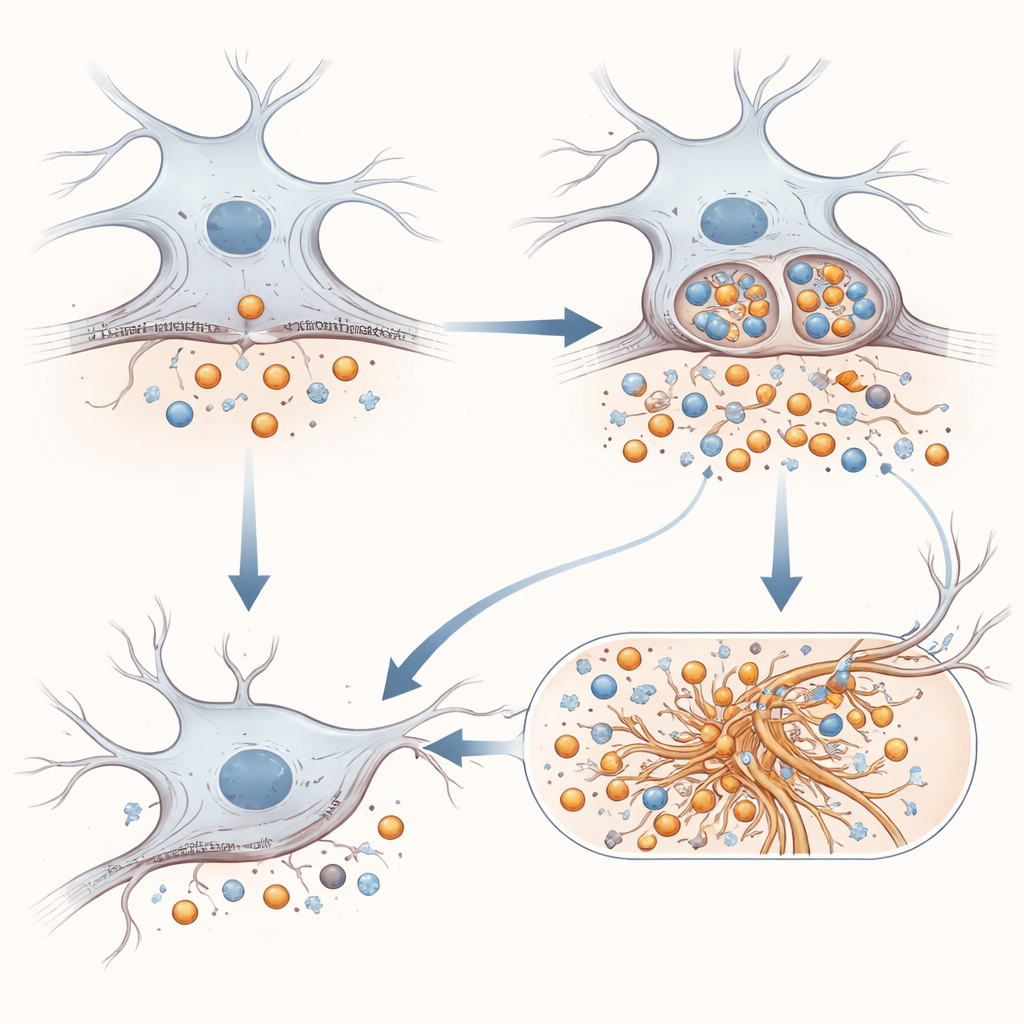
لفهم سبب إنتاج شظايا سامة أكثر، درس الفريق مكان تواجد APP وحركته على سطح الخلية. العديد من القصاصات التي تخلق Aβ تحدث فقط بعد أن يُسحب APP إلى داخل الخلية عبر عملية تسمى الالتقام الخلوي (endocytosis). باستخدام تصوير وحيل كيميائية حيوية تُعلّم البروتينات على السطح ثم تتتبع إدخالها إلى الداخل، أظهر العلماء أن APP المطوّر أقل وفرة على سطح الخلايا ويُؤخذ إلى الداخل بسرعة أكبر من APP الطبيعي. بمجرد دخوله إلى الحويصلات المبكرة (البِلاثِيات المبكرة)، يلتقي APP بالإنزيمات التي تولِّد Aβ، ويبدو أن هذا التغير في الحركة يمنح تلك الإنزيمات فرصًا أكبر للعمل. في الوقت نفسه، زاد القطع في موقع η على السطح أيضًا، مما يفسر الارتفاع في Aη.
من شظايا البروتين إلى تشابك تاو والالتهاب الدماغي
لا تتوقف القصة عند الشظايا المرتبطة بالأميلويد. اختبر الباحثون ما إذا كان APP المطوّر سيؤثر على تاو، البروتين البنيوي الذي يشكل أليافًا ملتفة في العديد من أشكال الخرف. في نماذج خلوية تتوهج عندما تتسبب بذور تاو في تشكل تكتلات تاو جديدة، أدت وجود APP E590D إلى تجمّع أقوى مقارنةً إما بـ APP الطبيعي أو بعدم وجود APP. في نموذج فأري معرض لمشكلات تاو، أدى حقن فيروس يصنع APP المطوّر في الحُصَين إلى تفاقم تشابكات تاو وتحفيز تفعيل أقوى للخلايا النجمية والميكروجليا، خلايا الدعم والمناعة في الدماغ. ومن المثير للاهتمام أن قطع الأميلويد الذائبة التقليدية كان من الصعب اكتشافها في أدمغة هذه الفئران، لكن شظية مميزة مأخوذة من APP ظهرت فقط عند وجود الطفرة، مما يشير إلى معالجة متغيرة في النسيج الحي.
ما الذي يعنيه هذا لفهم ألزهايمر
عند جمع النتائج، تظهر أن هذه الطفرة النادرة في APP ليست حميدة. إنها تدفع APP نحو توليد أكثر من ببتيد سام واحد، وتسرّع خطوات الإدخال إلى الداخل التي تُفضّل القصاصات الضارة، وتضخّم تشابك تاو والالتهاب في الدماغ. للقراء غير المتخصصين، الرسالة الأساسية هي أن بيولوجيا ألزهايمر لا يقودها عامل وحيد سيء، بل شبكة من الشظايا البروتينية المتفاعلة والاستجابات الخلوية. دراسة مثل هذه المتغيرات الجينية القوية لكن غير المألوفة توفر رؤية مكبرة لتلك الشبكة. في هذه الحالة، يمكن أن توحي بأن العلاجات قد تضطر إلى أخذ كل من الأميلويد والببتيدات البديلة المشتقة من APP مثل Aη، بالإضافة إلى تأثيرهما المشترك على تاو، في الاعتبار بدلاً من استهداف مسار واحد بمعزل.
الاستشهاد: Liu, T., Wetzel, L., Roy, D. et al. APP E590D mutation increases generation of Aβ and Aη peptides and exacerbates tauopathy. npj Dement. 2, 21 (2026). https://doi.org/10.1038/s44400-026-00069-9
الكلمات المفتاحية: داء ألزهايمر, بروتين السلف الأميلويد, تشابكات تاو, الالتهاب العصبي, طفرة جينية