Clear Sky Science · ar
ترميز الحواف الوظيفية في الرسوم البيانية لنمذجة العلاقات المتغيرة مكانيًا في بيئة الورم الدقيقة
لماذا يهم رسم خرائط حيِّ السرطان
السرطان لا ينمو بمعزل عن محيطه. تعيش خلايا الورم في حيٍّ مزدحم من الخلايا المناعية، وخلايا الدعم، والأوعية الدموية، والإشارات الكيميائية، جميعها متجمعة في الفضاء. كيف تُرتَّب هذه الجيران ومدى تأثيرهم على بعضهم البعض يمكن أن يحدد ما إذا كان السرطان سينتشر أو يستجيب للعلاج أو يبقى تحت السيطرة. تقدم هذه المقالة إطارًا جديدًا للذكاء الاصطناعي اسمه SPIFEE يحوّل الصور المجهرية والخرائط الجزيئية للأورام إلى شبكات، مما يساعد الباحثين على تحديد أي التفاعلات بين الخلايا والمسارات مرتبطة أكثر بنوع المرض ونتائج المرضى.
تحويل النسيج إلى خريطة شبكية
يمكن للدراسات السرطانية الحديثة قياس أكثر من مجرد مظهر الورم تحت الميكروسكوب. تبرز بعض الأساليب عشرات البروتينات على خلايا منفردة، وتقدّم أخرى شرائح ملونة مفصّلة لهياكل النسيج، وتُسجّل أدوات أحدث أي الجينات نشطة عبر آلاف المواضع في شريحة من الورم. يعامل SPIFEE كل هذه كمرئيات مختلفة لنفس الحي. يمثل كل عينة كرسوم بياني: العقد ترمز إلى كيانات رئيسية في بيئة الورم الدقيقة—مثل أنواع الخلايا، أو أنماط النسيج المرئية، أو المسارات الجزيئية—بينما تلتقط الحواف كيف تتفاعل هذه الكيانات عبر الفضاء. والأهم من ذلك، أن SPIFEE لا يختزل التفاعل إلى رقم واحد مثل «المسافة». بدلاً من ذلك، يخزن كل هامش منحنى صغير يصف مدى امتزاج كيانين أو تنافرهما عبر نطاق من المسافات، محافظًا بذلك على تفاصيل مكانية أغنى بكثير.
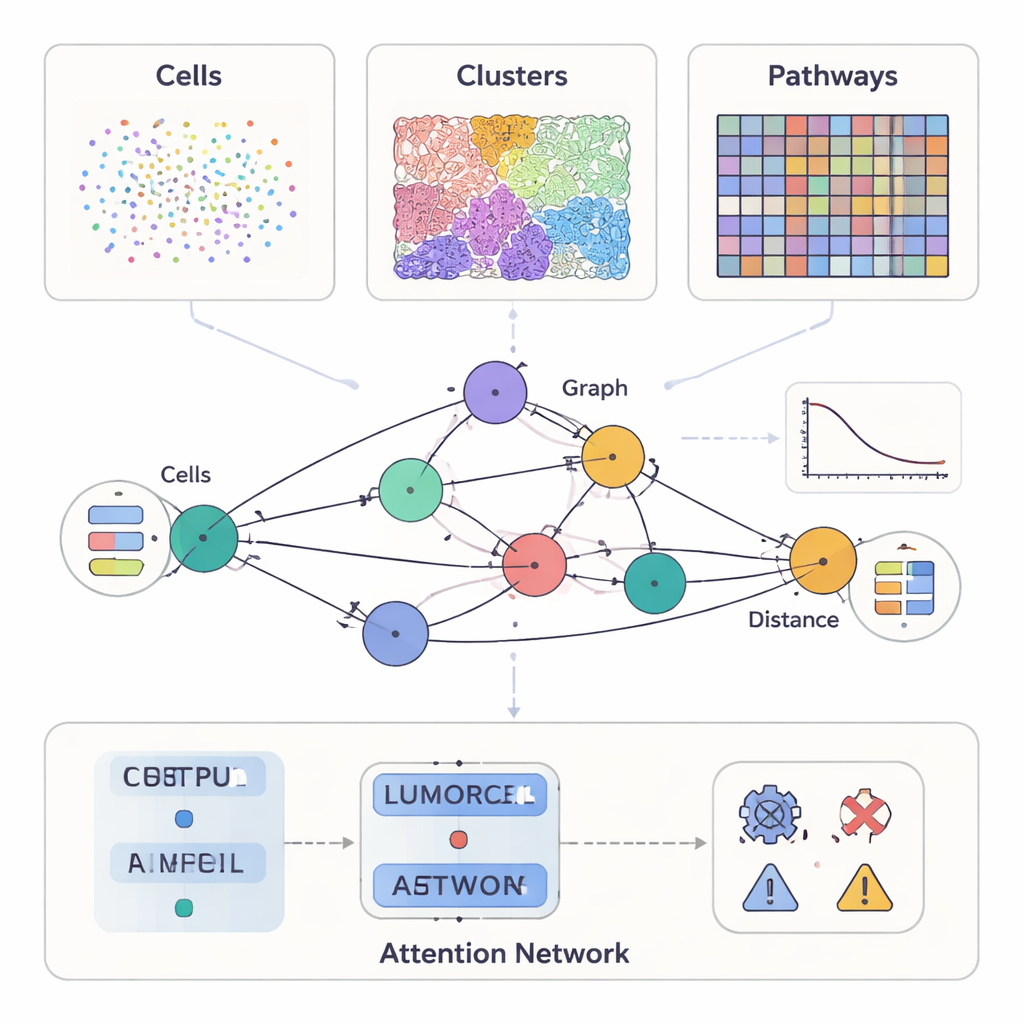
عدسة مرنة لأنواع متعددة من بيانات السرطان
اختبر المؤلفون SPIFEE على عدة مجموعات بيانات سرطانية كبيرة ومستقلة تغطي تقنيات ومقاييس مختلفة. في عينات أمراض البنكرياس المعلّمة بتلوين مناعي مضاعف، مثّل كل عقدة نوع خلية، وجاءت ميزات العقد من تسلسل الحمض النووي الريبي أحادي الخلية الذي لخص كيفية تواصل هذه الخلايا عادةً. في شرائح سرطان الرئة الملطَّخة بطريقة الهيماتوكسيلين والإيوزين الروتينية، مثّلت العقد أنماطًا بصرية متكررة للنسيج، اكتُشِفت تلقائيًا بواسطة نظام تعلّم ذاتي. في إعداد ثالث، حوّلت شرائح سرطان الرئة القياسية بأداة عميقة التعلم إلى نسخ افتراضية من النَّسخ المكانية، ومثّلت عقد SPIFEE المسارات الجزيئية مثل نقص التأكسج، والاستروجين، أو إشارة JAK–STAT، مع ميزات مستمدة من نشاط الجينات. عبر كل هذه الإعدادات، كان بالإمكان لمثل هذا الإطار استيعاب أنواع عقد مختلفة وبناء رسوم مكانية قابلة للمقارنة.
اكتشاف التفاعلات التي تفرّق نتائج الصحة
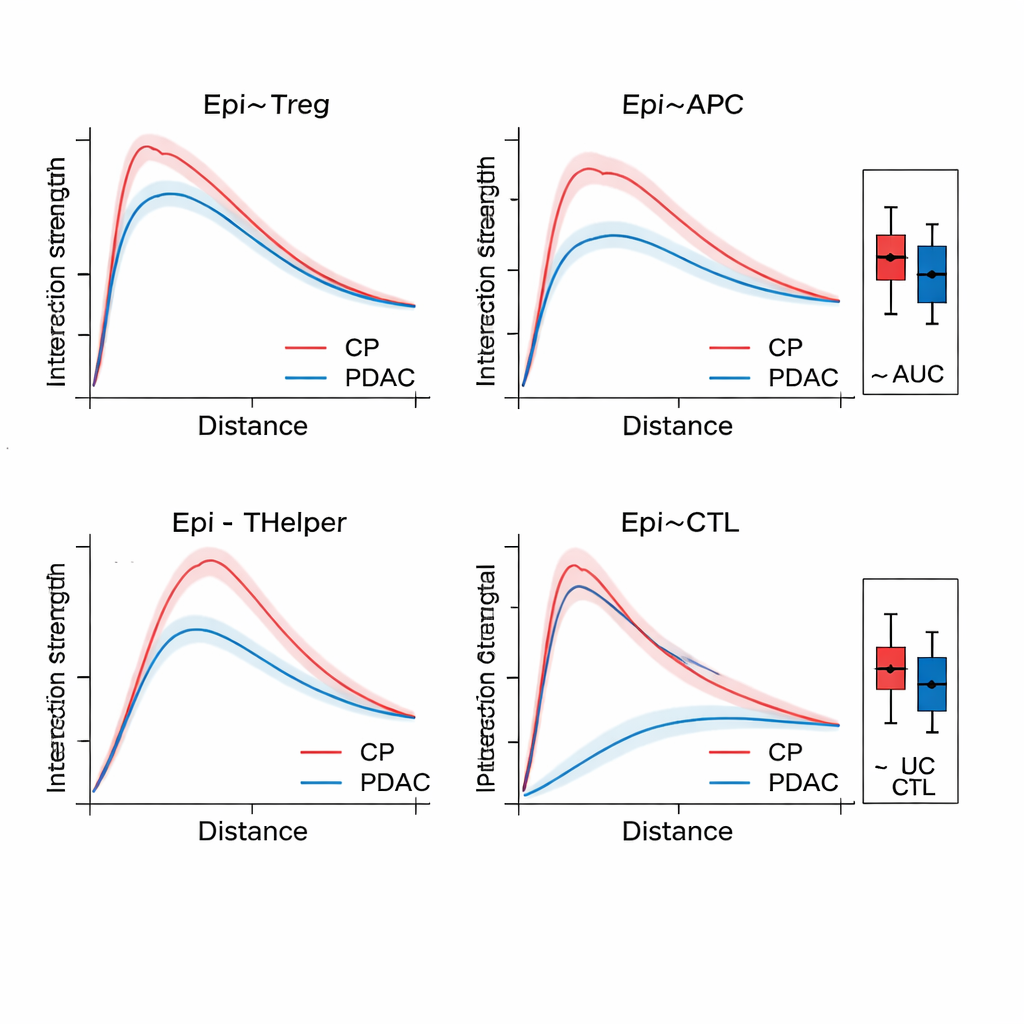
بمجرد أن يبني SPIFEE الرسم البياني، يمرره عبر شبكة انتباه بيانية، وهي نوع من الشبكات العصبية التي تتعلم ليس فقط التنبؤ بنتيجة—مثل نوع السرطان، خطر البقاء، أو المرض مقابل الالتهاب غير السرطاني—بل أيضًا إبراز أي الحواف كانت الأكثر أهمية لذلك التنبؤ. في نسيج البنكرياس، ميّز SPIFEE التهاب البنكرياس المزمن عن سرطان قناة البنكرياس بدقة أعلى من الطرق البيانية السابقة. ركز النموذج باستمرار على التفاعلات التي تشمل الخلايا الظهارية (الشبيهة بالورم) والخلايا التائية التنظيمية، والخلايا المقدمة للمستضد، والخلايا المساعدة التائية، مشيرًا إلى حي مناعي مثبط أكثر بروزًا في السرطان منه في الالتهاب. في شرائح سرطان الغدد الرئوية، حدّد SPIFEE أنماطًا خاصة من النسيج الضام-الورمية التي ارتبطت تفاعلاتها بتحسن أو تدهور البقاء، ما يوحي بأن «مناطق الحدود» بين الورم والنسيج الداعم تحمل دلائل تنبؤية مهمة قد تفوتها التحليلات المعيارية.
قراءة التبادل الجزيئي من الشرائح الروتينية
وربما الأبرز أن SPIFEE استطاع استنتاج تفاعلات مسارات ذات معنى من صور الباثولوجيا الاعتيادية بمجرد ترجمتها إلى خرائط متوقعة لنشاط الجينات. من خلال معاملة المسارات كعقد وتزامنها المكاني كحواف وظيفية، برزت أزواج مثل نقص التأكسج مع EGFR أو JAK–STAT مع PI3K—تراكيب معروفة بالفعل بدفعها للهروب المناعي ومقاومة الأدوية في سرطان الرئة. كما أبرز المسارات المرتبطة بالاستروجين في سرطان الغدد الرئوية وبعض المسارات المناعية ومسارات الإجهاد في الأورام الحرشفية، وهي نتائج تتوافق مع الأنماط المرصودة في تسلسل الحمض النووي الريبي الكتلي وفي مجموعة بيانات استقصاء نسخي مكاني مستقلة وحقيقية. هذا يوحي بأنه حتى عندما تُقَدَّر القياسات الجزيئية، فإن الأنماط المكانية في الشرائح الروتينية لا تزال تحمل إشارات قابلة للاسترداد حول كيفية تفاعل المسارات الرئيسية في الأورام الحية.
ماذا يعني هذا لرعاية السرطان المستقبلية
بالنسبة لغير المتخصص، الرسالة الأساسية هي أن SPIFEE يقدّم طريقة جديدة لقراءة «الحياة الاجتماعية» لخلايا السرطان مباشرة من الصور والخرائط الجزيئية. من خلال ترميز كيفية تغير العلاقات مع المسافة بدلاً من تسطيحها إلى درجات مفردة، وباستخدام شبكات عصبية قائمة على الانتباه لترتيب أي التفاعلات هي الأهم، يستطيع الإطار كشف تراكيب من الخلايا والأنماط النسيجية والمسارات التي تميّز أنواع السرطان وتتنبأ بالبقاء. وبينما لا تزال هذه النتائج بحاجة إلى تحقق بيولوجي وسريري، تشير نهج مثل SPIFEE إلى مستقبل يمكن أن تولّد فيه عينات الورم الروتينية ليس فقط لقطات ثابتة، بل خرائط دينامية لبؤر التفاعل التي تساعد في التوجيه التشخيصي، وتصنيف المخاطر، وفي النهاية خيارات العلاج المخصّص.
الاستشهاد: Tsang, A.P., Krishnan, S.N., Kulkarni, R. et al. Encoding functional edges in graphs to model spatially varying relationships in the tumor microenvironment. npj Artif. Intell. 2, 27 (2026). https://doi.org/10.1038/s44387-026-00075-5
الكلمات المفتاحية: بيئة الورم الدقيقة, النَّسخ المكانية, شبكات الرسوم العصبية البيانية, علم الأمراض السرطاني, تفاعلات الخلية-الخلية