Clear Sky Science · ar
توليد جزيئات ثلاثية الأبعاد مقيدة بالتفاعلات باستخدام نموذج الانتشار يتيح نمذجة فارماكوفور تعتمد على البنية لتصميم الأدوية
لماذا تصميم أدوية أفضل أمر صعب للغاية
غالبًا ما تعتمد جهود اكتشاف الأدوية الحديثة على إقناع جزيء صغير بالانزلاق داخل بروتين كما ينطبق المفتاح في القفل. لكن المفتاح يجب أن يفعل أكثر من مجرد الانسجام: يجب أن يشكل مجموعة الصحيحة من الجاذبيات الدقيقة — مثل السحبات الكهربائية الضعيفة والبقع الطاردة للماء — لكي يبقى الدواء مربوطًا بقوة وبشكل محدد. الكون الكيميائي هائل لدرجة تفوق ما تحتويه قواعد البيانات الحالية، لذا يبحث الباحثون عن طرق أذكى لاختراع مفاتيح جديدة من الصفر مع الحفاظ على أنماط التماس الحاسمة هذه.
تعليم الحاسوب ما يهم فعلاً
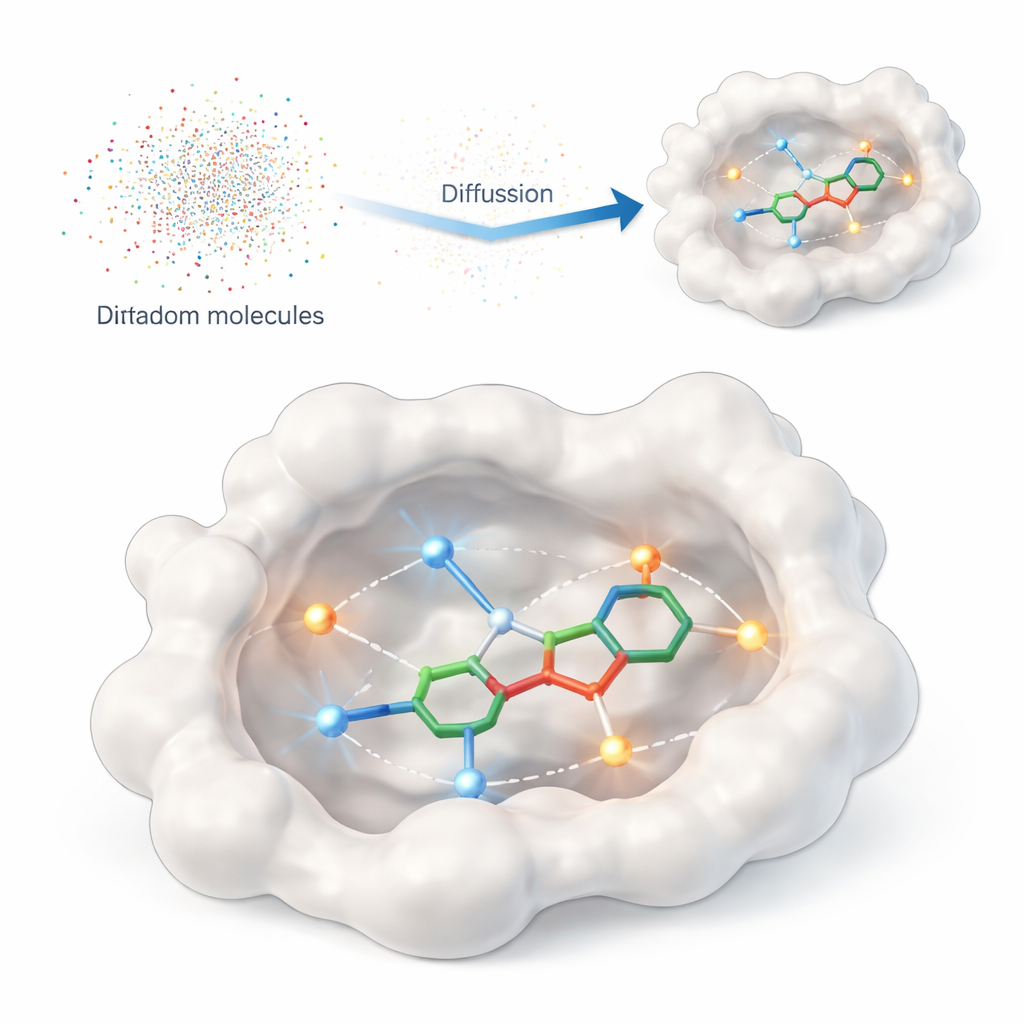
تقدم هذه الدراسة DiffPharma، إطارًا حسابيًا يولّد جزيئات شبيهة بالأدوية ثلاثية الأبعاد مباشرة داخل موقع ارتباط البروتين. بدلًا من مطالبة الخوارزمية بتفتيش فهارس ضخمة من المركبات الموجودة، يقوم DiffPharma بإنشاء جزيئات جديدة ذرّة إثر ذرّة، موجهًا بمدى تفاعلها المفترض مع البروتين. تبنى الطريقة على فئة حديثة من النماذج التوليدية تُسمى نماذج الانتشار، التي تبدأ من ضوضاء عشوائية وتقوم تدريجيًا «بتنقيتها» إلى كائن منظم — في هذه الحالة، جزيء ثلاثي الأبعاد يستقر داخل جيب البروتين.
ترميز مصافحة البروتين
لكي يخبروا النموذج بما يهم على سطح البروتين، يمثل المؤلفون التماسّات الرئيسية كـ «جسيمات تفاعل» صغيرة مرشوشة على طول المسارات بين البروتين وجزيء مرجعي. يتم التشديد على نوعين شائعين من التفاعلات: روابط الهيدروجين، التي تعمل كمغناطيسات اتجاهية بين ذرات محددة، والاتصالات الكارهة للماء حيث تتجمع المناطق الزيتية معًا مبتعدة عن الماء. تتعلم شبكات عصبية منفصلة هندسة وكيمياء كل نوع من أنواع التفاعل، بالإضافة إلى الشكل العام لجيب الارتباط، ثم تدمج بنية تكامل خاصة وجهات النظر هذه في صورة واحدة متماسكة توجه توليد الجزيء.
ما مدى محاكاتها لأنماط الارتباط الحقيقية؟
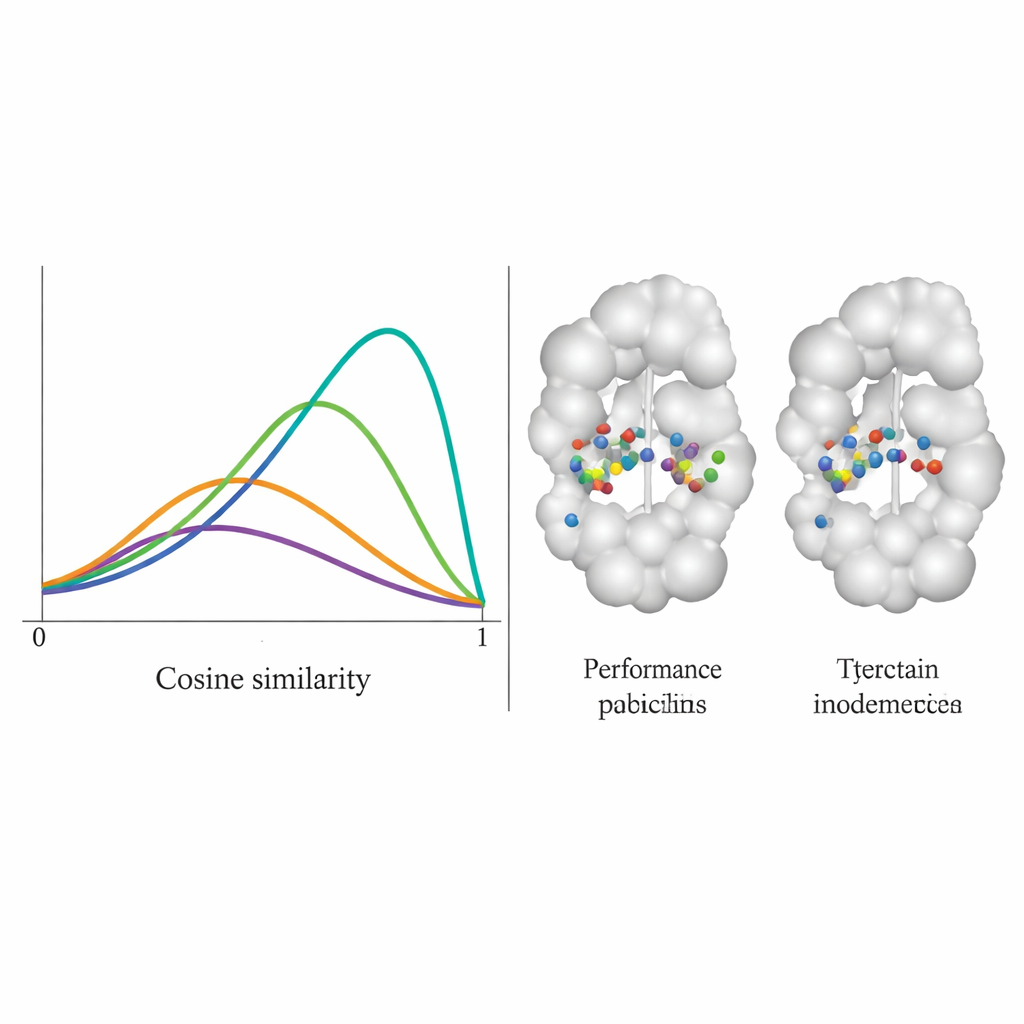
اختبر الفريق DiffPharma على 100 زوج مختلف من البروتين–الجزيء وسألوا إلى أي مدى أعادت الجزيئات الجديدة إنتاج أنماط التماس الأصلية، بقاعدة بقاعدة. قاسوا ذلك بواسطة مقياس تشابه جيب التمام (cosine similarity) بين 0 و1، حيث يعني 1 اتفاقًا تامًا. توزُّع DiffPharma بلغ ذروة حول 0.9، ما يعني أنه، في المتوسط، شكلت نفس بقايا البروتين نفس أنواع التفاعلات الرئيسية كما في الهياكل المرجعية — أفضل بكثير من ست طرق منافسة. وبشكل مهم، حقق النموذج ذلك مع الاستمرار في إنتاج تنوّع في أشكال الجزيئات، وحافظت المركبات المولدة على أطوال وروابط وزوايا ثلاثية الأبعاد واقعية نمطية للجزيئات الحقيقية والمستقرة.
من النظرية إلى مرشحات دوائية عملية
بعيدًا عن المقاييس المعيارية، سأل المؤلفون ما إذا كان DiffPharma يمكنه تصميم مرشحين دوائيين محتملين لأهداف حقيقية. بالنسبة لإنزيمين درسا جيدًا — كيناز AKT وβ‑لاكتاماز المرتبط بمقاومة المضادات الحيوية — ولّدت الطريقة جزيئات حافظت على أنماط التفاعل الأساسية للروابط المعروفة لكنها غالبًا ما استخدمت هياكل كيميائية مختلفة، وهو شكل مرغوب من «القفز بين الهياكل» في كيمياء الأدوية. في دراسة حالة أكثر تطلبًا على البروتياز الرئيسي لـ SARS‑CoV‑2، تم توجيه DiffPharma باستخدام اختيارات تفاعلية محددة ثم فحصت الجزيئات بمحاكاة الديناميكيات الجزيئية وتقديرات طاقة الارتباط. الجزيئات المولدة تحت قيود تفاعلية أشد شكلت مركبات أكثر استقرارًا وأحيانًا أظهرت طاقات ارتباط متوقعة أكثر ملاءمة من مثبط مرجعي معروف. واللافت أن النظام أعاد اكتشاف ذلك المركب المرجعي — رغم أنه لم يظهر أبدًا في التدريب — اعتمادًا فقط على بنية البروتين وتعليمات التفاعل.
ماذا يعني هذا للأدوية المستقبلية
لغير المتخصص، يمكن التفكير في DiffPharma كأداة ذكية توفر وعيًا ثلاثي الأبعاد لرسم مخططات جزيئات دوائية: بمعرفة شكل جيب البروتين ونمط «المصافحات» المرغوب، يقترح مفاتيح كيميائية معقولة تنسجم وتتفاعل بالطرق الصحيحة. وبينما لا يظلّل بعد كل خاصية يحتاجها الدواء، مثل الذائبية أو الأيض، فإن الطريقة تحافظ بثبات على خريطة التماس الحيوية على سطح البروتين وتستكشف مناطق جديدة من الفضاء الكيميائي تتجاوز الفهارس الحالية. قد تساعد هذه المقاربة الموجهة بالتفاعل الباحثين على الانتقال بسرعة أكبر من بيانات البنية عن البروتينات المرتبطة بالأمراض إلى نقاط انطلاق متنوعة وواقعية للتطوير التجريبي للأدوية.
الاستشهاد: Sako, M., Yasuo, N. & Sekijima, M. Interaction-constrained 3D molecular generation using a diffusion model enables structure-based pharmacophore modeling for drug design. npj Drug Discov. 3, 8 (2026). https://doi.org/10.1038/s44386-026-00040-x
الكلمات المفتاحية: تصميم الأدوية القائم على البنية, نماذج التوليد الجزيئية, نمذجة الفارماكوفور, تفاعلات البروتين–اليروس, البروتياز الرئيسي لـ SARS-CoV-2